Clear Sky Science · tr
Yeni pirimidin-tabanlı sulfonamid türevlerinin tasarımı, sentezi, moleküler doklanması ve sitotoksik değerlendirmesi: Güçlü antikanser ajanlar olarak SAR bulguları ve biyolojik profil
Geleceğin kanser bakımında bunun önemi
Kemoterapi ilaçları hayat kurtarabilir, ancak birçoğu sağlıklı dokulara da tümörlere yakın derecede zarar vererek şiddetli yan etkilere yol açar ve doktorların kanseri agresif biçimde tedavi etme sınırlarını kısıtlar. Bu çalışma, kanser hücrelerine sağlıklı hücrelerden daha fazla zarar vermeyi hedefleyen, vücut için hem güçlü hem daha nazik olabilecek yeni bir laboratuvar kaynaklı molekül ailesini araştırıyor. Araştırmacılar, iki iyi bilinen ilaç “yapı taşı”nın özelliklerini harmanlayarak, daha güvenli antikanser ilaçların başlangıç noktası olabilecek bileşikler sentezleyip test ettiler.
Aşina parçalarla yeni moleküller inşa etmek
Grup, modern tıpta zaten önemli roller oynayan iki kimyasal aileye odaklandı. Bunlardan biri başlangıçta antibiyotik olarak ün kazanmış, ancak günümüzde glokomdan yüksek tansiyona ve kansere kadar çeşitli durumlarda kullanılan bir ilaç sınıfı olan sulfonamidler. Diğeriyse, DNA’mızın bir parçasını oluşturan ve hücrelerin genetik materyallerini kopyalama süreçlerini bozabildikleri için antikanser ilaçlarda yaygın olarak kullanılan halka şeklinde yapılar olan pirimidinler. Araştırmacıların fikri, kanser hücrelerinin bölünmeye bağımlı süreçlerini daha iyi tanıyıp bozabilecek tek bir hibrit molekül içinde bu iki motifi birleştirmekti.
Tezgâh kimyasından aday kütüphanesine
Basamaklı organik sentez kullanarak bilim insanları çeşitli pirimidin-tabanlı sulfonamid bileşiklerinden oluşan bir kütüphane oluşturdu. Çekirdek iskeleti triazoller, pyrazoller, tiazoller ve triazinler gibi farklı çevre halkalarıyla bağlayarak elektronik yük, şekil ve yağda çözünürlük gibi özellikleri ayarladılar. Bu özellikler bir molekülün hücre zarlarını ne kadar iyi geçebileceğini, hedefe ulaşma yeteneğini ve tuzağa düşme ya da hızla atılma eğilimlerini belirlemeye yardımcı olur. Her yeni yapı standart kimyasal analiz araçlarıyla dikkatle doğrulandı; böylece biyolojik testlere geçilmeden önce araştırmacıların ne yaptıklarını tam olarak bilmesi sağlandı.
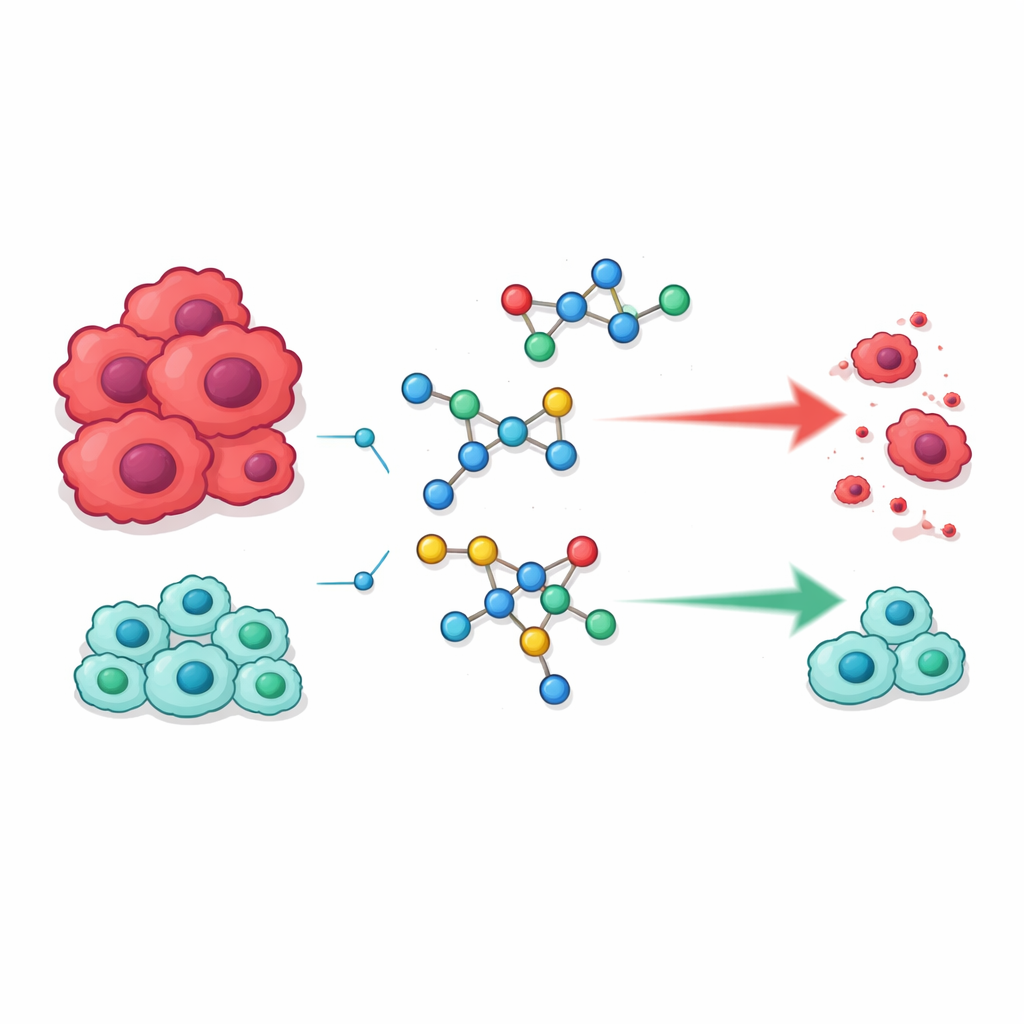
Yeni bileşikleri teste sokmak
Yeni moleküller, hem etkinlik hem de güvenlik değerlendirmesi için iki insan kanser hücre hattına—HepG2 (karaciğer) ve MCF‑7 (meme)—ve iki normal hücre türüne, WI‑38 akciğer fibroblastlarına ve VERO böbrek hücrelerine karşı tarandı. Birkaç aday öne çıktı. 18, 21, 23 ve 24 olarak etiketlenen dört bileşik, yaygın kullanılan ilaç 5‑florourasil ile benzer veya daha düşük konsantrasyonlarda kanser hücrelerini öldürdü. Ancak 5‑florourasilin aksine, bu bileşikler normal hücrelere belirgin şekilde daha az zarar veriyordu; bu da etkililik ve toksisite arasında daha elverişli bir denge olduğuna işaret ediyor. Serinin diğer üyeleri, belirli faydalı özelliklerden yoksun olduklarında çok daha zayıf aktivite gösterdi; bu da antikanser etkilerin küçük yapısal değişimlere karşı ne kadar hassas olduğunu vurguluyor.
En güçlü adayları farklı kılan nedir
Yapılar ve test sonuçları karşılaştırılarak nelerin en iyi çalıştığına dair erken kurallar ortaya kondu. En aktif bileşikler genellikle çekirdek iskelete elektron yoğunluğu veren küçük gruplar taşıyordu; bu da moleküllerin biyolojik hedefleriyle etkileşimini iyileştiriyor. Ayrıca, hücre zarlarından geçebilmeleri için yeterli, ancak her şeyi yapışkanlaştırmayacak kadar aşırı olmayan “tam yerinde” bir lipofiliklik düzeyine sahiptiler. Şekilleri de aktif bölgeler yakınındaki hantal engellerden kaçınıyor, böylece bağlanma bölgelerine daha sıkı bir uyum sağlıyordu. Bu özellikler hem kanser hücresi öldürücü gücü artırıyor hem de normal hücreleri daha çok koruyor gibi görünerek moleküllerin tümörlerin bağımlı olduğu yollara daha seçici şekilde yönelmiş olabileceğini düşündürüyor.
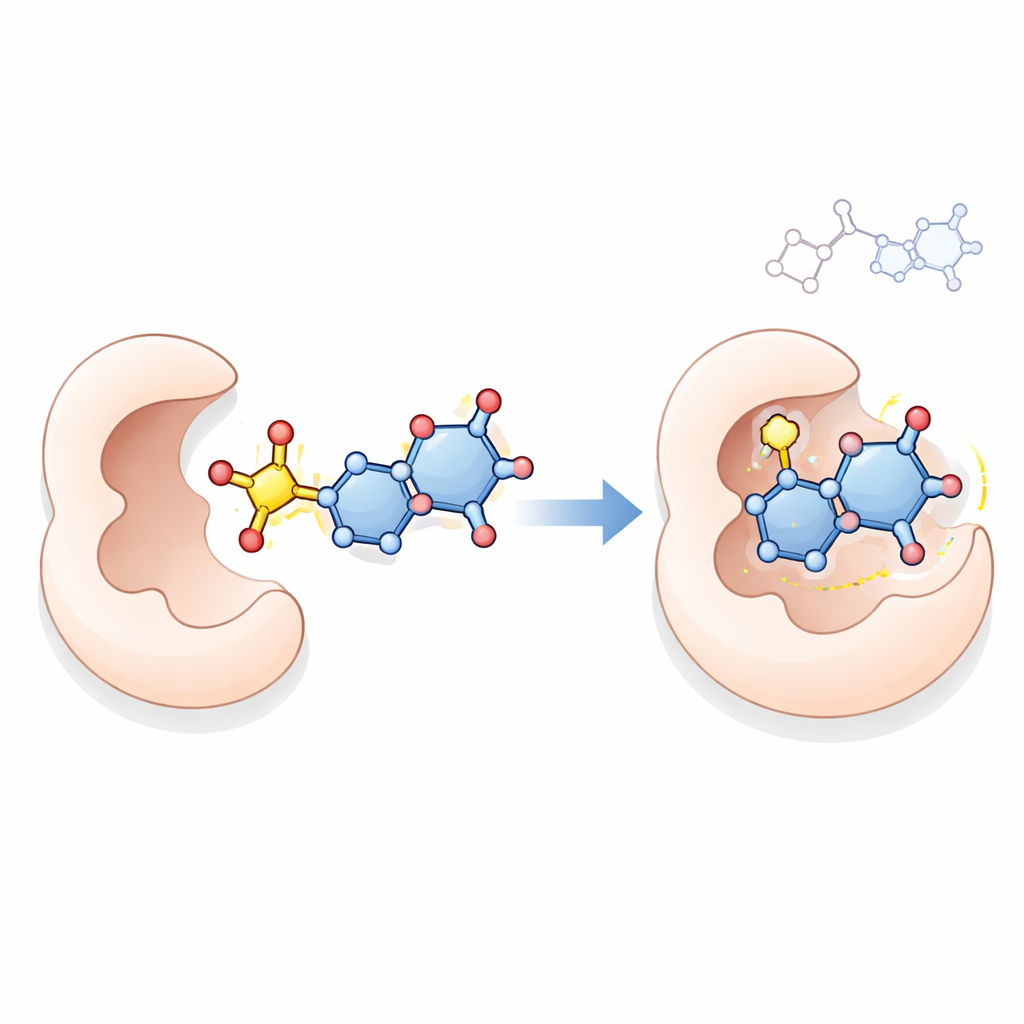
Nasıl çalışıyor olabilirler: daha yakından bakış
Olası bir etki mekanizmasını araştırmak için ekip, küçük bir molekülün bir proteinin aktif bölgesine nasıl oturabileceğini simüle eden bilgisayar tabanlı moleküler doklanma tekniğini kullandı. En iyi bileşikler olan 18, 21, 23 ve 24’ün, kanser hücrelerinin DNA yapmak için ihtiyaç duyduğu ve 5‑florourasil gibi ilaçların bilinen hedefi olan timidilat sentaz ile nasıl etkileştiği incelendi. Simülasyonlar, özellikle 23 numaralı bileşiğin, enzim cebindeki birden çok stabilize edici temas kurabildiğini ve bazı durumlarda referans ilaçtan daha güçlü bağlanma gösterebildiğini öne sürdü. Doklanma tek başına bileşiklerin canlı hücre içindeki çalışma şeklini kanıtlayamaz, ancak güçlü antiproliferatif etkileriyle tutarlı, makul bir açıklama sunuyor.
İleriye dönük anlamı
Genel olarak bu çalışma, karaciğer ve meme kanseri hücrelerine karşı güçlü aktivite ile normal hücreler üzerinde daha hafif etkileri birleştiren dört lider molekül sunuyor ve bu dengenin arkasındaki yapısal özelliklere dair erken ipuçları veriyor. Günlük ifadeyle, araştırmacılar hem etkili hem de sağlıklı dokuya daha nazik olabilecek yeni nesil kemoterapi adayları için kimyasal bir taslak çizdiler. Enzimlerde, bütün hücrelerde ve nihayetinde hayvan modellerinde daha ileri çalışmalar gerekecek, ancak bu pirimidin‑sulfonamid hibritleri daha hedefe yönelik ve tolere edilebilir kanser tedavilerine doğru ümit verici bir adımı işaret ediyor.
Atıf: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Anahtar kelimeler: antikanser ilaçlar, sulfonamidler, pirimidin hibritleri, timidilat sentaz, moleküler doklanma