Clear Sky Science · ja
新規ピリミジン系スルホンアミド誘導体の設計、合成、分子ドッキングおよび細胞毒性評価:抗がん剤としての有効性、構造活性相関と生物学的プロファイリング
将来のがん治療にとっての意義
化学療法薬は命を救うことがある一方で、多くは腫瘍とほぼ同程度に健康な組織にもダメージを与え、強い副作用を引き起こし、医師が治療をどれだけ積極的に行えるかを制限します。本研究は、健常細胞よりもがん細胞を強く標的にできるよう設計された新しい一連の合成分子を探り、強力でありながら体にやさしい治療法を目指しています。研究者らは、よく知られた二つの医薬品“構成要素”を組み合わせることで、より安全な抗がん薬の出発点となり得る化合物を作成・評価しました。
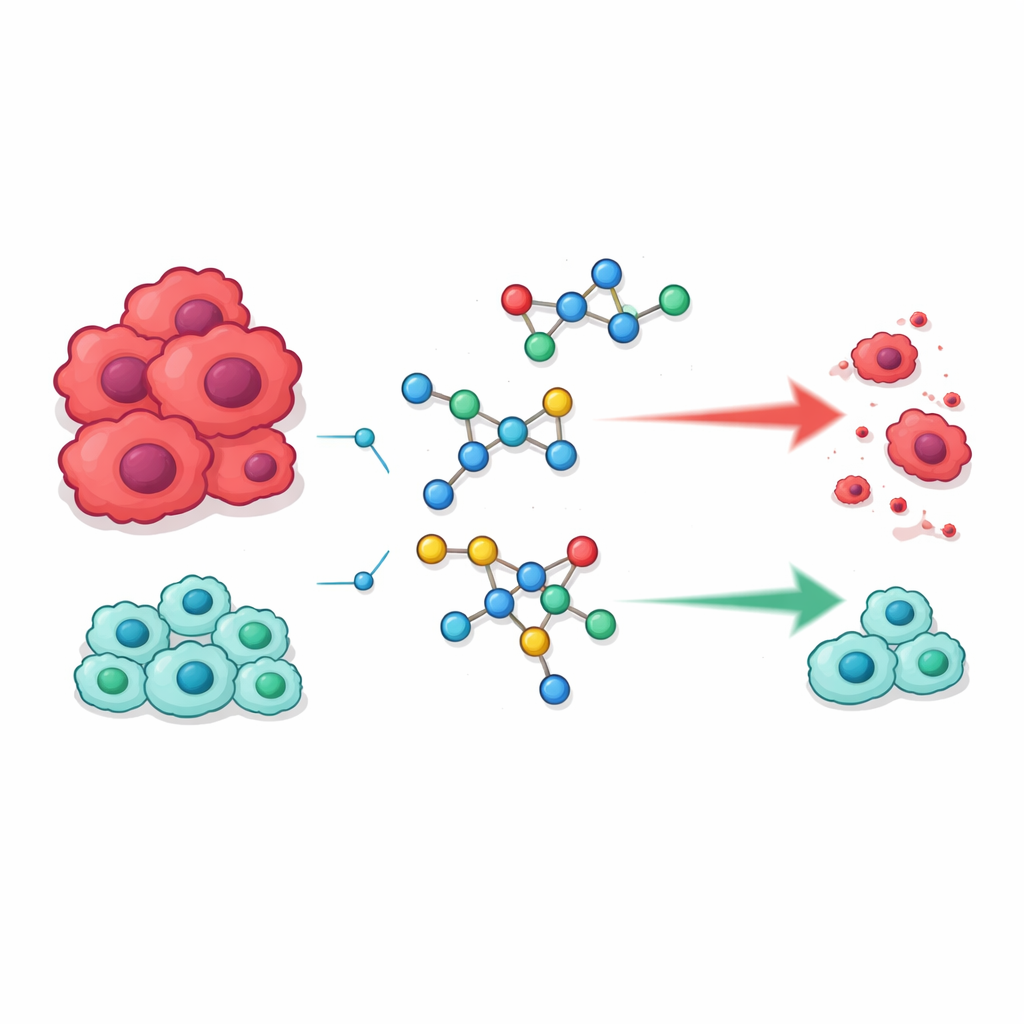
馴染みある要素から新しい分子を構築する
研究チームは、すでに医療で重要な役割を担っている二つの化学族に注目しました。一つはスルホンアミドで、当初は抗生物質として有名でしたが、現在では緑内障や高血圧、がん治療薬など幅広い薬剤に含まれています。もう一つはピリミジンで、環状構造がDNAの一部を形成し、細胞が遺伝情報を複製する過程に干渉できるため抗がん薬で広く用いられます。研究者らのアイデアは、これら二つのモチーフを単一のハイブリッド分子に融合させ、がん細胞の分裂に依存するプロセスをよりよく認識・阻害できる分子を作ることでした。
基礎実験から候補化合物ライブラリへ
段階的な有機合成を用いて、研究者は多様なピリミジン系スルホンアミド化合物のセットを合成しました。コアフレームワークをトリアゾール、ピラゾール、チアゾール、トリアジンなどの異なる周辺環状系につなぐことで、電子特性、分子形状、脂溶性などの性質を調整しました。これらの特徴は、分子が細胞膜をどれだけ通過できるか、標的に到達できるか、あるいはトラップされたり洗い流されたりしにくいかを左右します。各新規構造は標準的な化学解析手法で慎重に確認され、次の生物学的試験に進む前に正確に何が作られたかが明らかにされました。
新規化合物の試験
新規分子は、二つのヒトがん細胞株(肝がん由来のHepG2と乳がん由来のMCF‑7)および二種類の正常細胞(肺線維芽細胞のWI‑38と腎細胞のVERO)に対してスクリーニングされ、効果と安全性の両面が評価されました。いくつかの候補が際立ちました。化合物18、21、23、24の四つは、広く使用される薬剤である5‑フルオロウラシルと同程度かそれ以下の濃度でがん細胞を死滅させました。しかし、5‑フルオロウラシルとは異なり、これらの化合物は正常細胞に対しては明らかに低い有害性を示し、有効性と毒性のバランスがより好ましいことが示唆されました。役立つ特徴を欠く系列の他の化合物は活性が大幅に弱く、小さな構造変化が抗がん効果に与える影響の敏感さを裏付けました。
最も有望な候補が異なる点
構造と試験結果を比較することで、著者らは何が効果的かに関する初期的な規則をまとめました。最も活性の高い化合物は、コア骨格へ電子を供与する小さな置換基を持つ傾向があり、これが分子と生物学的標的との相互作用を改善しました。また、膜透過のために十分な脂溶性を持ちつつ、過度に脂質親和性が高くて非特異的に付着してしまうほどではない「ほどよい」脂溶性を示しました。さらに、活性領域近傍に大きな障害を作らない形状を保ち、結合部位にぴったり収まれることが多かったです。これらの特性は、がん細胞への殺傷力を高めつつ正常細胞の保護にも寄与しているように見え、腫瘍が依存する経路をより選択的に狙っている可能性を示唆します。
作用機序の考察
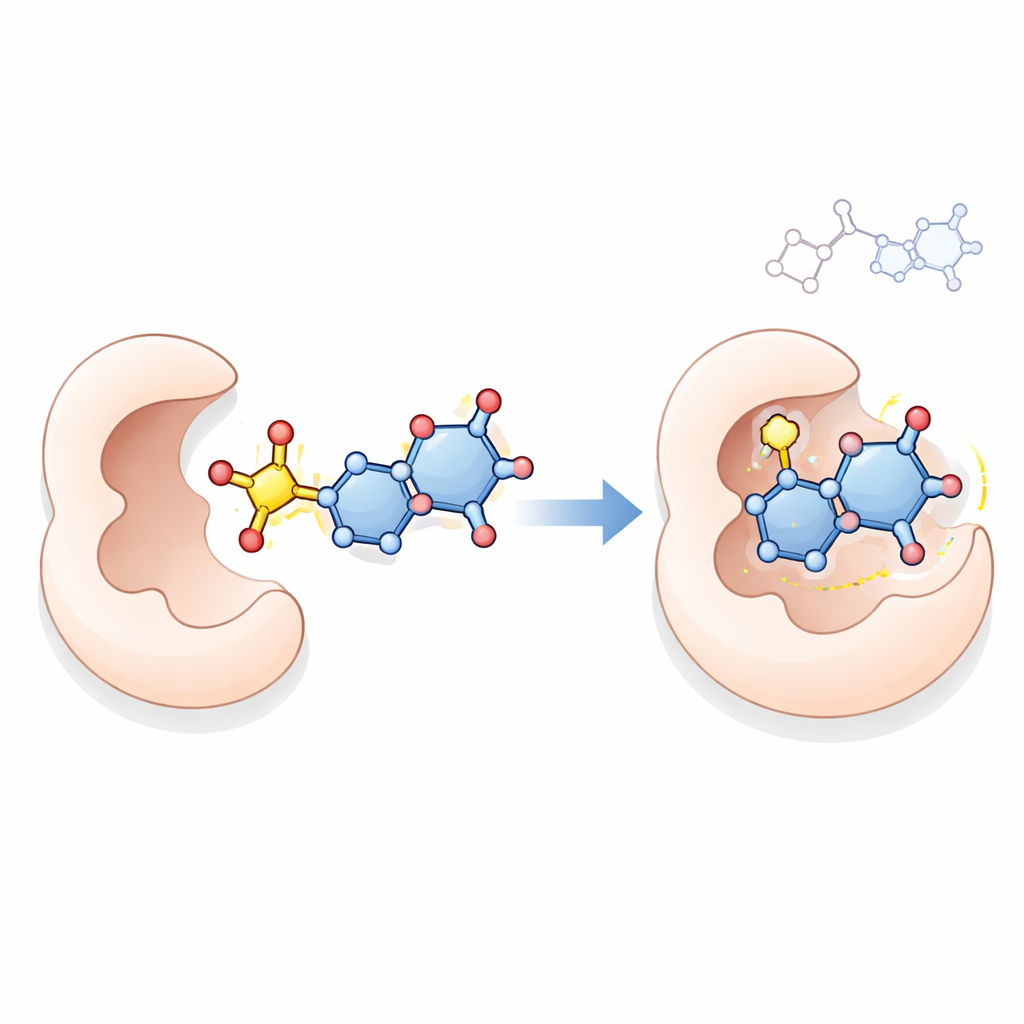
可能な作用機序を探るために、研究チームはコンピュータベースの分子ドッキングを用いて、小分子がタンパク質の活性部位にどのように収まるかをシミュレートしました。彼らは上位の化合物18、21、23、24が、DNA合成に必要ながん細胞の主要酵素であり、5‑フルオロウラシルの既知の標的でもあるチミジル酸合成酵素とどのように相互作用するかを調べました。シミュレーションは、特に化合物23が酵素のポケット内で複数の安定化相互作用を形成し、場合によっては参照薬よりも強く結合する可能性を示唆しました。ドッキングだけで生細胞内での作用を証明することはできませんが、これらの結果は強い増殖抑制効果と整合するもっともらしい説明を提供します。
今後の展開が意味するもの
総じて、本研究は肝がんおよび乳がん細胞に対して強い活性を示しながら正常細胞への影響は穏やかな四つのリード化合物と、このバランスを支える構造的特徴に関する初期の手がかりを提示します。わかりやすく言えば、研究者らは次世代の化学療法候補のための設計図を描き、効果的でありながら健常組織に優しい可能性を示しました。酵素アッセイ、全細胞、最終的には動物実験でのさらなる検証が必要ですが、これらのピリミジン‑スルホンアミドハイブリッドは、より標的化され耐容性の高いがん治療へ向けた有望な一歩を示しています。
引用: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
キーワード: 抗がん薬, スルホンアミド, ピリミジンハイブリッド, チミジル酸合成酵素, 分子ドッキング