Clear Sky Science · he
עיצוב, סינתזה, דוקינג מולקולרי והערכה ציטוטוקסית של נגזרות סולפונאמיד חדשות מבוססות פירימידין כסוכנים אנטי‑סרטניים חזקים: תובנות SAR ופרופיל ביולוגי
מדוע הדבר חשוב לטיפול בסרטן בעתיד
תרופות כימותרפיה יכולות להציל חיים, אך רבות מהן פוגעות ברקמות תקינות כמעט באותה מידה כמו בגידולים, מה שמוביל לתופעות לוואי קשות ומגביל את עוצמת הטיפול האפשרית. המחקר הזה בוחן משפחה חדשה של מולקולות מעבדתיות שנועדו לפגוע בתאי סרטן ביתר שאת מאשר בתאים בריאים, במטרה לפתח טיפולים שיהיו גם עוצמתיים וגם עדינים יותר לגוף. על ידי שילוב תכונות משני "לבני בניין" ידועים בביומדיסין, החוקרים יצרו וניסו תרכובות שעשויות לשמש נקודת התחלה לתרופות אנטי‑סרטניות בטוחות יותר.
בניית מולקולות חדשות מחלקים מוכרים
הצוות התרכז בשתי משפחות כימיות שכבר ממלאות תפקידים מרכזיים ברפואה המודרנית. אחת מהן היא סולפונאמידים, קלאס מוקדם של תרופות שזכו לפרסום כתרופות אנטיביוטיות אך מופיעות כיום בתרופות למצבים שונים, החל מגלוקומה ועד לחץ דם וסרטן. השנייה היא פירימידינים, מבנים טבעתיים שהם חלק מה‑DNA שלנו ומשמשים תרופות אנטי‑סרטניות מכיוון שהם יכולים להפריע לאופן שבו תאים משכפלים את החומר הגנטי שלהם. הרעיון של החוקרים היה למזג את שני המוטיבים האלה למולקולות היברידיות בודדות שעשויות לזהות ולהפריע יותר ביעילות לתהליכים שתאי סרטן מסתמכים עליהם לחלוקה.
מכימיה במבחנה לספרייה של מועמדים
באמצעות סינתזה אורגנית שלב‑אחר‑שלב, המדענים בנו מערך מגוון של תרכובות סולפונאמיד מבוססות פירימידין. על ידי קישור השלד המרכזי למערכות טבעתיות שונות — כגון טריאזולים, פיאזולים, תיאזולים וטריאזינים — כוונו תכונות כמו מטען אלקטרוני, צורה ושומניות. תכונות אלה קובעות עד כמה טוב מולקולה יכולה לעבור דרך ממברנות תאים, להגיע ליעד שלה ולהמנע מלכידה או שטיפה. כל מבנה חדש אומת בקפידה באמצעות כלים סטנדרטיים של ניתוח כימי, כדי להבטיח שהחוקרים ידעו בדיוק מה יצרו לפני שמתקדמים לניסויים ביולוגיים.
בדיקת התרכובות החדשות
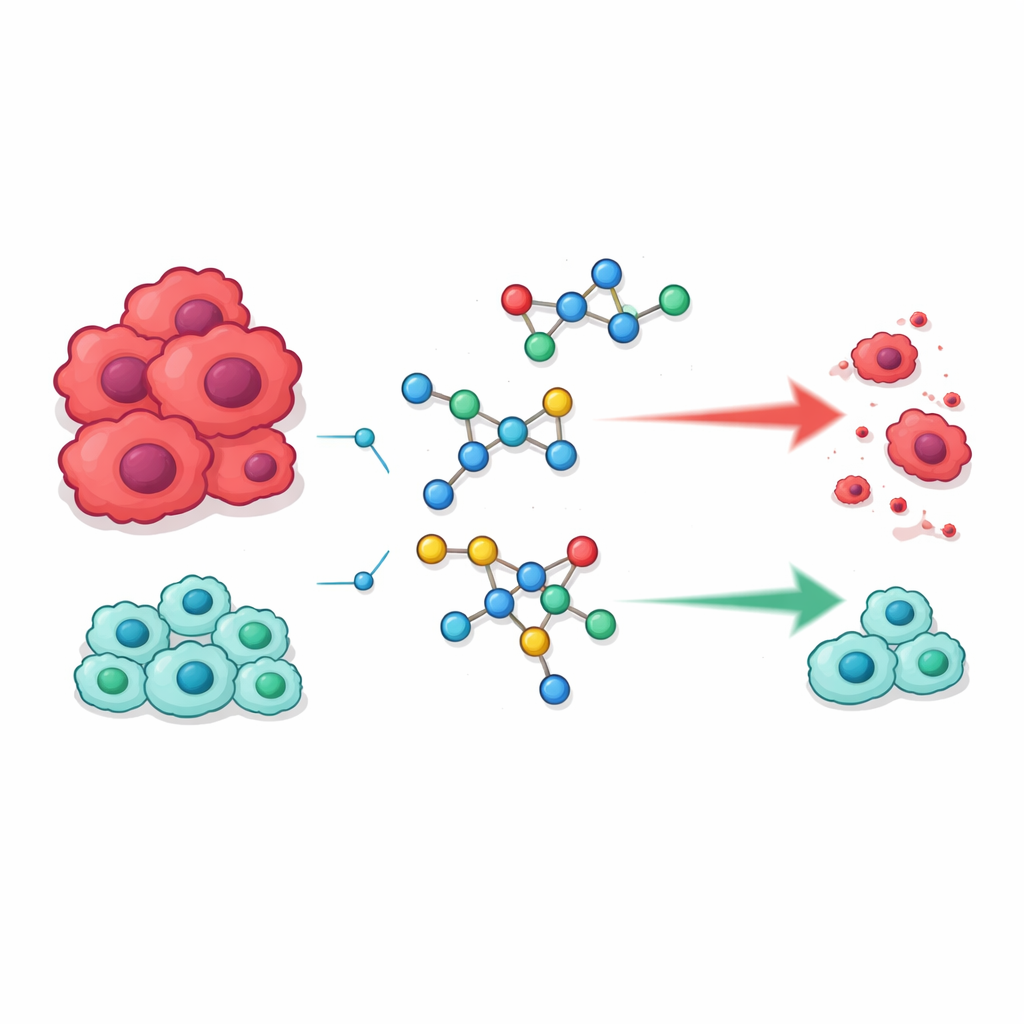
המולקולות החדשות נסקרו נגד שני תאי סרטן אנושיים — HepG2 (כבד) ו‑MCF‑7 (שד) — וכמו כן נגד שני סוגי תאים נורמליים, פיברובלסטים ריאתיים WI‑38 ותאי כליה VERO, כדי להעריך גם עוצמה וגם בטיחות. מספר מועמדים בלטו. ארבע תרכובות, שמסומנות 18, 21, 23 ו‑24, הרגו תאי סרטן בריכוזים דומים או נמוכים מאלה הנדרשים לתרופה הנפוצה 5‑פלואורואורציל. עם זאת, בניגוד ל‑5‑פלואורואורציל, אותן תרכובות היו פחות מזיקות באופן בולט לתאים נורמליים, מה שמרמז על איזון עדיף בין יעילות לרעילות. חברים אחרים בסדרה שלקו בחוסר תכונות מועילות הראו פעילות חלשה יותר, מה שמדגיש עד כמה ההשפעות האנטי‑סרטניות רגישות לשינויים מבניים קטנים.
מה מבדיל את המועמדים החזקים ביותר
על ידי השוואת מבנים ותוצאות הניסויים, המחברים הרכיבו כללי יסוד מוקדמים לגבי מה עובד הכי טוב. התרכובות הפעילות ביותר נטו לשאת קבוצות קטנות המעניקות צפיפות אלקטרונית לשלד המרכזי, מה שמשפר את האינטראקציה של המולקולות עם היעדים הביולוגיים שלהן. הן הראו גם רמת שומניות "בדיוק־נכון" — מספיק משכה לשומנים כדי לחדור ממברנות תאים, אך לא כל כך שומניות עד שהן נדבקות באופן לא ספציפי לכל דבר. בנוסף, צורתן הימנעה ממכשולים גדולים באזורים הפעילים, מהאפשר התאמה הדוקה לאתרי קשירה. תכונות אלה נראו כמגבירות הן כוח חיסול תאי הסרטן והן חסכון בתאים נורמליים, מה שמרמז שהמולקולות עלולות להתמקד באופן סלקטיבי יותר במסלולים שהתאים הסרטניים תלויים בהם.
מבט קרוב יותר על מנגנון אפשרי
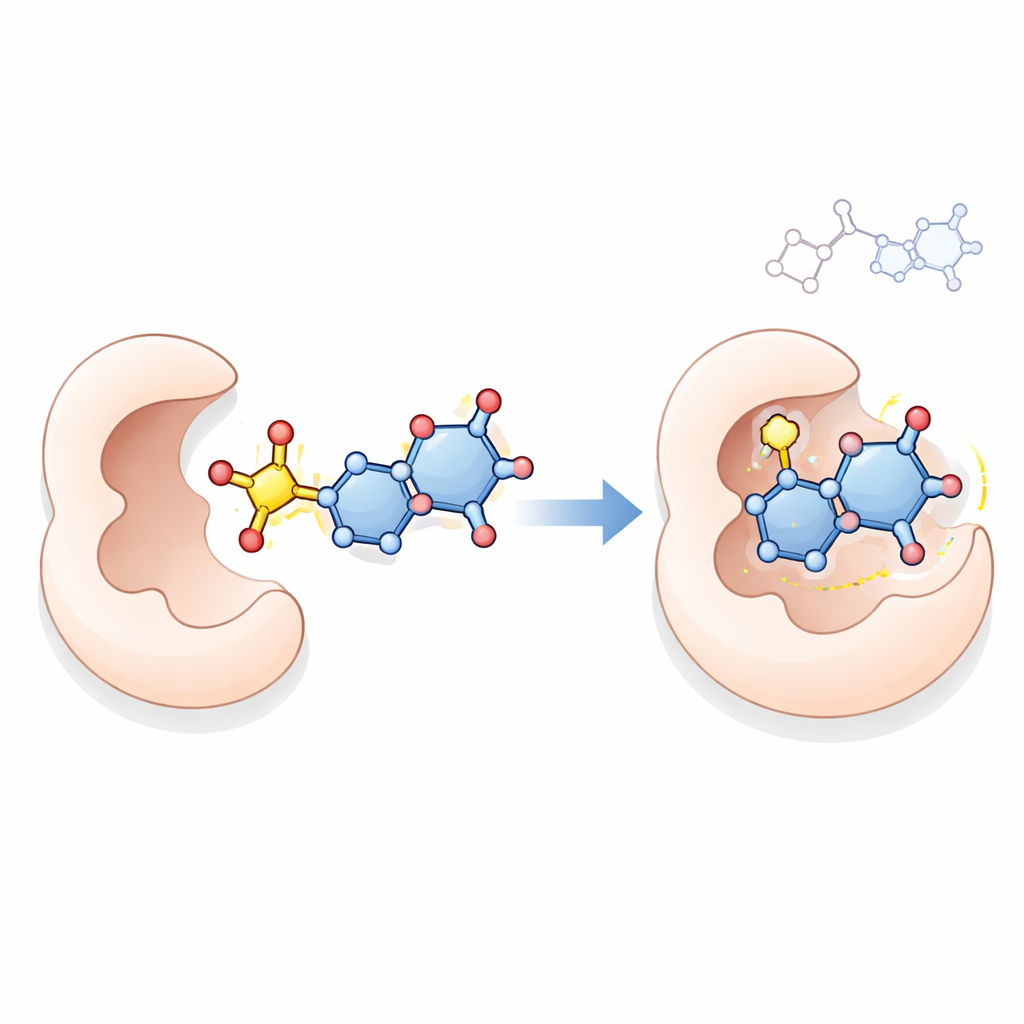
כדי לחקור מצב פעולה אפשרי, הצוות השתמש בדוקינג מולקולרי מבוסס מחשב, טכניקה המדמה כיצד מולקולה קטנה עשויה לשבת בתוך האתר הפעיל של חלבון. הם בדקו כיצד התרכובות המובילות 18, 21, 23 ו‑24 אינטראקט עם תימידילאט סינתאז, אנזים מפתח שנדרש לתאים סרטניים ליצירת DNA וידוע כיעד של תרופות כמו 5‑פלואורואורציל. הסימולציות הציעו שהת molecules החדשות הללו, ובמיוחד התרכובת 23, יכולות ליצור מספר קשרים מייצבים בתוך הכיס של האנזים, ובחלק מהמקרים לקשור בעוצמה רבה יותר מהתרופה הייחוס. אמנם דוקינג לבדו אינו יכול להוכיח כיצד התרכובות פועלות בתאים חיים, אך הוא מציע הסבר סביר התואם להשפעות האנטי‑פרוליפרטיביות החזקות שלהם.
מסקנות והמשך הדרך
בסך הכל, עבודה זו מספקת ארבע מולקולות מובילות שמשלבות פעילות עוצמתית נגד תאי סרטן כבד ושד עם השפעות מתונות יותר על תאים נורמליים, יחד עם רמזים ראשוניים לגבי התכונות המבניות שמניעות את האיזון הזה. במילים פשוטות, החוקרים שרטטו תוכנית כימית למועמדי כימותרפיה מדור הבא שעשויים להיות גם יעילים וגם עדינים יותר לרקמות בריאות. נדרש מחקר נוסף על אנזימים, בתאים שלמים ולבסוף בבעלי חיים, אך ההיברידים של פירימידין‑סולפונאמיד האלה מהווים צעד מבטיח לקראת טיפולים ממוקדים ומסבלנים יותר בסרטן.
ציטוט: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
מילות מפתח: תרופות אנטי‑סרטניות, סולפונאמידים, היברידים של פירימידין, תימידילאט סינתאז, דוקינג מולקולרי