Clear Sky Science · es
Diseño, síntesis, acoplamiento molecular y evaluación citotóxica de nuevos derivados sulfonamídicos basados en pirimidina como potentes agentes anticancerígenos: perspectivas SAR y perfil biológico
Por qué esto importa para la atención oncológica futura
Los fármacos de quimioterapia pueden salvar vidas, pero muchos dañan los tejidos sanos casi tanto como los tumores, provocando efectos secundarios severos y limitando la agresividad con la que los médicos pueden tratar el cáncer. Este estudio explora una nueva familia de moléculas sintéticas diseñadas para atacar con más fuerza a las células cancerosas que a las sanas, con el objetivo de tratamientos que sean potentes y a la vez más suaves para el organismo. Al combinar rasgos de dos «ladrillos» medicinales bien conocidos, los investigadores crearon y evaluaron compuestos que podrían servir como puntos de partida para fármacos anticancerígenos más seguros.
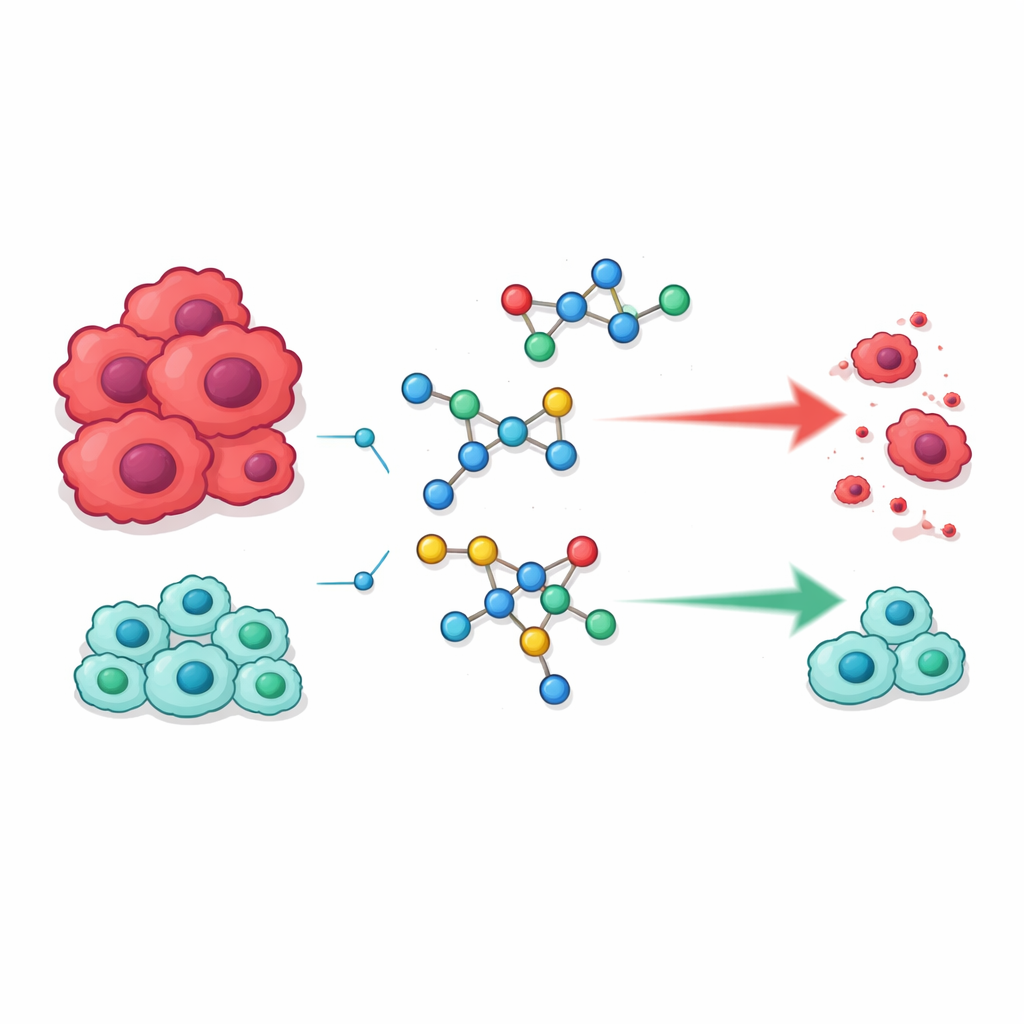
Construir nuevas moléculas a partir de piezas familiares
El equipo se centró en dos familias químicas que ya desempeñan papeles destacados en la medicina moderna. Una son las sulfonamidas, una clase temprana de fármacos originalmente famosa como antibióticos pero ahora presente en medicamentos para afecciones que van desde el glaucoma hasta la hipertensión y el cáncer. La otra son las pirimidinas, estructuras en forma de anillo que forman parte de nuestro ADN y se usan ampliamente en fármacos anticancerígenos porque pueden interferir con la copia del material genético celular. La idea de los investigadores fue fusionar estos dos motivos en moléculas híbridas únicas que pudieran reconocer y alterar mejor los procesos de los que dependen las células cancerosas para dividirse.
De la química de laboratorio a una biblioteca de candidatos
Mediante síntesis orgánica escalonada, los científicos construyeron un conjunto diverso de compuestos sulfonamídicos basados en pirimidina. Al enlazar el armazón central con distintos sistemas de anillos circundantes —como triazoles, pirazoles, tiazoles y triazinas— ajustaron propiedades como la carga electrónica, la forma y la liposolubilidad. Estas características influyen en cuánto puede una molécula atravesar las membranas celulares, alcanzar su blanco y evitar quedar atrapada o ser eliminada. Cada nueva estructura se verificó cuidadosamente con herramientas estándar de análisis químico, asegurando que los investigadores supieran exactamente lo que habían sintetizado antes de pasar a las pruebas biológicas.
Poner a prueba los nuevos compuestos
Las nuevas moléculas se evaluaron frente a dos líneas celulares humanas de cáncer —HepG2 (hígado) y MCF‑7 (mama)— así como frente a dos tipos de células normales, fibroblastos pulmonares WI‑38 y células renales VERO, para valorar tanto la potencia como la seguridad. Varios candidatos destacaron. Cuatro compuestos, etiquetados como 18, 21, 23 y 24, eliminaron células cancerosas a concentraciones similares o inferiores a las necesarias para el fármaco de uso extendido 5‑fluorouracilo. Sin embargo, a diferencia del 5‑fluorouracilo, estos mismos compuestos fueron notablemente menos dañinos para las células normales, lo que sugiere un equilibrio más favorable entre eficacia y toxicidad. Otros miembros de la serie que carecían de ciertas características beneficiosas mostraron una actividad mucho más débil, lo que subraya lo sensibles que son los efectos anticancerígenos a pequeños cambios estructurales.
Qué distingue a los candidatos más fuertes
Al comparar estructuras y resultados, los autores elaboraron reglas tempranas sobre qué funciona mejor. Los compuestos más activos tendían a portar grupos pequeños que donan densidad electrónica al armazón central, mejorando cómo interactúan las moléculas con sus blancos biológicos. También mostraban un nivel «justo» de lipofilicidad: lo suficiente para atravesar membranas celulares, pero no tan grasosos como para unirse de forma inespecífica a todo. Además, sus formas evitaban obstáculos voluminosos cerca de las regiones activas, permitiendo un ajuste ceñido en los sitios de unión. Estas características parecían potenciar tanto el poder citotóxico contra el cáncer como la preservación de las células normales, lo que sugiere que las moléculas podrían dirigirse con mayor selectividad a vías de las que dependen los tumores.
Una mirada más cercana a cómo podrían actuar
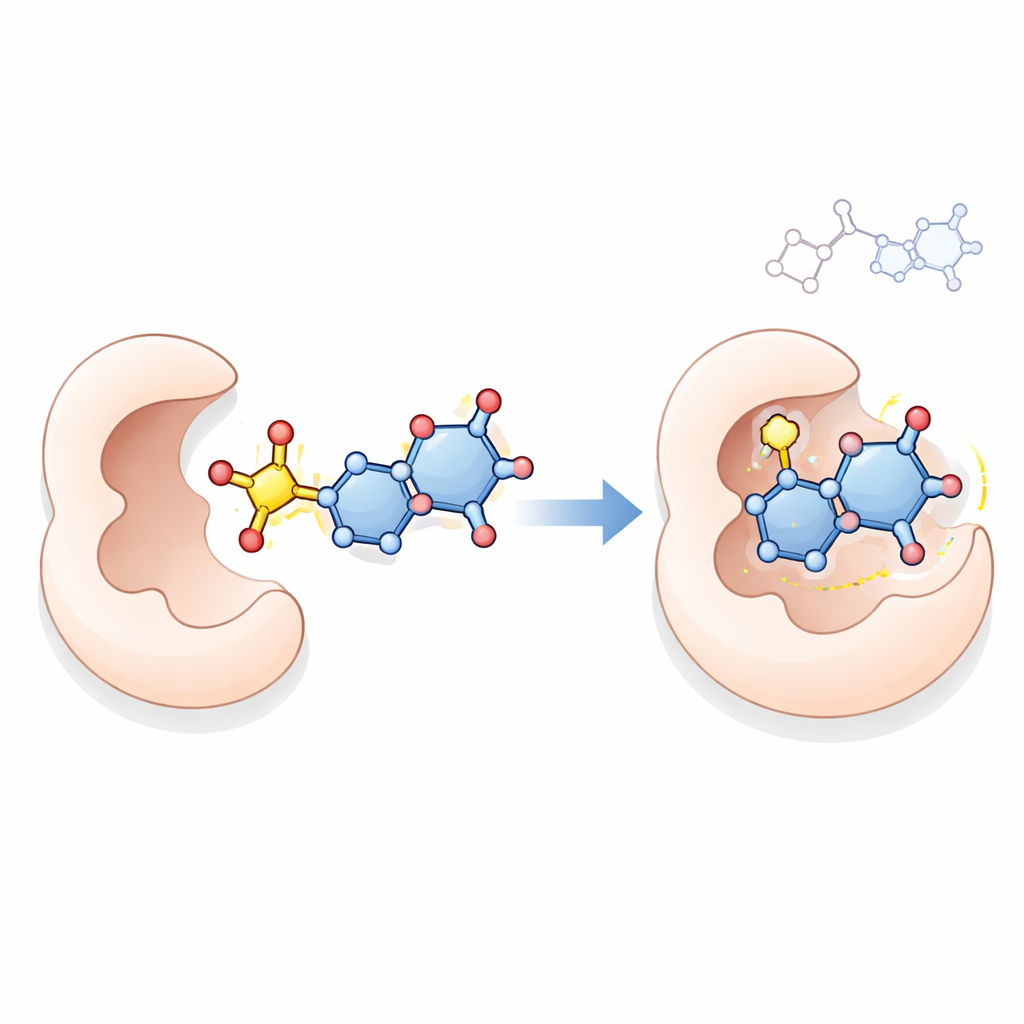
Para explorar un posible modo de acción, el equipo empleó acoplamiento molecular asistido por ordenador, una técnica que simula cómo una molécula pequeña puede acomodarse en el sitio activo de una proteína. Examinaron cómo los compuestos principales 18, 21, 23 y 24 interactúan con la timidilato sintasa, una enzima clave que las células cancerosas necesitan para sintetizar ADN y un blanco conocido de fármacos como el 5‑fluorouracilo. Las simulaciones sugirieron que estas nuevas moléculas, particularmente el compuesto 23, pueden formar múltiples contactos estabilizantes dentro del bolsillo de la enzima, en algunos casos uniéndose con mayor afinidad que el fármaco de referencia. Aunque el acoplamiento por sí solo no puede probar cómo actúan las moléculas dentro de células vivas, ofrece una explicación plausible y coherente con sus fuertes efectos antiproliferativos.
Qué significa esto de cara al futuro
En conjunto, este trabajo aporta cuatro moléculas líderes que combinan actividad potente contra células de cáncer de hígado y mama con efectos más moderados sobre células normales, junto con indicios tempranos sobre las características estructurales que impulsan este equilibrio. En términos cotidianos, los investigadores han esbozado un plano químico para candidatos a quimioterapia de próxima generación que podrían ser efectivos y más respetuosos con el tejido sano. Serán necesarios estudios adicionales en enzimas, células completas y, eventualmente, en animales, pero estos híbridos pirimidina‑sulfonamida representan un paso prometedor hacia tratamientos contra el cáncer más dirigidos y tolerables.
Cita: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Palabras clave: fármacos anticancerígenos, sulfonamidas, híbridos de pirimidina, timidilato sintasa, acoplamiento molecular