Clear Sky Science · de
Design, Synthese, molekulares Docking und zytotoxische Bewertung neuartiger pyrimidinbasierter Sulfonamid‑Derivate als potente Antikrebsmittel: SAR‑Erkenntnisse und biologische Profiling
Warum das für die künftige Krebsbehandlung wichtig ist
Chemotherapeutika können lebensrettend sein, schädigen aber häufig gesundes Gewebe fast genauso stark wie Tumoren, was zu starken Nebenwirkungen führt und die Möglichkeit einschränkt, wie aggressiv Ärzte behandeln können. Diese Studie untersucht eine neue Familie synthetischer Moleküle, die Krebszellen stärker treffen sollen als gesunde Zellen, mit dem Ziel, Therapien zu entwickeln, die sowohl wirkkräftig als auch schonender für den Körper sind. Indem die Forschenden Eigenschaften zweier etablierter medizinischer „Bausteine“ kombinierten, erzeugten und testeten sie Verbindungen, die als Ausgangspunkte für sicherere Antikrebsmittel dienen könnten.
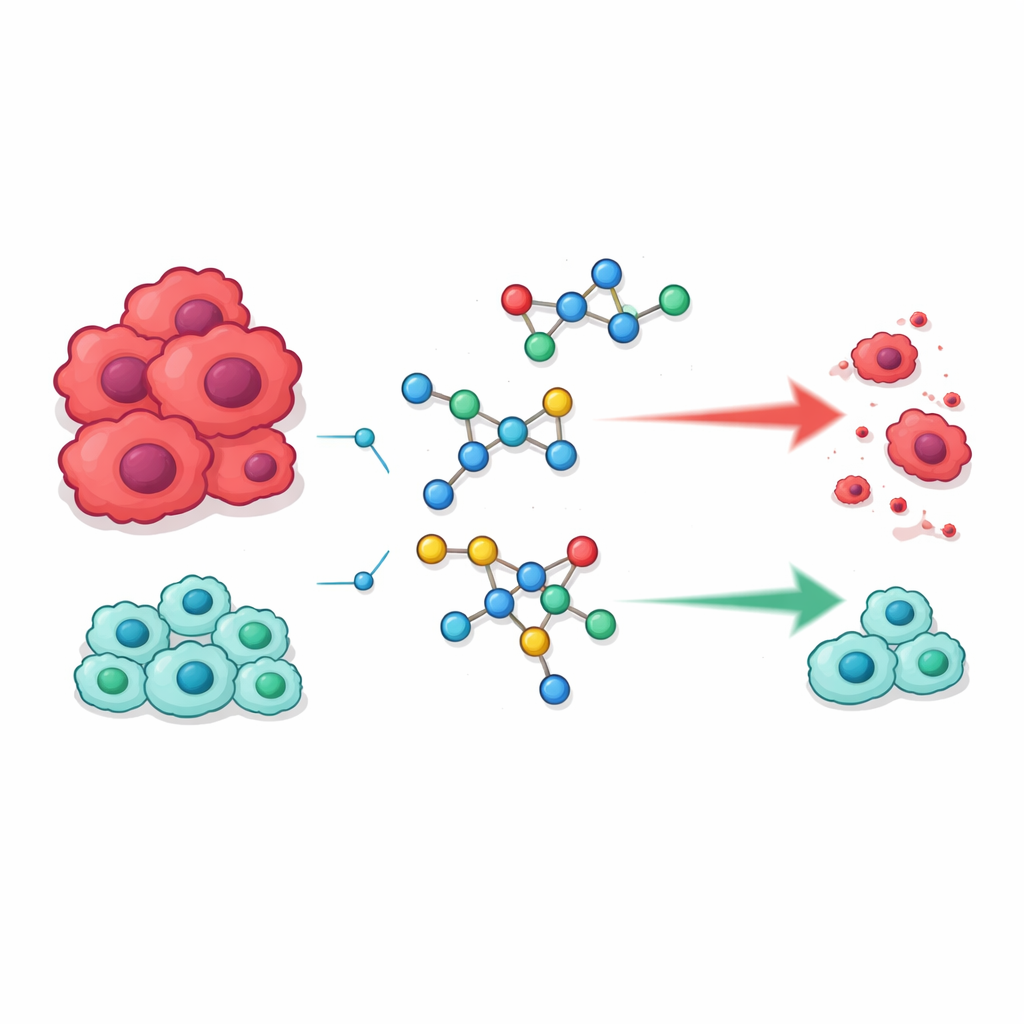
Neue Moleküle aus vertrauten Bausteinen
Das Team konzentrierte sich auf zwei chemische Familien, die bereits eine wichtige Rolle in der modernen Medizin spielen. Die eine sind Sulfonamide, eine frühe Wirkstoffklasse, die ursprünglich als Antibiotika bekannt wurde, heute aber in Arzneimitteln gegen Erkrankungen von Glaukom bis Bluthochdruck und Krebs vorkommt. Die andere sind Pyrimidine, ringförmige Strukturen, die Teil unserer DNA sind und häufig in Krebsmedikamenten eingesetzt werden, weil sie in die Vervielfältigung des genetischen Materials eingreifen können. Die Idee der Forschenden war, diese beiden Motive in einzelnen Hybridmolekülen zu verschmelzen, die Prozesse, von denen Krebszellen zur Teilung abhängen, besser erkennen und stören könnten.
Von der Laborchemie zu einer Bibliothek von Kandidaten
Durch stufenweise organische Synthese bauten die Wissenschaftlerinnen und Wissenschaftler eine vielfältige Reihe pyrimidinbasierter Sulfonamid‑Verbindungen auf. Indem sie das Kerngerüst mit verschiedenen umliegenden Ringsystemen wie Triazolen, Pyrazolen, Thiazolen und Triazinen verbanden, passten sie Eigenschaften wie Elektronenverteilung, Form und Lipophilie an. Diese Merkmale bestimmen, wie gut ein Molekül Zellmembranen passieren, sein Ziel erreichen und vermeiden kann, gebunden oder ausgeschieden zu werden. Jede neue Struktur wurde mit gängigen chemischen Analyseverfahren sorgfältig verifiziert, sodass die Forschenden genau wussten, was sie hergestellt hatten, bevor sie zu biologischen Tests übergingen.
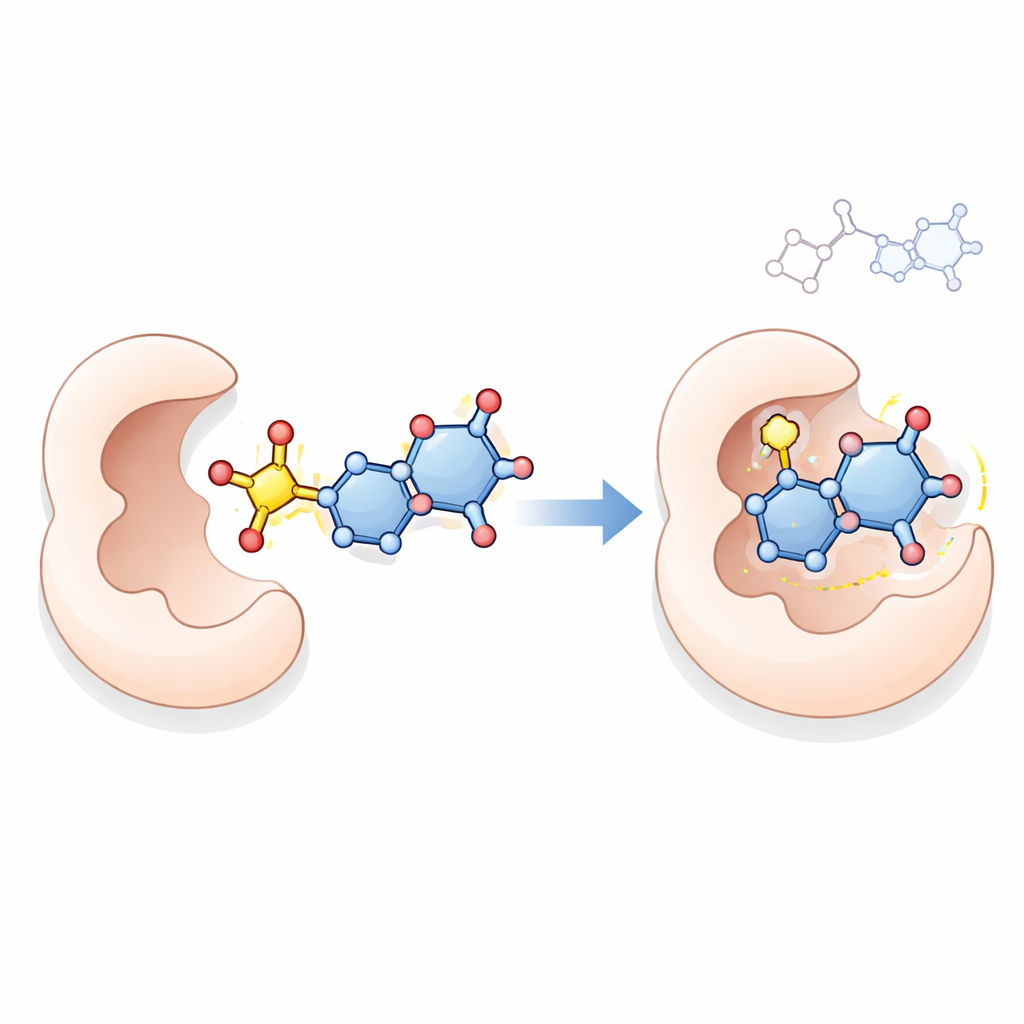
Die neuen Verbindungen auf dem Prüfstand
Die neuen Moleküle wurden gegen zwei menschliche Krebszelllinien—HepG2 (Leber) und MCF‑7 (Brust)—sowie gegen zwei Typen normaler Zellen, WI‑38 Lungenfibroblasten und VERO Nierenzellen, getestet, um sowohl Wirksamkeit als auch Sicherheit zu bewerten. Mehrere Kandidaten stachen hervor. Vier Verbindungen, bezeichnet als 18, 21, 23 und 24, töteten Krebszellen bei Konzentrationen, die denen des weit verbreiteten Medikaments 5‑Fluorouracil ähnlich waren oder unterschritten. Im Gegensatz zu 5‑Fluorouracil waren diese Verbindungen jedoch deutlich weniger schädlich für normale Zellen, was auf ein günstigeres Verhältnis von Wirksamkeit zu Toxizität hindeutet. Andere Mitglieder der Serie, denen bestimmte vorteilhafte Merkmale fehlten, zeigten deutlich schwächere Aktivität, was unterstreicht, wie empfindlich antitumorale Effekte auf kleine strukturelle Änderungen reagieren.
Was die stärksten Kandidaten unterscheidet
Durch den Vergleich von Strukturen und Testergebnissen leiteten die Autorinnen und Autoren erste Regeln ab, was am besten funktioniert. Die aktivsten Verbindungen trugen tendenziell kleine Gruppen, die Elektronendichte an das Kerngerüst abgeben und damit die Wechselwirkung der Moleküle mit ihren biologischen Zielen verbessern. Sie zeigten außerdem ein „gerade richtiges“ Maß an Lipophilie—hinreichend fettliebend, um Zellmembranen zu durchdringen, aber nicht so fettig, dass sie unspezifisch an alles haften. Darüber hinaus vermieden ihre Formen sperrige Hindernisse in der Nähe aktiver Regionen, sodass sie gut in Bindungstaschen passen konnten. Diese Eigenschaften schienen sowohl die Krebszell‑tötende Wirkung als auch das Schonendsein für normale Zellen zu erhöhen und deuten darauf hin, dass die Moleküle selektiver auf Wege abzielen könnten, von denen Tumoren abhängen.
Ein genauerer Blick auf die mögliche Wirkweise
Um einen möglichen Wirkmechanismus zu untersuchen, verwendete das Team computergestütztes molekulares Docking, eine Technik, die simuliert, wie ein kleines Molekül in der aktiven Stelle eines Proteins sitzen könnte. Sie untersuchten, wie die Top‑Verbindungen 18, 21, 23 und 24 mit der Thymidylatsynthase interagieren—einem Schlüsselenzym, das Krebszellen zur DNA‑Synthese benötigen, und einem bekannten Ziel von Wirkstoffen wie 5‑Fluorouracil. Die Simulationen legten nahe, dass diese neuen Moleküle, insbesondere Verbindung 23, mehrere stabilisierende Kontakte innerhalb der Enzymtasche ausbilden können und in einigen Fällen stärker binden als das Referenzmedikament. Während Docking allein nicht beweisen kann, wie die Verbindungen in lebenden Zellen wirken, liefert es eine plausiblen Erklärung, die mit ihren starken antiproliferativen Effekten vereinbar ist.
Was das für die Zukunft bedeutet
Insgesamt liefert diese Arbeit vier Leitsubstanzen, die potente Aktivität gegen Leber‑ und Brustkrebszellen mit milderen Effekten auf normale Zellen kombinieren, sowie erste Hinweise auf strukturelle Merkmale, die dieses Gleichgewicht antreiben. Alltagssprachlich haben die Forschenden einen chemischen Bauplan für nächste Generationen von Chemotherapie‑Kandidaten skizziert, die sowohl wirksam als auch schonender für gesundes Gewebe sein könnten. Weitere Studien an Enzymen, ganzen Zellen und schließlich im Tiermodell werden erforderlich sein, aber diese Pyrimidin‑Sulfonamid‑Hybride stellen einen vielversprechenden Schritt in Richtung gezielterer und besser verträglicherer Krebsbehandlungen dar.
Zitation: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Schlüsselwörter: Antikrebsmittel, Sulfonamide, Pyrimidin‑Hybride, Thymidylatsynthase, molekulares Docking