Clear Sky Science · ru
Проектирование, синтез, молекулярный докинг и оценка цитотоксичности новых сульфонамидных производных на основе пиримидина как мощных противораковых агентов: выводы SAR и биологический профиль
Почему это важно для будущей онкологической помощи
Химиотерапевтические препараты могут спасать жизни, но многие из них повреждают здоровые ткани почти так же сильно, как и опухоли, что приводит к тяжелым побочным эффектам и ограничивает агрессивность лечения. В этом исследовании изучается новый класс синтетических молекул, нацеленных на то, чтобы поражать раковые клетки сильнее, чем здоровые, с целью создания лечебных средств, одновременно мощных и более щадящих для организма. Сочетая элементы двух хорошо известных «кирпичиков» медицины, исследователи синтезировали и протестировали соединения, которые могут послужить отправной точкой для создания более безопасных противораковых препаратов.
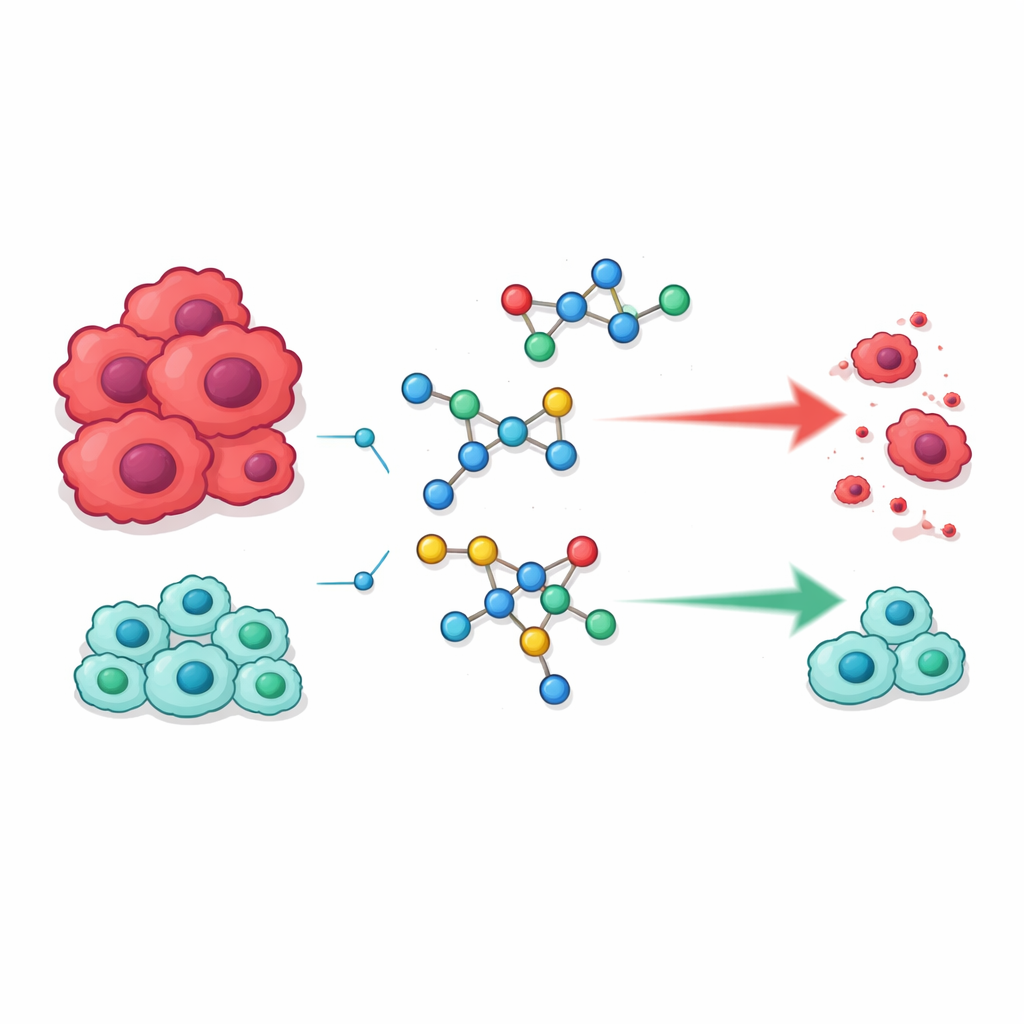
Создание новых молекул из знакомых фрагментов
Команда сосредоточилась на двух химических семействах, уже играющих ключевые роли в современной медицине. Первые — сульфонамиды, ранний класс препаратов, прославившийся как антибиотики, но ныне встречающийся в лекарствах от глаукомы, гипертонии и рака. Вторые — пиримидины, кольцевые структуры, входящие в состав ДНК и широко используемые в противораковых средствах, поскольку могут мешать копированию генетического материала клетки. Идея исследователей состояла в объединении этих двух мотивов в гибридные молекулы, которые могли бы лучше распознавать и нарушать процессы, необходимые раковым клеткам для деления.
От лабораторной химии к библиотеке кандидатов
С помощью поэтапного органического синтеза ученые создали разнообразную коллекцию сульфонамидных соединений на основе пиримидина. Связывая основную структуру с различными окружающими кольцевыми системами — такими как триазолы, пиразолы, тиазолы и триазины — они настраивали такие свойства, как электронная плотность, форма и липофильность. Эти характеристики определяют, насколько хорошо молекула проходит через клеточные мембраны, достигает своей мишени и не задерживается или не вымывается. Каждая новая структура была тщательно верифицирована стандартными аналитическими методами, что гарантировало знание точного состава соединений перед переходом к биологическим испытаниям.
Испытание новых соединений
Новосинтезированные молекулы были протестированы на двух линиях раковых человеческих клеток — HepG2 (печень) и MCF‑7 (молочная железа), а также на двух типах нормальных клеток, фибробластах легких WI‑38 и почечных клетках VERO, чтобы оценить как активность, так и безопасность. Несколько кандидатов выделились. Четыре соединения, обозначенные как 18, 21, 23 и 24, убивали раковые клетки при концентрациях, сопоставимых или ниже, чем у широко применяемого препарата 5‑фторурацил. При этом, в отличие от 5‑фторурацила, эти соединения заметно меньше повреждали нормальные клетки, что указывает на более благоприятное соотношение эффективности и токсичности. Другие представители серии, лишенные некоторых полезных признаков, проявляли значительно более слабую активность, что подчеркивает высокую чувствительность противоопухолевого эффекта к небольшим структурным изменениям.
Чем отличаются самые сильные кандидаты
Сопоставляя структуры и результаты тестов, авторы вывели ранние правила того, что работает лучше всего. Наиболее активные соединения, как правило, несли небольшие донорные заместители, повышающие электронную плотность основного скелета и улучшающие взаимодействие молекул с биологическими мишенями. Они также демонстрировали «вмеру» выраженную липофильность — достаточно сродную с жирами, чтобы пройти через мембраны, но не настолько жирную, чтобы нелинейно связываться со всеми компонентами. Кроме того, их форма избегала громоздких препятствий около активных участков, обеспечивая плотное вхождение в сайты связывания. Эти характеристики, по-видимому, повышали как противоопухолевую активность, так и селективность по отношению к нормальным клеткам, что наталкивает на мысль о более прицельном воздействии на пути, от которых зависят опухоли.
Более детально о возможном механизме действия
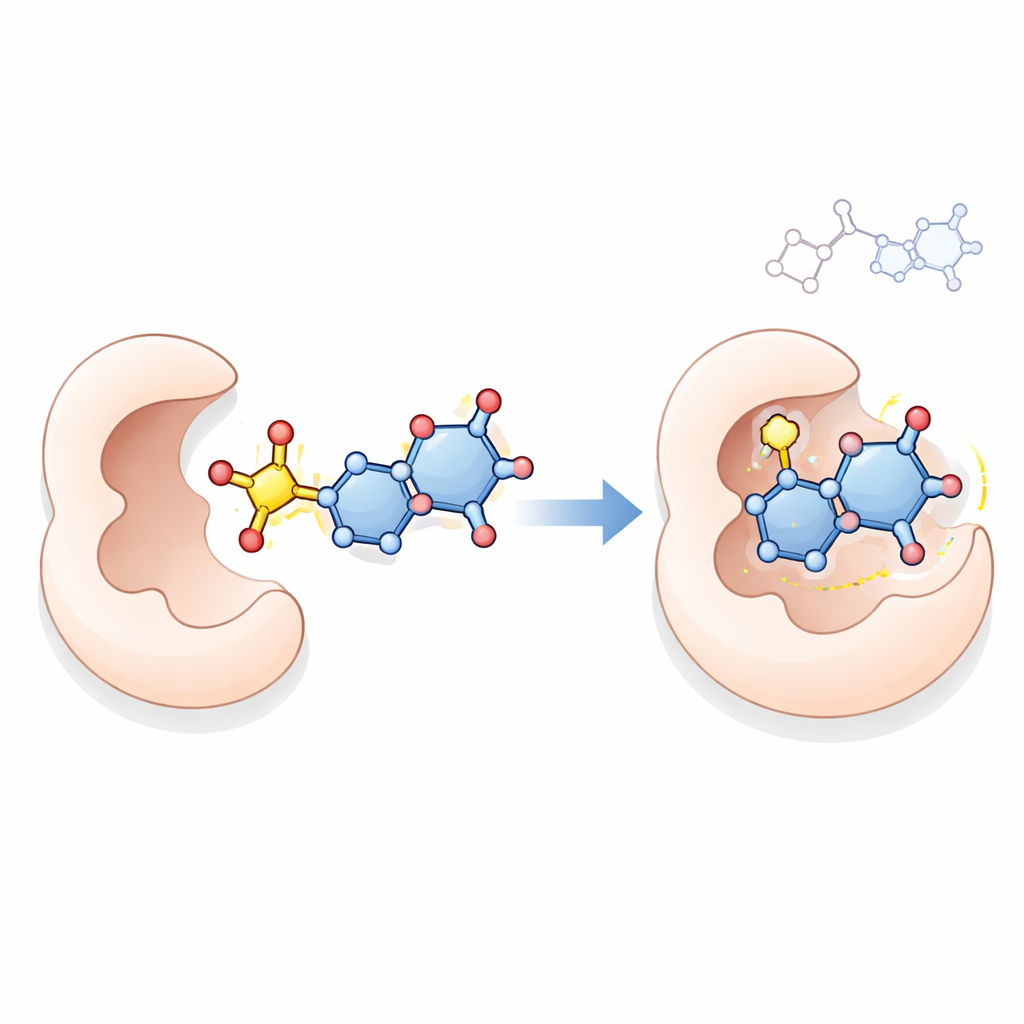
Чтобы изучить возможный механизм, команда использовала компьютерный молекулярный докинг — метод, моделирующий, как малая молекула может располагаться в активном кармане белка. Они исследовали взаимодействия ведущих соединений 18, 21, 23 и 24 с тимидилатсинтазой, ключевым ферментом, необходимым раковым клеткам для синтеза ДНК и известной мишенью таких препаратов, как 5‑фторурацил. Симуляции показали, что эти новые молекулы, особенно соединение 23, могут образовывать несколько стабилизирующих контактов в кармане фермента, в некоторых случаях связываясь сильнее, чем эталонный препарат. Хотя докинг сам по себе не доказывает механизм действия в живой клетке, он предлагает правдоподобное объяснение, согласующееся с их сильными антипроліферативными эффектами.
Что это означает для будущих исследований
В целом эта работа предоставляет четыре лидирующие молекулы, сочетающие мощную активность против печеночных и молочных раковых клеток с более мягким воздействием на нормальные клетки, а также ранние подсказки о структурных особенностях, определяющих этот баланс. Проще говоря, исследователи наметили химический чертеж для кандидатов следующего поколения химиотерапии, которые могут быть одновременно эффективными и более щадящими для здоровых тканей. Потребуются дальнейшие исследования на уровне ферментов, целых клеток и, в конечном счете, животных моделей, но эти пиримидин‑сульфонамидные гибриды представляют собой многообещающий шаг к более прицельным и переносимым методам лечения рака.
Цитирование: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Ключевые слова: препараты против рака, сульфонамиды, пиримидиновые гибриды, тимидилатсинтаза, молекулярный докинг