Clear Sky Science · sv
Design, syntes, molekylär dockning och cytotoxisk utvärdering av nya pyrimidinbaserade sulfonamidderivat som potenta anticancer‑ämnen: SAR‑insikter och biologisk profilering
Varför detta spelar roll för framtidens cancerbehandling
Kemoterapi kan rädda liv, men många läkemedel skadar friska vävnader nästan lika mycket som tumörer, vilket leder till hårda biverkningar och begränsar hur aggressivt läkare kan behandla cancer. Denna studie undersöker en ny familj av laboratorietillverkade molekyler utformade för att slå hårdare mot cancerceller än friska celler, med målet att ta fram behandlingar som både är kraftfulla och skonsammare för kroppen. Genom att kombinera kännetecken från två välkända medicinska ”byggstenar” skapade och testade forskarna föreningar som kan fungera som startpunkter för säkrare anticancerläkemedel.
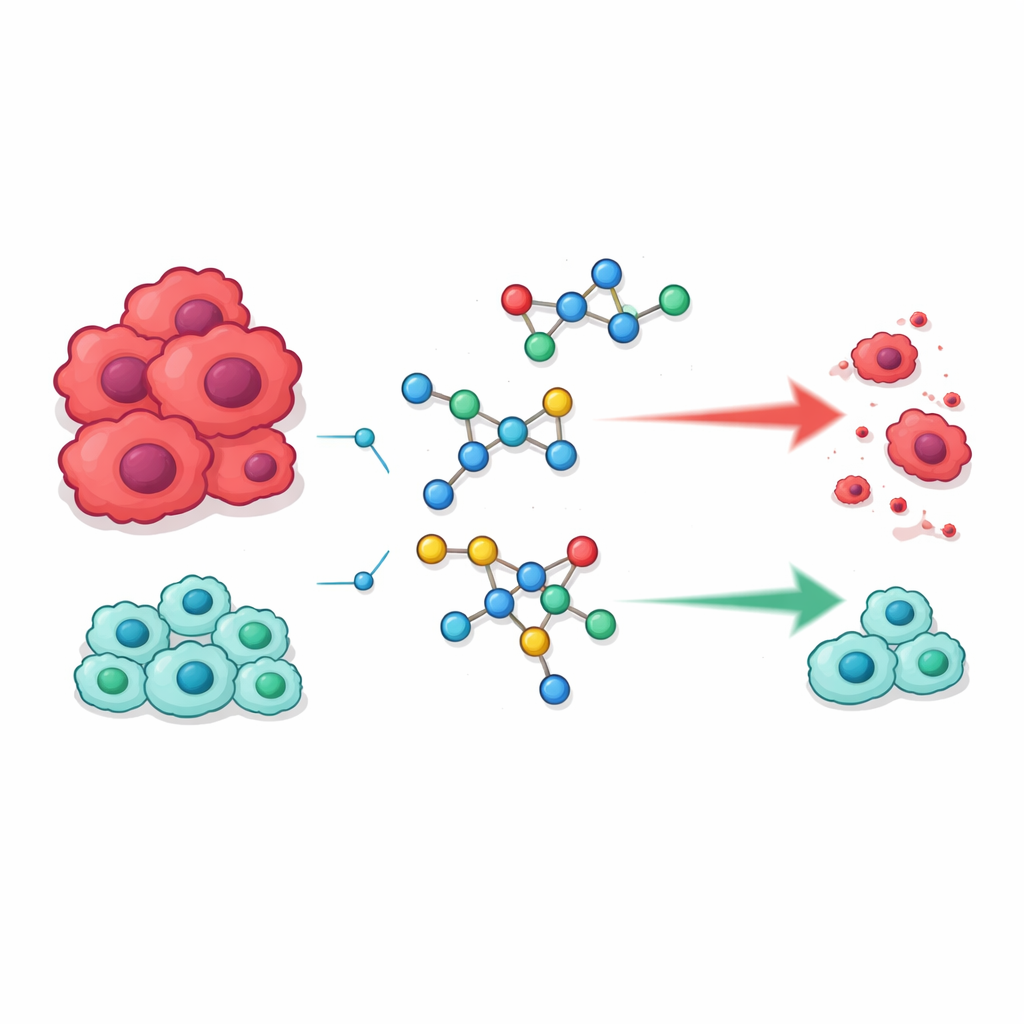
Bygga nya molekyler av bekanta delar
Gruppen fokuserade på två kemiska familjer som redan spelar framträdande roller i modern medicin. Den ena är sulfonamider, en tidig läkemedelsklass som ursprungligen blev känd som antibiotika men som nu återfinns i läkemedel mot allt från glaukom till högt blodtryck och cancer. Den andra är pyrimidiner, ringstrukturer som ingår i vårt DNA och som ofta används i anticancerläkemedel eftersom de kan störa hur celler kopierar sitt genetiska material. Forskarna ville förena dessa två motiv i enskilda hybridmolekyler som bättre kan känna igen och störa processer som cancerceller förlitar sig på för att dela sig.
Från bänk‑kemi till ett bibliotek av kandidater
Genom stegvis organisk syntes byggde forskarna upp en mångfaldig uppsättning pyrimidinbaserade sulfonamidföreningar. Genom att koppla huvudskalet till olika omgivande ringsystem—såsom triazoler, pyrazoler, thiazoler och triaziner—justerade de egenskaper som elektronisk laddning, form och fettlöslighet. Dessa egenskaper avgör hur väl en molekyl kan passera cellmembran, nå sitt mål och undvika att fastna eller spolas ut. Varje ny struktur verifierades noggrant med standardverktyg för kemisk analys, vilket säkerställde att forskarna visste exakt vad de hade framställt innan de gick vidare till biologiska tester.
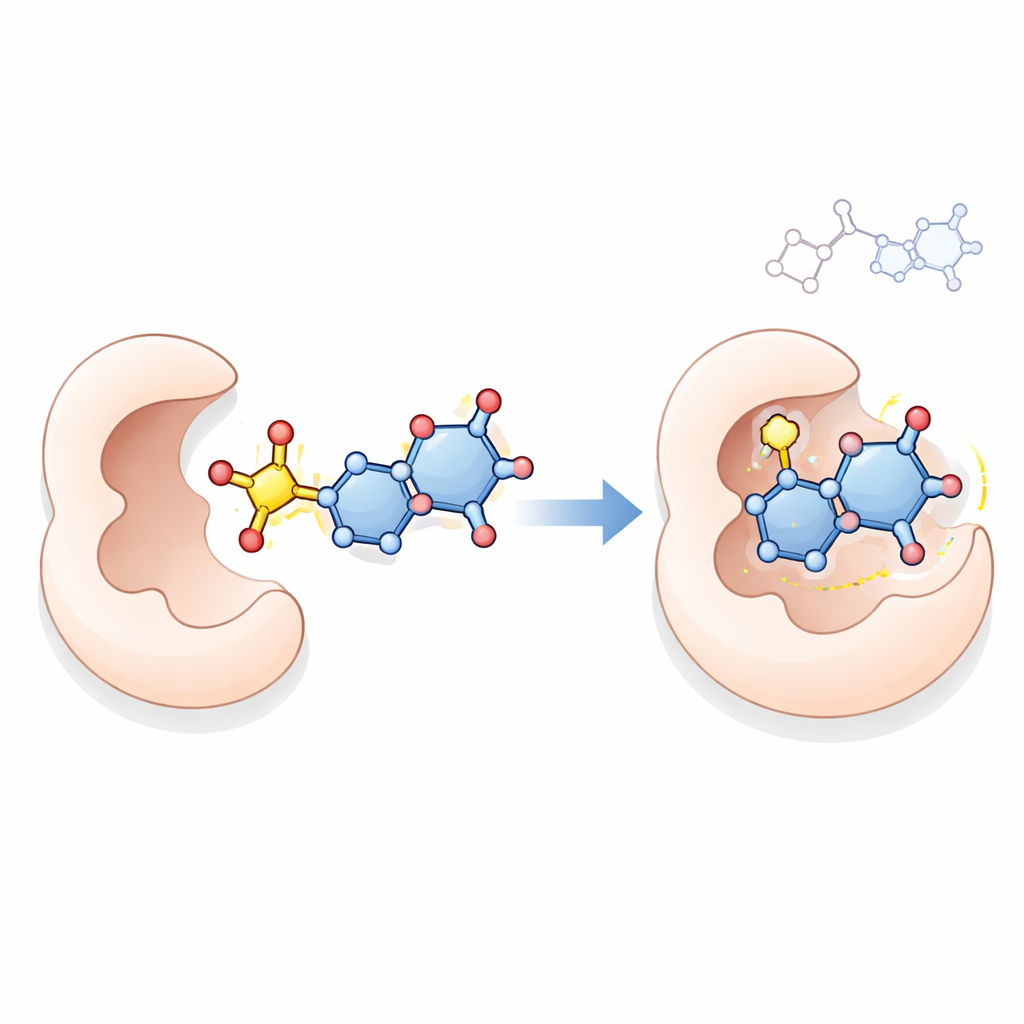
Att pröva de nya föreningarna
De nya molekylerna skärmdes mot två humana cancercellinjer—HepG2 (lever) och MCF‑7 (bröst)—samt två typer av normala celler, WI‑38 lungfibroblaster och VERO njurceller, för att bedöma både potens och säkerhet. Flera kandidater utmärkte sig. Fyra föreningar, märkta 18, 21, 23 och 24, dödade cancerceller vid koncentrationer som var likvärdiga med eller lägre än de som krävdes för det välanvända läkemedlet 5‑fluorouracil. Till skillnad från 5‑fluorouracil var dessa föreningar dock märkbart mindre skadliga för normala celler, vilket tyder på en mer fördelaktig balans mellan effekt och toxicitet. Andra medlemmar i serien som saknade vissa gynnsamma egenskaper visade mycket svagare aktivitet, vilket understryker hur känsliga anticancer‑effekter är för små strukturella förändringar.
Vad som skiljer de starkaste kandidaterna
Genom att jämföra strukturer och testresultat sammanställde författarna tidiga regler för vad som fungerar bäst. De mest aktiva föreningarna tenderade att bära små grupper som donerar elektrontäthet till huvudskalet, vilket förbättrar hur molekylerna interagerar med sina biologiska mål. De uppvisade också en ”lagom” nivå av lipofilicitet—tillräckligt benägna att föredra fett för att glida genom cellmembran, men inte så feta att de ospecifikt fastnar i allt. Dessutom undvek deras former skrymmande hinder nära aktiva regioner, vilket tillät en tät passform i bindningsfickorna. Dessa egenskaper verkade öka både cancercellsdödande effekt och sparsamhet mot normala celler, vilket antyder att molekylerna kan rikta in sig mer selektivt på de vägar tumörer är beroende av.
En närmare titt på hur de kan fungera
För att utforska en möjlig verkningsmekanism använde teamet datorbaserad molekylär dockning, en teknik som simulerar hur en liten molekyl kan sitta inne i en proteins aktiva site. De undersökte hur toppföreningarna 18, 21, 23 och 24 interagerar med tymidylatsyntas, ett nyckelenzym som cancerceller behöver för att tillverka DNA och ett känt mål för läkemedel som 5‑fluorouracil. Simulationerna antydde att dessa nya molekyler, särskilt förening 23, kan bilda flera stabiliserande kontakter inom enzymets ficka och i vissa fall binda starkare än referensläkemedlet. Dockning ensam kan inte bevisa hur föreningarna fungerar inne i levande celler, men det erbjuder en rimlig förklaring som stämmer överens med deras starka antiproliferativa effekter.
Vad detta innebär framöver
Sammanfattningsvis levererar detta arbete fyra ledande molekyler som kombinerar potent aktivitet mot lever‑ och bröstcancerceller med mildare effekter på normala celler, tillsammans med tidiga ledtrådar om de strukturella egenskaper som styr denna balans. I praktiska termer har forskarna skissat en kemisk ritning för nästa generationens kemoterapikandidater som kan vara både effektiva och snällare mot frisk vävnad. Ytterligare studier på enzymer, hela celler och så småningom djur kommer att behövas, men dessa pyrimidin‑sulfonamid‑hybrider utgör ett lovande steg mot mer riktade och tolererbara cancerbehandlingar.
Citering: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Nyckelord: anticancerläkemedel, sulfonamider, pyrimidinhybrider, tymidylatsyntas, molekylär dockning