Clear Sky Science · nl
Ontwerp, synthese, moleculair docken en cytotoxische evaluatie van nieuwe pyrimidine-gebaseerde sulfonamide-afgeleiden als krachtige anti-kanker middelen: SAR-inzichten en biologische profilering
Waarom dit belangrijk is voor toekomstige kankerzorg
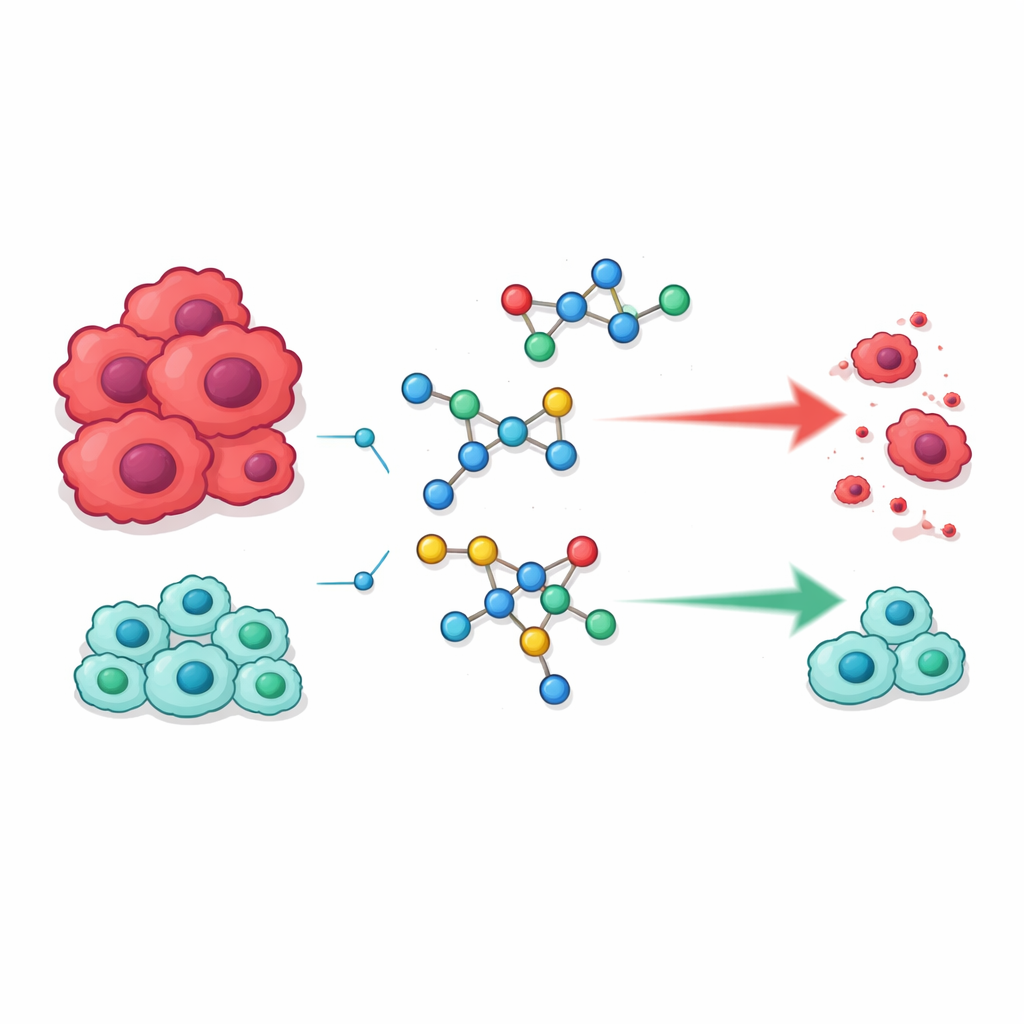
Chemotherapie kan levensreddend zijn, maar veel middelen beschadigen gezonde weefsels bijna net zo sterk als tumoren, wat leidt tot zware bijwerkingen en de mate waarin artsen agressief kunnen behandelen beperkt. Deze studie onderzoekt een nieuwe familie laboratoriumgemaakte moleculen die bedoeld zijn om kankercellen harder te raken dan gezonde cellen, met als doel behandelingen die zowel krachtig als milder voor het lichaam zijn. Door kenmerken van twee bekende medicinale “bouwstenen” te combineren, creëerden en testten de onderzoekers verbindingen die als uitgangspunten voor veiligere anti-kankergeneesmiddelen kunnen dienen.
Nieuwe moleculen bouwen uit vertrouwde onderdelen
Het team concentreerde zich op twee chemische families die al een prominente rol spelen in de moderne geneeskunde. De ene zijn sulfonamiden, een vroege klasse geneesmiddelen die aanvankelijk bekend werd als antibioticum maar nu voorkomt in medicijnen tegen aandoeningen variërend van glaucoom tot hoge bloeddruk en kanker. De andere zijn pyrimidines, ringvormige structuren die deel uitmaken van ons DNA en veel worden gebruikt in anti-kankermiddelen omdat ze kunnen interfereren met hoe cellen hun genetisch materiaal kopiëren. Het idee van de onderzoekers was deze twee motieven te versmelten tot hybride moleculen die processen waar kankercellen van afhankelijk zijn beter zouden kunnen herkennen en verstoren.
Van laboratoriumchemie naar een bibliotheek kandidaten
Middels stapsgewijze organische synthese bouwden de wetenschappers een diverse set pyrimidine-gebaseerde sulfonamideverbindingen. Door het kernskelet te koppelen aan verschillende omringende ringsystemen — zoals triazolen, pyrazolen, thiazolen en triazines — stemden ze eigenschappen af als elektrische lading, vorm en lipofiliteit. Deze kenmerken bepalen hoe goed een molecuul celmembranen kan passeren, zijn doel kan bereiken en voorkomt dat het vastloopt of wordt uitgespoeld. Elke nieuwe structuur werd zorgvuldig geverifieerd met standaardinstrumenten voor chemische analyse, zodat de onderzoekers precies wisten wat ze hadden gemaakt voordat ze verdergingen naar biologische tests.
De nieuwe verbindingen op de proef gesteld
De nieuwe moleculen werden gescreend tegen twee humane kankercellijnen — HepG2 (lever) en MCF-7 (borst) — evenals twee typen normale cellen, WI-38 longfibroblasten en VERO niercellen, om zowel werkzaamheid als veiligheid te evalueren. Verschillende kandidaten vielen op. Vier verbindingen, gelabeld 18, 21, 23 en 24, doodden kankercellen bij concentraties die vergelijkbaar waren met of lager dan die nodig voor het veelgebruikte middel 5-fluorouracil. Toch waren dezezelfde verbindingen, in tegenstelling tot 5-fluorouracil, duidelijk minder schadelijk voor normale cellen, wat wijst op een gunstigere balans tussen werkzaamheid en toxiciteit. Andere leden van de reeks die bepaalde gunstige kenmerken misten, toonden veel zwakkere activiteit, wat benadrukt hoe gevoelig anti-kankerwerking is voor kleine structurele veranderingen.
Wat de sterkste kandidaten anders maakt
Door structuren en testresultaten te vergelijken, stelden de auteurs vroege regels op over wat het beste werkt. De meest actieve verbindingen droegen vaak kleine groepen die elektrondichtheid naar het kernskelet doneren, wat de interactie van de moleculen met hun biologische doelwitten verbetert. Ze vertoonden ook een “precies goed” niveau van lipofiliteit — voldoende vetminnend om door celmembranen te glippen, maar niet zo vet dat ze zich niet-specifiek overal aan hechten. Daarnaast vermeden hun vormen volumineuze obstakels nabij de actieve regio’s, waardoor ze goed in bindingsplaatsen passen. Deze eigenschappen leken zowel het kankerceldodend vermogen als het sparen van normale cellen te versterken, wat erop wijst dat de moleculen mogelijk selectiever de routes herkennen waarop tumoren vertrouwen.
Een nadere blik op hoe ze zouden kunnen werken
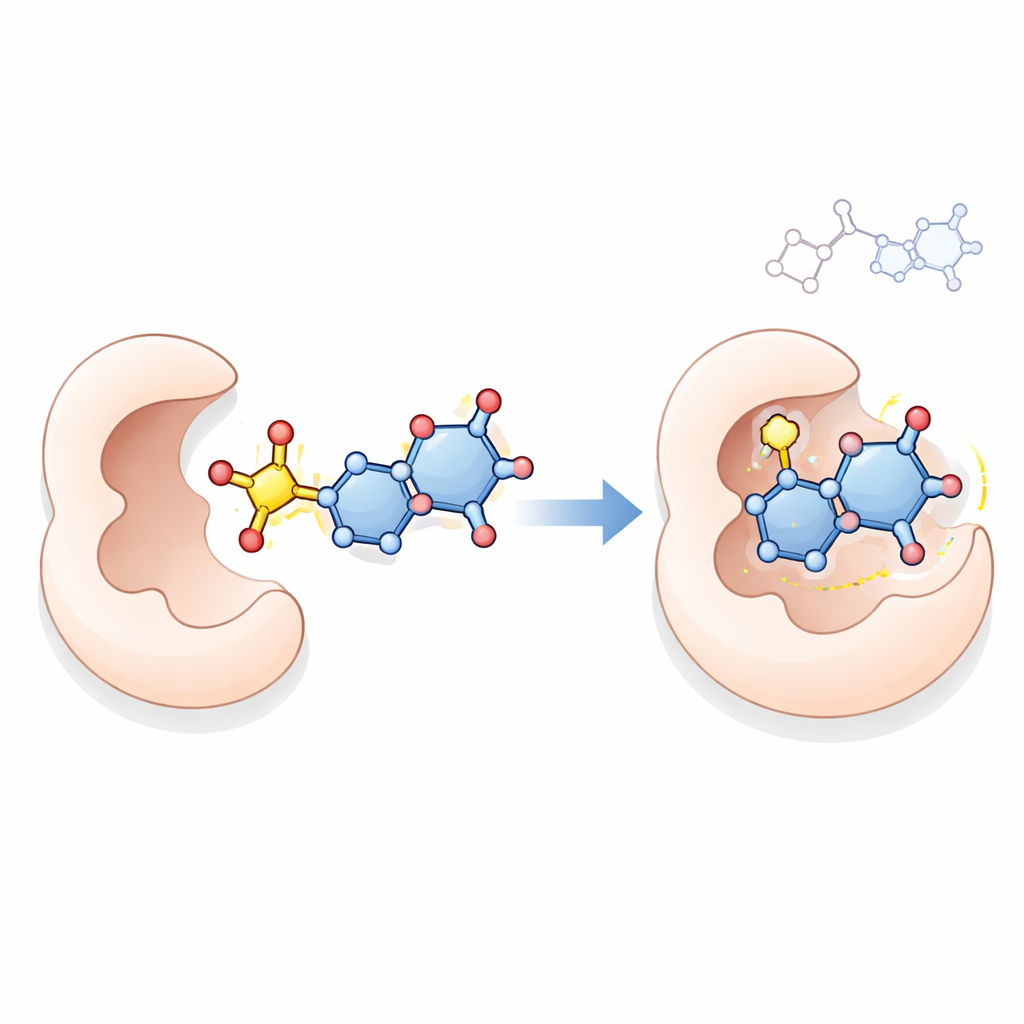
Om een mogelijke werkingsmechaniek te verkennen, gebruikte het team computergebaseerd moleculair docken, een techniek die simuleert hoe een klein molecuul in de actieve plaats van een eiwit kan passen. Ze onderzochten hoe topverbindingen 18, 21, 23 en 24 interacteren met thymidylaatsynthase, een sleutelenzym dat kankercellen nodig hebben om DNA te maken en een bekend doelwit van middelen zoals 5-fluorouracil. De simulaties suggereerden dat deze nieuwe moleculen, met name verbinding 23, meerdere stabiliserende contacten binnen het enzymvak kunnen vormen, in sommige gevallen sterker bindend dan het referentiemiddel. Hoewel docken op zichzelf niet kan bewijzen hoe de verbindingen in levende cellen werken, biedt het een plausibele verklaring die consistent is met hun sterke antiproliferatieve effecten.
Wat dit betekent voor de toekomst
In het algemeen levert dit werk vier leidende moleculen op die krachtige activiteit tegen lever- en borstkankercellen combineren met mildere effecten op normale cellen, samen met vroege aanwijzingen over de structurele kenmerken die deze balans aansturen. In gewone taal hebben de onderzoekers een chemisch blauwdruk geschetst voor de volgende generatie chemotherapiemiddelen die effectief kunnen zijn en vriendelijker voor gezond weefsel. Verdere studies op enzymniveau, in volledige cellen en uiteindelijk in dieren zijn nodig, maar deze pyrimidine-sulfonamidehybriden vormen een veelbelovende stap richting meer gerichte en beter verdragen kankerbehandelingen.
Bronvermelding: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Trefwoorden: anti-kankergeneesmiddelen, sulfonamiden, pyrimidine-hybriden, thymidylaatsynthase, moleculair docken