Clear Sky Science · it
Progettazione, sintesi, docking molecolare e valutazione citotossica di nuovi derivati sulfonammidici a base di pirimidina come potenti agenti antitumorali: approfondimenti SAR e profilazione biologica
Perché questo è importante per la cura del cancro in futuro
I farmaci chemioterapici possono salvare vite, ma molti danneggiano i tessuti sani quasi quanto i tumori, causando effetti collaterali gravi e limitando l’aggressività con cui i medici possono trattare il cancro. Questo studio esplora una nuova famiglia di molecole sintetiche progettate per colpire le cellule tumorali più duramente rispetto a quelle sane, con l’obiettivo di terapie potenti ma più delicate per l’organismo. Combinando caratteristiche di due «mattoni» medicinali ben noti, i ricercatori hanno creato e testato composti che potrebbero fungere da punti di partenza per farmaci antitumorali più sicuri.
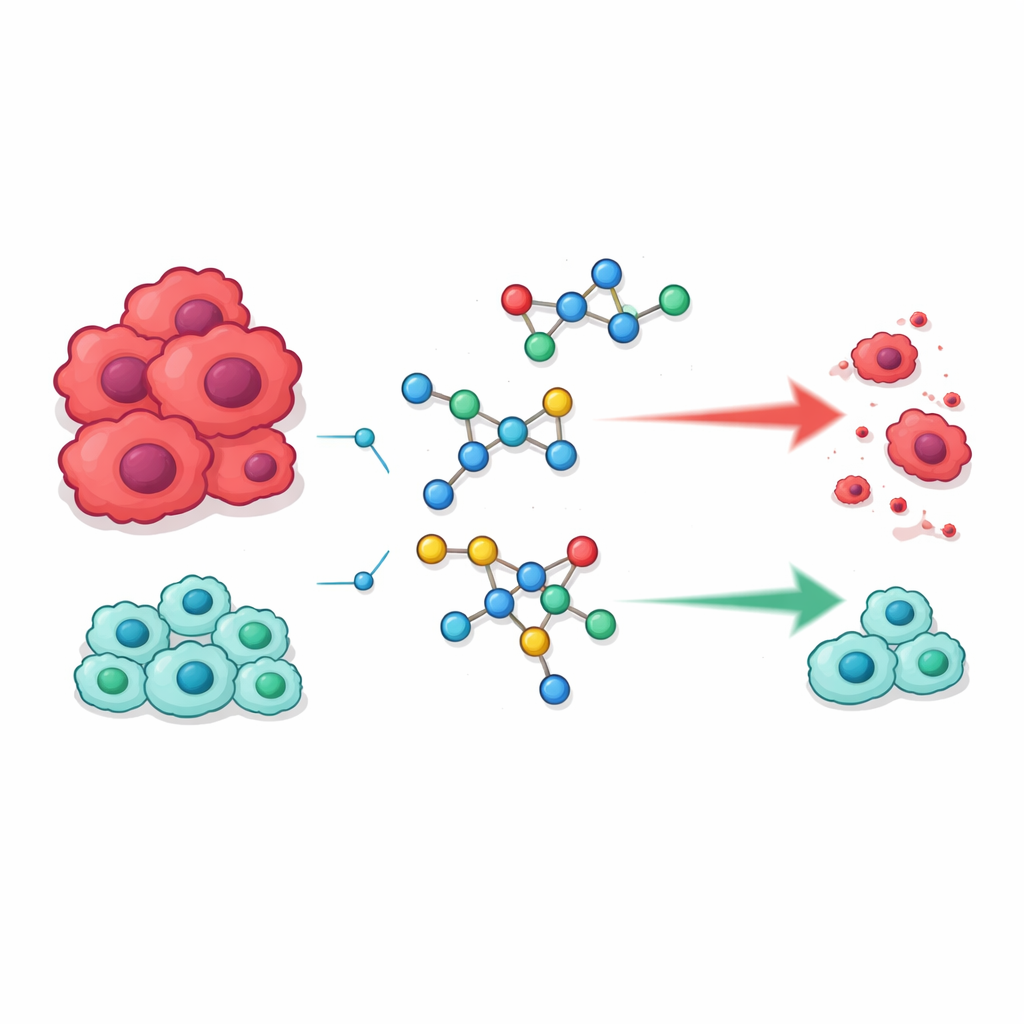
Costruire nuove molecole partendo da elementi familiari
Il gruppo si è concentrato su due famiglie chimiche che già svolgono ruoli di primo piano nella medicina moderna. Una sono le sulfonammidi, una classe di farmaci storicamente nota come antibiotico ma oggi presente in terapie per condizioni che vanno dal glaucoma all’ipertensione e al cancro. L’altra sono le pirimidine, strutture ad anello che fanno parte del DNA e sono ampiamente impiegate nei farmaci antitumorali perché possono interferire con la replicazione del materiale genetico. L’idea dei ricercatori è stata fondere questi due motivi in ibridi singoli che potrebbero riconoscere e interrompere meglio i processi di cui le cellule tumorali dipendono per dividersi.
Dalla chimica di laboratorio a una libreria di candidati
Attraverso una sintesi organica stepwise, gli scienziati hanno costruito un insieme diversificato di composti sulfonamidici basati su pirimidina. Collegando il nucleo a diversi sistemi ad anello circostanti—come triazoli, pirazoli, tiazoli e triazine—hanno modulato proprietà quali carica elettronica, forma e lipofilia. Queste caratteristiche determinano quanto bene una molecola può attraversare le membrane cellulari, raggiungere il bersaglio ed evitare di rimanere intrappolata o eliminata. Ogni nuova struttura è stata accuratamente verificata con strumenti standard di analisi chimica, assicurando che i ricercatori sapessero esattamente cosa avevano sintetizzato prima di passare ai test biologici.
Mettere alla prova i nuovi composti
Le nuove molecole sono state testate su due linee cellulari tumorali umane—HepG2 (fegato) e MCF‑7 (seno)—e su due tipi di cellule normali, fibroblasti polmonari WI‑38 e cellule renali VERO, per valutare potenza e sicurezza. Diversi candidati si sono distinti. Quattro composti, etichettati 18, 21, 23 e 24, hanno ucciso le cellule tumorali a concentrazioni simili o inferiori rispetto al farmaco ampiamente usato 5‑fluorouracile. Tuttavia, a differenza del 5‑fluorouracile, questi composti erano notevolmente meno dannosi per le cellule normali, suggerendo un rapporto più favorevole tra efficacia e tossicità. Altri membri della serie privi di alcune caratteristiche utili hanno mostrato un’attività molto più debole, sottolineando quanto gli effetti antitumorali siano sensibili a piccoli cambiamenti strutturali.
Cosa differenzia i candidati più potenti
Confrontando strutture e risultati dei test, gli autori hanno ricostruito regole iniziali su ciò che funziona meglio. I composti più attivi tendevano a portare piccoli gruppi che donano densità elettronica al nucleo, migliorando le interazioni con i bersagli biologici. Mostravano inoltre un livello «giusto» di lipofilia—sufficientemente attratti dai lipidi da attraversare le membrane cellulari, ma non così grassi da aderire in modo non specifico a tutto. Inoltre le loro forme evitavano ingombri vicino alle regioni attive, consentendo un’incastonatura aderente nei siti di legame. Questi tratti sembravano aumentare sia il potere antiproliferativo sulle cellule tumorali sia la protezione delle cellule normali, suggerendo che le molecole potrebbero mirare in modo più selettivo a percorsi di cui i tumori dipendono.
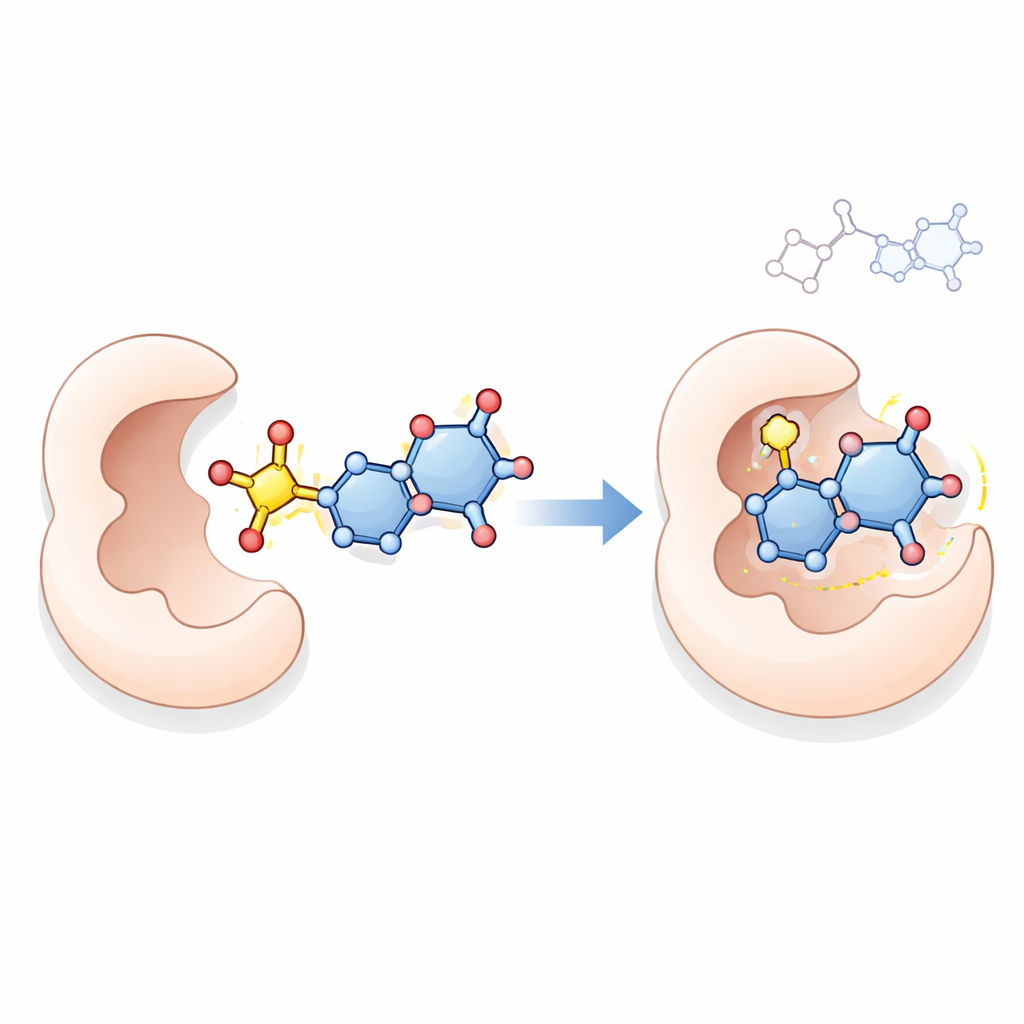
Uno sguardo più approfondito sul possibile meccanismo
Per esplorare una possibile modalità d’azione, il team ha usato il docking molecolare al computer, una tecnica che simula come una piccola molecola possa posizionarsi nel sito attivo di una proteina. Hanno esaminato l’interazione dei migliori composti 18, 21, 23 e 24 con la timidilato sintetasi, un enzima chiave di cui le cellule tumorali hanno bisogno per sintetizzare il DNA e noto bersaglio di farmaci come il 5‑fluorouracile. Le simulazioni hanno suggerito che queste nuove molecole, in particolare il composto 23, possono formare molteplici contatti stabilizzanti nella tasca dell’enzima, in alcuni casi legandosi con affinità superiore rispetto al farmaco di riferimento. Sebbene il docking da solo non possa provare come i composti agiscano nelle cellule viventi, offre una spiegazione plausibile coerente con i forti effetti antiproliferativi osservati.
Cosa significa per il futuro
Nel complesso, questo lavoro fornisce quattro molecole guida che combinano attività potente contro cellule di cancro del fegato e del seno con effetti più miti sulle cellule normali, insieme a indizi iniziali sulle caratteristiche strutturali che guidano questo equilibrio. In termini pratici, i ricercatori hanno tracciato un progetto chimico per candidati chemioterapici di nuova generazione potenzialmente efficaci e più rispettosi dei tessuti sani. Saranno necessari ulteriori studi su enzimi, cellule intere e infine modelli animali, ma questi ibridi pirimidina‑sulfonamide rappresentano un promettente passo verso trattamenti antitumorali più mirati e tollerabili.
Citazione: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Parole chiave: farmaci antitumorali, sulfonammidi, ibridi di pirimidina, timidilato sintetasi, docking molecolare