Clear Sky Science · pt
Desenvolvimento, síntese, docking molecular e avaliação citotóxica de novos derivados de sulfonamida à base de pirimidina como potentes agentes anticâncer: insights SAR e perfil biológico
Por que isso importa para o futuro do tratamento do câncer
Os quimioterápicos podem salvar vidas, mas muitos danificam tecidos saudáveis quase tanto quanto os tumores, provocando efeitos colaterais severos e limitando a intensidade com que os médicos podem tratar o câncer. Este estudo explora uma nova família de moléculas sintéticas projetadas para atingir as células cancerosas de forma mais eficaz do que as células saudáveis, visando tratamentos que sejam ao mesmo tempo potentes e mais suaves para o organismo. Ao combinar características de dois "blocos de construção" farmacêuticos conhecidos, os pesquisadores criaram e testaram compostos que podem servir como pontos de partida para drogas anticâncer mais seguras.
Construindo novas moléculas a partir de peças familiares
A equipe concentrou-se em duas famílias químicas que já têm papel central na medicina moderna. Uma são as sulfonamidas, uma classe antiga de fármacos originalmente famosa como antibióticos, mas hoje presentes em medicamentos para condições que vão desde glaucoma até hipertensão e câncer. A outra são as pirimidinas, estruturas em anel que fazem parte do nosso DNA e são amplamente usadas em fármacos anticâncer porque podem interferir na cópia do material genético pelas células. A ideia dos pesquisadores foi fundir esses dois motivos em moléculas híbridas únicas que possam reconhecer e interromper melhor os processos dos quais as células cancerosas dependem para se dividir.
Da síntese de bancada a uma biblioteca de candidatos
Usando síntese orgânica em etapas, os cientistas construíram um conjunto diverso de compostos de sulfonamida à base de pirimidina. Ao ligar a estrutura central a diferentes sistemas de anéis periféricos — como triazóis, pirazóis, tiazóis e triazinas — ajustaram propriedades como carga eletrônica, forma e lipossolubilidade. Essas características ajudam a determinar quão bem uma molécula consegue atravessar membranas celulares, alcançar seu alvo e evitar ficar retida ou ser eliminada. Cada nova estrutura foi cuidadosamente verificada com ferramentas padrão de análise química, garantindo que os pesquisadores soubessem exatamente o que haviam sintetizado antes de passar para os testes biológicos.
Colocando os novos compostos à prova
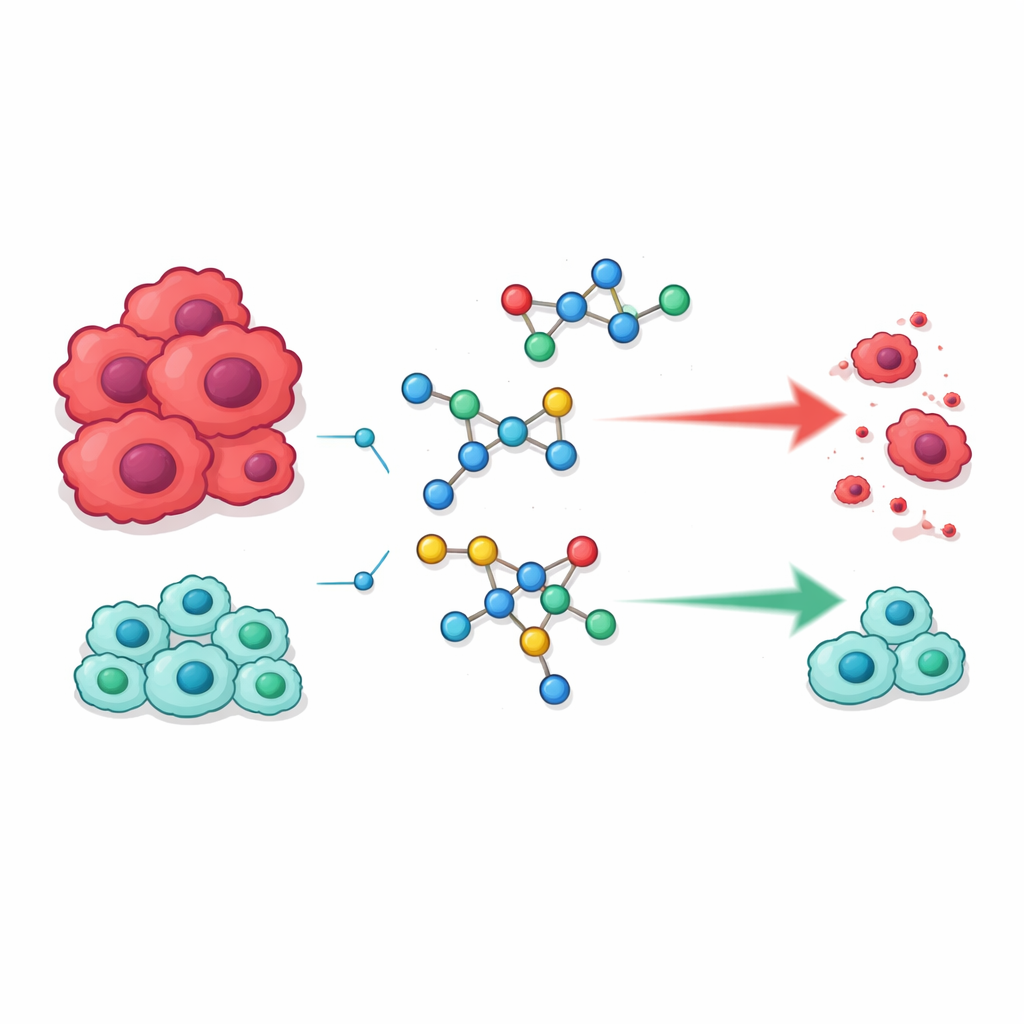
As novas moléculas foram triadas contra duas linhagens de células humanas cancerígenas — HepG2 (fígado) e MCF‑7 (mama) — bem como contra dois tipos de células normais, fibroblastos pulmonares WI‑38 e células renais VERO, para avaliar tanto potência quanto segurança. Vários candidatos se destacaram. Quatro compostos, rotulados 18, 21, 23 e 24, eliminaram células cancerígenas em concentrações semelhantes ou inferiores às necessárias para o fármaco amplamente usado 5‑fluorouracil. No entanto, ao contrário do 5‑fluorouracil, esses mesmos compostos foram notavelmente menos prejudiciais às células normais, sugerindo um balanço mais favorável entre eficácia e toxicidade. Outros membros da série que não possuíam certos elementos benéficos mostraram atividade muito mais fraca, ressaltando quão sensíveis são os efeitos anticâncer a pequenas alterações estruturais.
O que diferencia os candidatos mais potentes
Ao comparar estruturas e resultados dos testes, os autores reuniram regras iniciais sobre o que funciona melhor. Os compostos mais ativos tendiam a portar pequenos grupos que doam densidade eletrônica ao arcabouço central, melhorando a interação das moléculas com seus alvos biológicos. Também mostraram um nível "na medida" de lipofilicidade — suficientemente atraídos por lipídios para atravessar membranas celulares, mas não tão apolares a ponto de se ligarem de forma inespecífica a tudo. Além disso, suas formas evitavam obstáculos volumosos perto das regiões ativas, permitindo um encaixe preciso nos sítios de ligação. Essas características pareceram aumentar tanto o poder de eliminar células cancerosas quanto a preservação das células normais, sugerindo que as moléculas podem estar se dirigindo de forma mais seletiva a vias das quais os tumores dependem.
Uma visão mais detalhada de como podem atuar
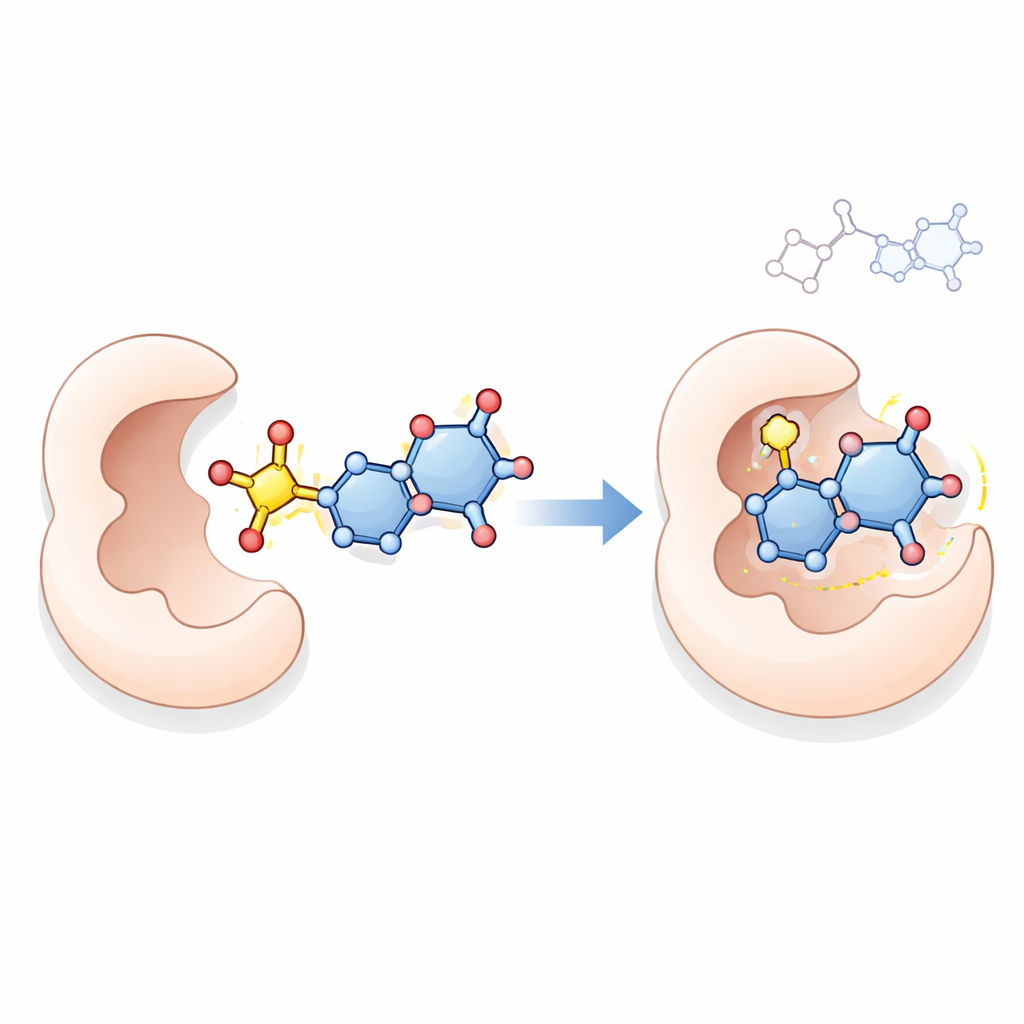
Para explorar um possível modo de ação, a equipe utilizou docking molecular assistido por computador, uma técnica que simula como uma pequena molécula pode acomodar‑se no sítio ativo de uma proteína. Eles examinaram como os principais compostos 18, 21, 23 e 24 interagem com a timidilato sintase, uma enzima chave que as células cancerígenas precisam para produzir DNA e alvo conhecido de drogas como o 5‑fluorouracil. As simulações sugeriram que essas novas moléculas, especialmente o composto 23, podem formar múltiplos contatos estabilizadores dentro do bolso da enzima, em alguns casos se ligando mais fortemente do que o fármaco de referência. Embora o docking por si só não comprove como os compostos atuam em células vivas, ele oferece uma explicação plausível consistente com seus fortes efeitos antiproliferativos.
O que isso significa daqui para frente
No conjunto, este trabalho apresenta quatro moléculas líderes que combinam atividade potente contra células de câncer de fígado e mama com efeitos mais brandos sobre células normais, juntamente com pistas iniciais sobre as características estruturais que promovem esse equilíbrio. Em termos práticos, os pesquisadores esboçaram um projeto químico para candidatos a quimioterápicos de próxima geração que podem ser tanto eficazes quanto menos agressivos ao tecido saudável. Serão necessários estudos adicionais em enzimas, em células completas e, eventualmente, em modelos animais, mas esses híbridos pirimidina‑sulfonamida representam um passo promissor rumo a tratamentos anticâncer mais direcionados e toleráveis.
Citação: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Palavras-chave: medicamentos anticâncer, sulfonamidas, híbridos de pirimidina, timidilato sintase, docking molecular