Clear Sky Science · ar
تصميم وتخليق وربط جزيئي وتقييم سمية خلوية لمشتقات سلفوناميد جديدة مبنية على البيريميدين كعوامل مضادة للسرطان قوية: رؤى البنية‑النشاط والتوصيف البيولوجي
لماذا يهم هذا لعلاج السرطان في المستقبل
قد تنقذ أدوية العلاج الكيميائي الأرواح، لكن كثيرًا منها يضر بالأنسجة السليمة تقريبًا بقدر ما يضر بالأورام، مما يؤدي إلى آثار جانبية قاسية ويقيد مدى شدة المعالجة التي يمكن للأطباء إعطاؤها. تستكشف هذه الدراسة عائلة جديدة من الجزيئات المصنوعة مخبريًا المصممة لاستهداف الخلايا السرطانية بشكل أقوى من الخلايا السليمة، بهدف علاجات تكون قوية وفي الوقت نفسه ألطف على الجسم. من خلال مزج خواص من اثنين من "لبِنات" الأدوية المعروفة، أنشأ الباحثون واختبروا مركبات قد تكون نقاط انطلاق لأدوية مضادة للسرطان آمنة أكثر.
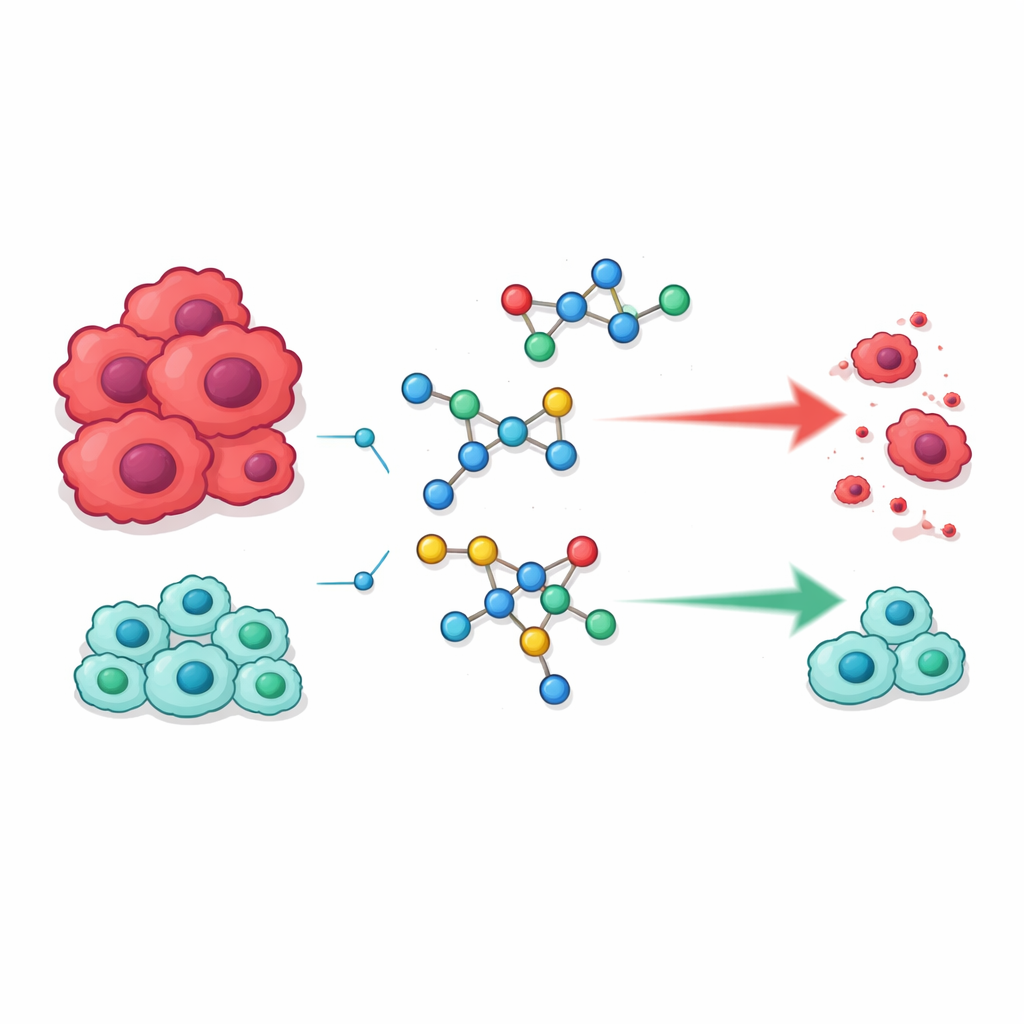
بناء جزيئات جديدة من قطع مألوفة
ركز الفريق على عائلتين كيميائيتين تلعبان بالفعل أدوارًا بارزة في الطب الحديث. الأولى هي السلفوناميدات، وهي فئة قديمة من الأدوية اشتهرت أصلاً كمضادات حيوية لكنها توجد الآن في أدوية لعلاجات تتراوح من الزرق إلى ارتفاع ضغط الدم والسرطان. والثانية هي البيريميدينات، تراكيب حلقية تشكل جزءًا من حمضنا النووي وتستخدم على نطاق واسع في أدوية السرطان لأنها يمكن أن تتداخل مع طريقة نسخ الخلايا لموادها الوراثية. كانت فكرة الباحثين دمج هاتين الوحدتين في جزيئات هجينة واحدة قد تتعرف وتعيق بشكل أفضل العمليات التي تعتمد عليها خلايا السرطان للانقسام.
من كيمياء المختبر إلى مكتبة من المرشحين
باستخدام تخليق عضوي خطوة بخطوة، بنى العلماء مجموعة متنوعة من مركبات السلفوناميد المبنية على البيريميدين. من خلال ربط الإطار الأساسي بأنظمة حلقية محيطة مختلفة—مثل التريازولات، البيرازولات، الثيازولات، والتريازينات—عدّلوا خصائص مثل الشحنة الإلكترونية والشكل والذوبانية في الدهون. هذه الخصائص تساعد على تحديد مدى قدرة الجزيء على عبور أغشية الخلايا، والوصول إلى هدفه، وتجنب أن يعلق أو يُطرد. كل بنية جديدة تم التحقق منها بعناية باستخدام أدوات التحليل الكيميائي القياسية، لضمان معرفة الباحثين بالضبط ما صنعوه قبل الانتقال للاختبارات البيولوجية.
اختبار المركبات الجديدة
تم فحص الجزيئات الجديدة ضد سلسلتي خلايا سرطانية بشرية—HepG2 (كبد) وMCF‑7 (ثدي)—وكذلك نوعين من الخلايا الطبيعية، هي أرومات ليفية رئوية WI‑38 وخلايا الكلى VERO، لتقييم كل من الفعالية والسلامة. برز عدد من المرشحين. أربع مركبات، موسومة بالأرقام 18 و21 و23 و24، قتلت الخلايا السرطانية بتركيزات مشابهة أو أقل من تلك المطلوبة للدواء المستخدم على نطاق واسع 5‑فلورويوراسيل. ومع ذلك، وعلى خلاف 5‑فلورويوراسيل، كانت هذه المركبات نفسها أقل ضررًا بشكل ملحوظ للخلايا الطبيعية، مما يشير إلى توازن أفضل بين الفعالية والسمية. أظهرت أعضاء أخرى في السلسلة تفتقر لميزات مفيدة ضعفًا أكبر في النشاط، مما يؤكد حساسية التأثيرات المضادة للسرطان للتغيرات الهيكلية الصغيرة.
ما الذي يجعل أقوى المرشحين مختلفين
من خلال مقارنة الهياكل ونتائج الاختبارات، جمع المؤلفون قواعد أولية حول ما يعمل بشكل أفضل. الميل إلى أن تكون المركبات الأكثر نشاطًا حاملة لمجموعات صغيرة مانحة للكثافة الإلكترونية إلى الإطار الأساسي، مما يحسن كيفية تفاعل الجزيئات مع أهدافها البيولوجية. أظهرت أيضًا مستوى "مناسبًا" من الذوبانية في الدهون—جذب كافٍ للدهون للانزلاق عبر أغشية الخلايا، لكنه ليس دهنيًا جدًا بحيث يلتصق بشكل غير نوعي بكل شيء. بالإضافة إلى ذلك، كانت أشكالها تتجنب العقبات الضخمة بالقرب من المناطق الفعالة، مما يسمح بملاءمة محكمة داخل مواقع الارتباط. بدت هذه السمات معززة لكل من قدرة قتل الخلايا السرطانية وتوفير الحماية للخلايا الطبيعية، مما يوحي بأن الجزيئات قد تستهدف بشكل أكثر انتقائية المسارات التي تعتمد عليها الأورام.
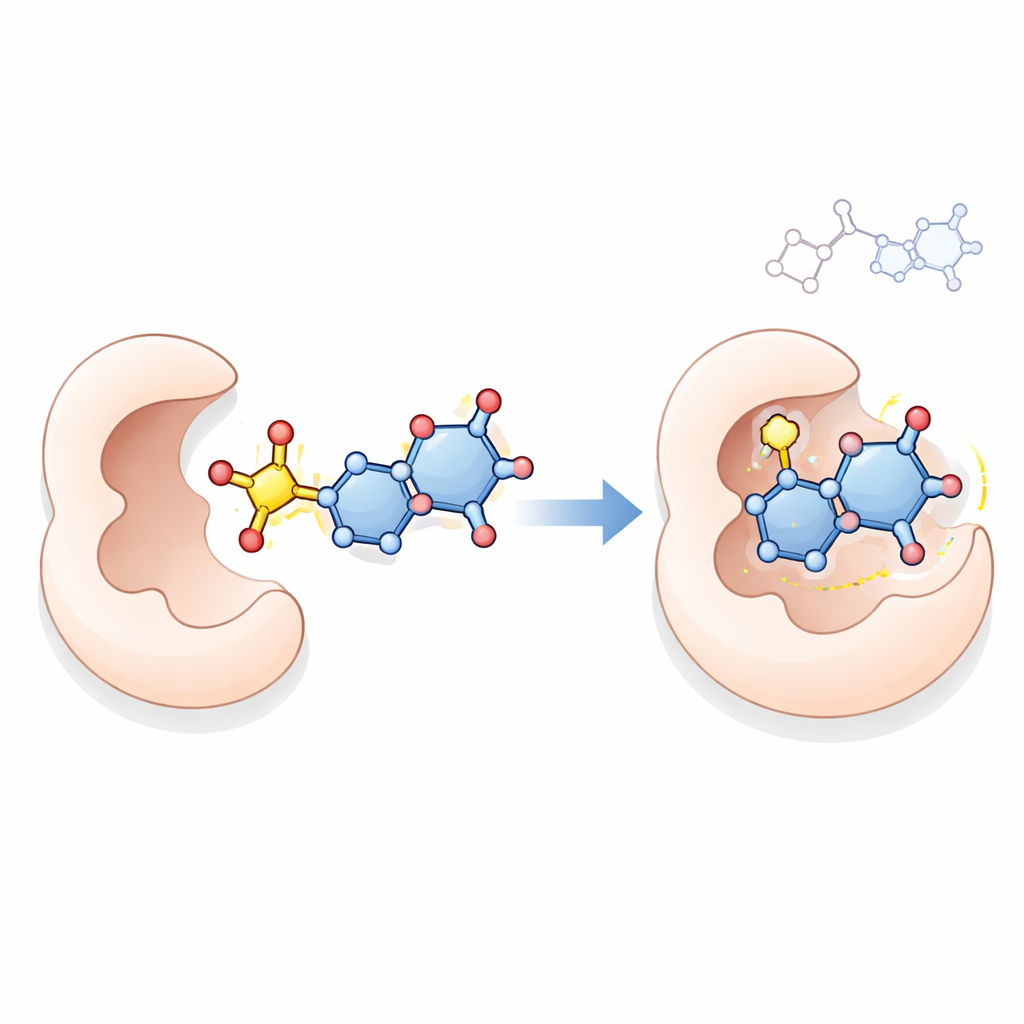
نظرة أقرب على كيفية عملها المحتمل
لاستكشاف وضع محتمل لآلية العمل، استخدم الفريق الربط الجزيئي الحاسوبي، وهي تقنية تحاكي كيف قد يجلس جزيء صغير داخل الموقع النشط للبروتين. درسوا كيفية تفاعل المركبات الأعلى أداءً 18 و21 و23 و24 مع ثيميديلات سينثاز، وهو إنزيم رئيسي تحتاجه خلايا السرطان لصنع الحمض النووي وهدف معروف لأدوية مثل 5‑فلورويوراسيل. أشارت المحاكاة إلى أن هذه الجزيئات الجديدة، وبالأخص المركب 23، يمكنها تكوين اتصالات مثبّتة متعددة داخل جيب الإنزيم، وفي بعض الحالات ترتبط بقوة أكبر من الدواء المرجعي. في حين أن الربط وحده لا يثبت كيف تعمل المركبات داخل الخلايا الحية، فإنه يقدم تفسيرًا معقولًا يتماشى مع تأثيراتها القوية المضادة للتكاثر.
ما معنى هذا للمستقبل
بشكل عام، يقدم هذا العمل أربعة جزيئات رائدة تجمع بين نشاط قوي ضد خلايا سرطان الكبد والثدي وتأثيرات أخف على الخلايا الطبيعية، إلى جانب أدلة مبكرة حول السمات الهيكلية التي تقود هذا التوازن. بمصطلحات يومية، رسم الباحثون مخططًا كيميائيًا أوليًا لمرشحي جراحة كيميائية جيوستهداف للجيل القادم الذين قد يكونون فعالين وأكثر لطفًا تجاه الأنسجة السليمة. ستكون هناك حاجة لدراسات إضافية على الإنزيمات والخلايا الكاملة وفي النهاية الحيوانات، لكن هذه الهجن من البيريميدين والسلفوناميد تمثل خطوة واعدة نحو علاجات سرطانية أكثر استهدافًا وتحملًا.
الاستشهاد: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
الكلمات المفتاحية: أدوية مضادة للسرطان, سلفوناميدات, هجن بيريميدين, ثيميديلات سينثاز, الربط الجزيئي