Clear Sky Science · fr
Conception, synthèse, docking moléculaire et évaluation cytotoxique de nouveaux dérivés sulfonamides à base de pyrimidine en tant qu’agents anticancéreux puissants : perspectives SAR et profilage biologique
Pourquoi cela compte pour les soins du cancer à venir
Les médicaments chimiothérapeutiques peuvent sauver des vies, mais beaucoup endommagent les tissus sains presque autant que les tumeurs, entraînant des effets secondaires sévères et limitant l’intensité des traitements que les médecins peuvent appliquer. Cette étude explore une nouvelle famille de molécules synthétiques conçues pour frapper davantage les cellules cancéreuses que les cellules saines, visant des traitements à la fois puissants et plus doux pour l’organisme. En combinant des caractéristiques de deux « blocs de construction » médicinaux bien connus, les chercheurs ont créé et testé des composés qui pourraient servir de points de départ pour des médicaments anticancéreux plus sûrs.
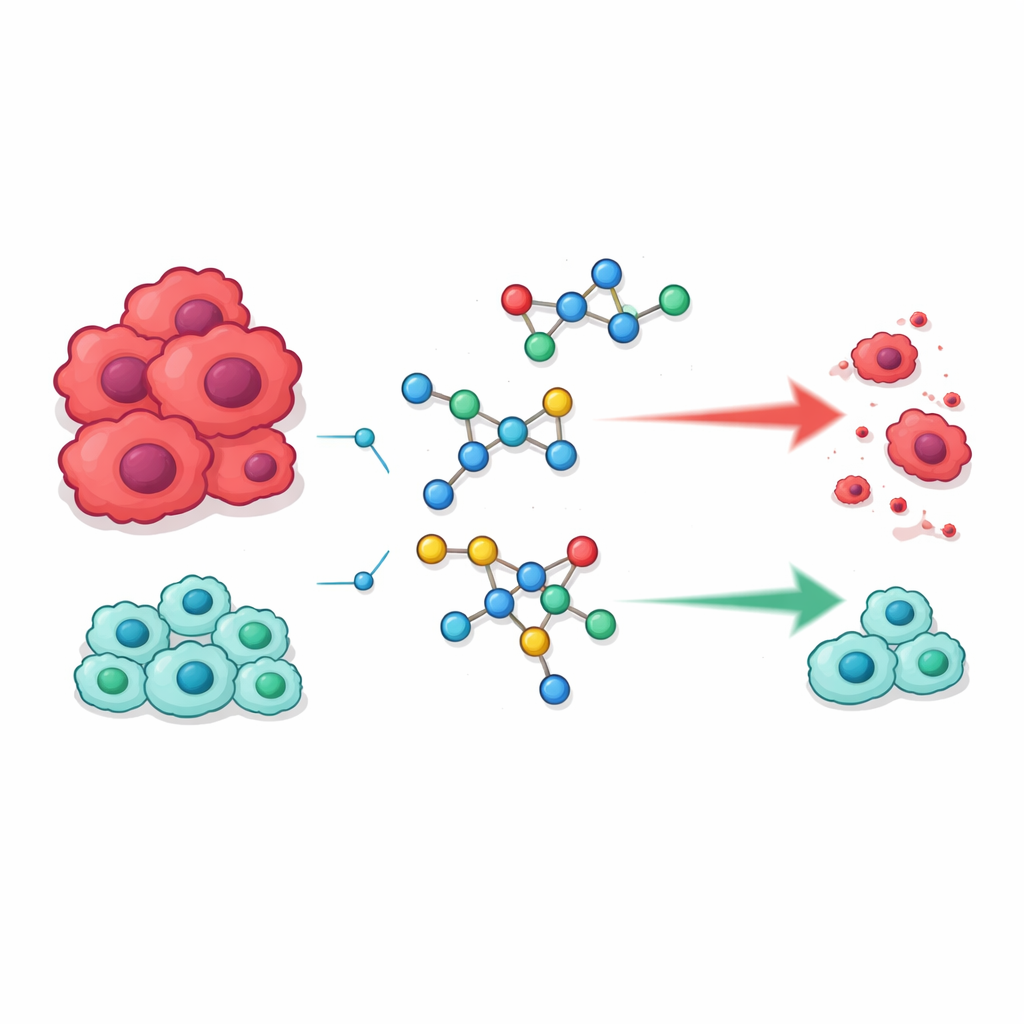
Construire de nouvelles molécules à partir d’éléments familiers
L’équipe s’est concentrée sur deux familles chimiques qui jouent déjà un rôle majeur en médecine moderne. L’une est celle des sulfonamides, une classe ancienne de médicaments initialement célèbre comme antibiotiques mais désormais présente dans des traitements allant du glaucome à l’hypertension et au cancer. L’autre est celle des pyrimidines, structures en anneau qui font partie de notre ADN et sont largement utilisées dans les médicaments anticancéreux car elles peuvent interférer avec la copie du matériel génétique des cellules. L’idée des chercheurs était de fusionner ces deux motifs en molécules hybrides uniques susceptibles de mieux reconnaître et perturber les processus dont les cellules cancéreuses dépendent pour se diviser.
De la chimie de paillasse à une bibliothèque de candidats
Par synthèse organique étape par étape, les scientifiques ont construit un ensemble diversifié de composés sulfonamides à base de pyrimidine. En reliant le squelette central à différents systèmes d’anneaux périphériques — tels que triazoles, pyrazoles, thiazoles et triazines — ils ont ajusté des propriétés comme la charge électronique, la conformation et la lipophilie. Ces caractéristiques déterminent en partie la capacité d’une molécule à traverser les membranes cellulaires, atteindre sa cible et éviter d’être piégée ou éliminée. Chaque nouvelle structure a été soigneusement vérifiée à l’aide d’outils standards d’analyse chimique, garantissant que les chercheurs connaissaient précisément ce qu’ils avaient synthétisé avant de passer aux tests biologiques.
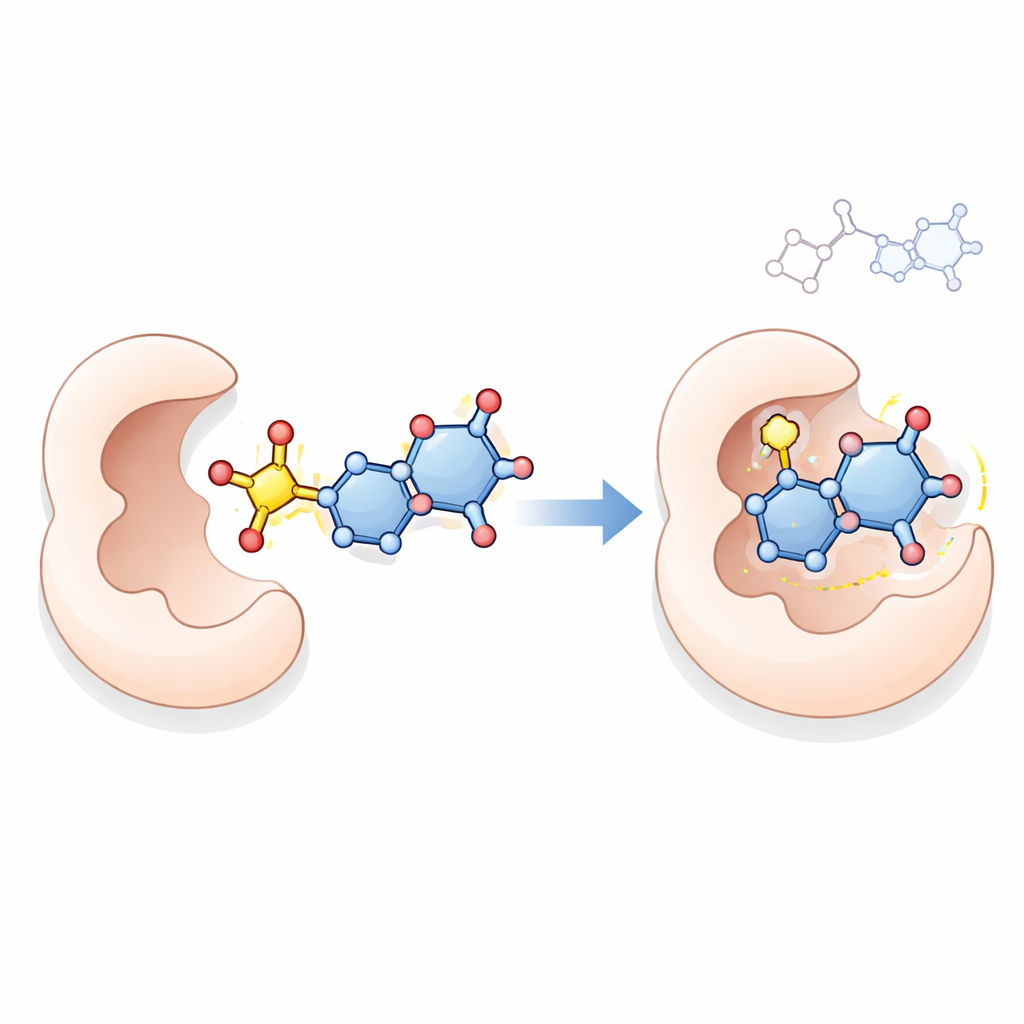
Mettre les nouveaux composés à l’épreuve
Les nouvelles molécules ont été criblées contre deux lignées cellulaires cancéreuses humaines — HepG2 (foie) et MCF‑7 (sein) — ainsi que contre deux types de cellules normales, des fibroblastes pulmonaires WI‑38 et des cellules rénales VERO, afin d’évaluer à la fois la puissance et la sécurité. Plusieurs candidats se sont distingués. Quatre composés, notés 18, 21, 23 et 24, ont tué les cellules cancéreuses à des concentrations similaires ou inférieures à celles nécessaires pour le médicament largement utilisé 5‑fluorouracile. Cependant, contrairement au 5‑fluorouracile, ces mêmes composés étaient notablement moins nocifs pour les cellules normales, suggérant un meilleur équilibre entre efficacité et toxicité. D’autres membres de la série dépourvus de certaines caractéristiques bénéfiques montraient une activité beaucoup plus faible, soulignant la sensibilité des effets anticancéreux à de petits changements structuraux.
Ce qui distingue les candidats les plus puissants
En comparant structures et résultats, les auteurs ont reconstitué des règles préliminaires sur ce qui fonctionne le mieux. Les composés les plus actifs avaient tendance à porter de petits groupes donneurs d’électrons sur le squelette central, améliorant les interactions avec leurs cibles biologiques. Ils présentaient également un niveau de lipophilie « juste adapté » — suffisamment attirés par les lipides pour traverser les membranes cellulaires, mais pas si gras qu’ils se lient de manière non spécifique à tout. De plus, leurs formes évitaient les encombrements volumineux près des régions actives, permettant un ajustement serré dans les sites de liaison. Ces caractéristiques semblaient augmenter à la fois le pouvoir antiprolifératif sur les cellules cancéreuses et la protection des cellules normales, laissant penser que les molécules ciblent plus sélectivement les voies dont dépendent les tumeurs.
Un regard plus approfondi sur leur mode d’action possible
Pour explorer un mode d’action possible, l’équipe a utilisé le docking moléculaire assisté par ordinateur, une technique qui simule la façon dont une petite molécule peut se loger dans le site actif d’une protéine. Ils ont examiné les interactions des meilleurs composés 18, 21, 23 et 24 avec la thymidylate synthase, une enzyme clé dont les cellules cancéreuses ont besoin pour synthétiser l’ADN et cible connue de médicaments comme le 5‑fluorouracile. Les simulations suggèrent que ces nouvelles molécules, en particulier le composé 23, peuvent former plusieurs contacts stabilisants dans la poche de l’enzyme, se liant dans certains cas plus fortement que le médicament de référence. Bien que le docking à lui seul ne puisse pas prouver le mécanisme d’action dans des cellules vivantes, il fournit une explication plausible cohérente avec leurs forts effets antiprolifératifs.
Ce que cela signifie pour la suite
Dans l’ensemble, ce travail met en évidence quatre molécules candidates qui allient une activité puissante contre des cellules cancéreuses hépatiques et mammaires à des effets plus modérés sur des cellules normales, ainsi que des indices initiaux sur les caractéristiques structurales qui sous-tendent cet équilibre. En termes concrets, les chercheurs ont dessiné un plan chimique pour des candidats chimiothérapeutiques de nouvelle génération susceptibles d’être à la fois efficaces et moins agressifs pour les tissus sains. Des études complémentaires sur des enzymes, des cellules entières et, finalement, des animaux seront nécessaires, mais ces hybrides pyrimidine‑sulfonamide marquent une étape prometteuse vers des traitements du cancer plus ciblés et mieux tolérés.
Citation: Bayoumy, N.M., Fadda, A.A., Gaffer, H.E. et al. Design, synthesis, molecular docking and cytotoxic evaluation of novel pyrimidine-based sulfonamide derivatives as potent anticancer agents: SAR insights and biological profiling. Sci Rep 16, 9820 (2026). https://doi.org/10.1038/s41598-026-41711-z
Mots-clés: médicaments anticancéreux, sulfonamides, hybrides de pyrimidine, thymidylate synthase, docking moléculaire