Clear Sky Science · tr
Kompleksiform-açık kovalent TRMT112 ligandleri ve METTL5’i allosterik olarak agonize etmeleri
Kalabalık Bir Hücrede Tek Bir Oyuncuyu Hedeflemek
Her insan hücresinin içinde, enerji kullanımından beyin devrelerinin şekillenmesine kadar her şeyi kontrol etmek için açılıp kapanan binlerce farklı protein makinesi yan yana bulunur. Bu makinelerin birçoğu, farklı kombinasyonlarda birbirine kenetlenen birden çok protein parçasından oluşur ve benzeyen ama ayrı kompleks aileleri oluşturur. Bu makale, kimyagerlerin bu tür bir kompleksin yalnızca belirli bir versiyonuna kenetlenen küçük moleküller tasarlayabileceğini ve onu kapatmak yerine aslında daha aktif hale getirebileceğini gösterir. Çalışma, ribozomların genetik bilgiyi nasıl okuduğunu ayarlamaya yardımcı olan bir protein çiftine odaklanarak, protein üretimini yüksek doğrulukla ayarlamak için yeni bir yol sunar.
Neden Protein Karışımı Önemli?
Yaklaşık 20.000 genimiz, 20.000’den çok daha fazla farklı protein varlığına yol açar. RNA kesilip biçimlendikten, kimyasal olarak değiştirildikten ve çok proteinli makineler halinde bir araya geldikten sonra her gen birçok “proteoform” üretebilir. Önemli kategorilerden biri de “kompleksoformlar”dır—ilişkili ama ayrı kompleksler oluşturan farklı protein birleşimleri. TRMT112 adlı küçük bir adaptör proteini bunun çarpıcı bir örneğidir. TRMT112, RNA, DNA veya proteinlere küçük kimyasal etiketler ekleyen çeşitli metiltransferaz enzimlerine bağlanan bir merkez görevi görür. TRMT112 birçok enzimle ortaklık kurduğundan, onu genetik olarak veya kaba bir ilaçla kapatmak birden çok yolu aynı anda bozardı. Yazarlar bunun yerine şunu sordular: yalnızca tek bir TRMT112 ortaklığına bağlanan ve yalnızca o enzimin davranışını değiştiren bir bileşik bulabilir miyiz?
İnce Kimyasal Problar Tasarlamak
Bu fikri araştırmak için araştırmacılar bisiklopirolidin akrilamidler adı verilen yeni, kompakt, üç boyutlu moleküller ailesi geliştirdiler. Bu bileşikler, genellikle proteinlerin reaktif ceplerinde bulunan kükürt içeren bir amino asit olan sistein ile kovalent olarak reaksiyona girecek şekilde tasarlandı. Aktivite temelli protein profilleme olarak bilinen bir kemoproteomik yöntem kullanarak, canlı kanser hücrelerini bu bileşiklerin ayna görüntüsü çiftlerine maruz bıraktılar ve sonra kütle spektrometrisi ile hangi proteinlerin işaretlendiğini incelediler. Her ayna görüntüsünün ne kadar kuvvetle bağlandığını karşılaştırarak şekle bağımlı etkileşimleri tespit edebildiler. Yeni bileşikler, önceki probaileşmelerden daha az genel olarak reaktif olmalarına rağmen, TRMT112 de dahil olmak üzere farklı bir protein setini hedefledi.
Tek Bir Tercih Edilen Ortaklığı Bulmak
Daha yakından yapılan analiz garip bir uyumsuzluğu ortaya koydu. Bütün proteinleri izleyen bir test, probların TRMT112’nin standart bir etiketleme reaktifinden neredeyse tamamen korunmasını sağladığını öne sürdü. Ancak tekil sistein bölgelerine bakan daha doğrudan ikinci bir test, TRMT112’deki tek bir belirli sistein üzerinde yalnızca ılımlı bir etki gösterdi. Bu, bileşiklerin tüm TRMT112 moleküllerinin yalnızca bir kısmını—belirli bir ortakla bağlı olan kısmını—tanıdığına işaret ediyordu. Hücre özlerini boyuta göre ayırıp, farklı bilinen TRMT112 ortaklarını birlikte eksprese ederek, prob bağlanmasının yalnızca TRMT112’nin METTL5 adlı ve küçük ribozomal RNA’daki belirli bir adenini değiştiren bir enzimle eşleştiğinde göründüğünü gösterdiler. METTL5’in yok edilmesi etkileşimi ortadan kaldırdı ve METTL5 seviyelerinin hücre hatları arasında değiştirilmesi, ne kadar TRMT112’nin etkilendiğini değiştirdi; bu da probun bir TRMT112:METTL5 kompleksoformunu tanıdığını doğruladı.
Moleküler Arayüzü Görmek ve Ayarlamak
Bu ortaklığı belirledikten sonra yazarlar moleküllerini daha sıkı ve seçici bağlanacak şekilde rafine ettiler. Optimize edilmiş bir bileşik olan FWG‑33B, METTL5 ile arayüzde tam olarak bulunan TRMT112 üzerindeki tek bir sistein ile reaksiyona girdi. Kompleksin X-ışını kristalografisi, FWG‑33B’nin her iki protein tarafından ortaklaşa oluşturulan bir cebe yerleştiğini gösterdi; bu cep METTL5’in aktif bölgesinden uzaktaydı ama enzimin kofaktör bağlama bölgesine yakın, esnek bir döngünün ince bir yeniden şekillenmesini tetikleyecek kadar yakındı. Bu bileşik cep yalnızca TRMT112:METTL5 kompleksinde var olup TRMT112’nin diğer enzimlerle oluşturduğu benzer komplekslerde yoktu. Sentetik RNA fragmanlarıyla yapılan biyokimyasal testler fonksiyonel sonucu ortaya koydu: FWG‑33B’nin kovalent bağlanmasından sonra METTL5, RNA substratına daha kolay bağlandı ve onu yaklaşık iki kat daha verimli metiletti; hedeflenen sisteini kaldıran kontrol mutasyonu ise bu artışı ortadan kaldırdı.
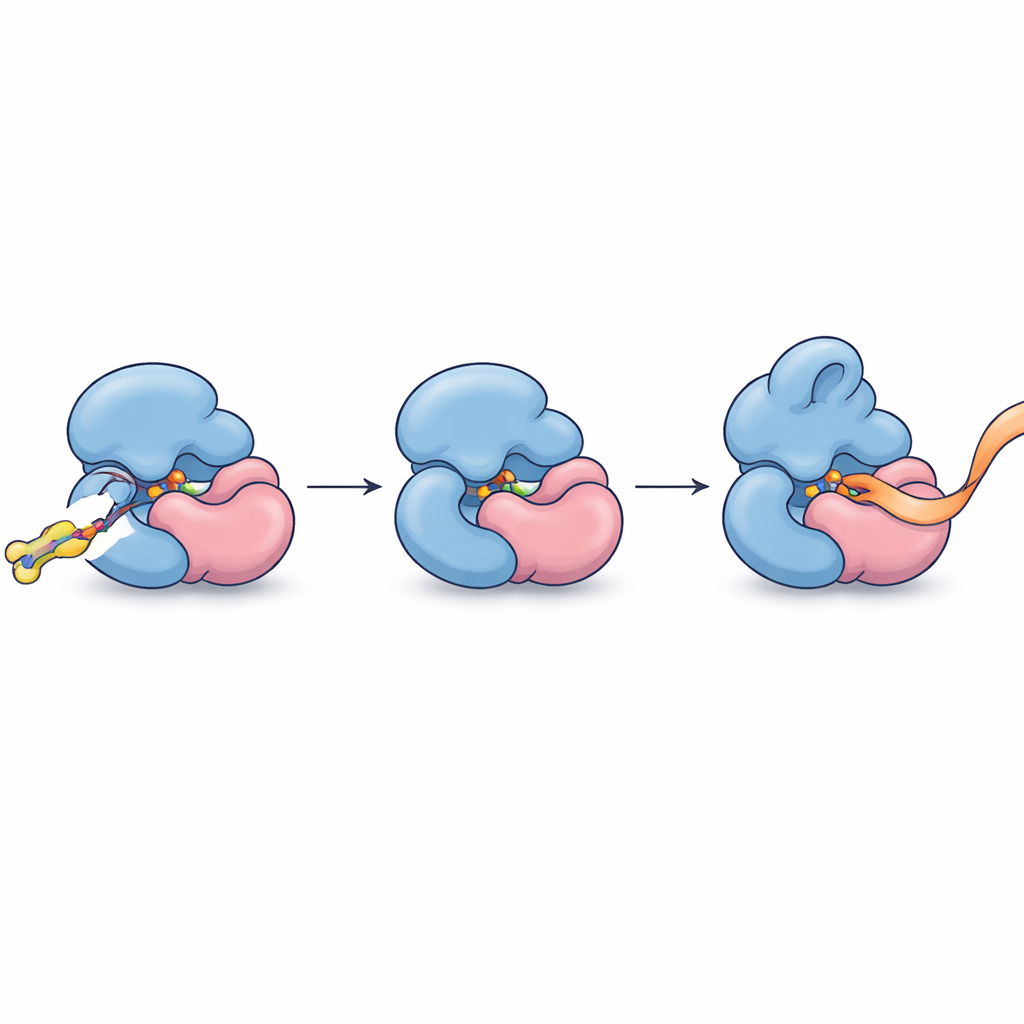
Kesin Bağlanmayı Kesin Kontrole Dönüştürmek
Günlük ifadeyle, araştırmacılar iki protein parçası arasındaki dikişe küçük bir moleküler kama sokarak onların RNA’ya tutuşlarını hafifçe sıkılaştırmanın ve yeniden şekillendirmenin bir yolunu buldular; böylece bir metilasyon enziminin akranlarını rahatsız etmeden daha hızlı çalışmasını sağladılar. Bu, daha önce hedeflenmesi çok kaba olduğu düşünülen yüksek bağlantılı adaptör proteinlerin bile, kovalent kimya ve proteom çapında profilleme kullanılarak bireysel kompleksler düzeyinde ele alınabileceğini gösterir. METTL5 için ilk allosterik kimyasal agonistleri sağlamanın ötesinde—METTL5 beyin gelişimi, metabolizma ve kanser ile giderek daha fazla ilişkilendirilen bir enzimdir—çalışma hücrenin doğal ortamında kalabalık protein ailelerinin tek bir üyesini tanıyan ve ayarlayan küçük moleküller keşfetmek için genel bir reçete sunar.
Atıf: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Anahtar kelimeler: protein kompleksleri, kimyasal problar, RNA metilasyonu, allosterik modülasyon, kemoproteomik