Clear Sky Science · pt
Ligantes covalentes restritos a complexoformas de TRMT112 que agonizam alostericamente METTL5
Alvejando Um Ator em Uma Célula Lotada
Dentro de cada célula humana, milhares de máquinas proteicas diferentes disputam espaço, ligando‑se e desligando‑se para controlar tudo, desde o uso de energia até a arquitetura do cérebro. Muitas dessas máquinas são construídas a partir de várias partes proteicas que se encaixam em combinações distintas, criando famílias de complexos semelhantes. Este artigo mostra como químicos podem construir pequenas moléculas que se prendem a apenas uma versão específica de um desses complexos e, em vez de bloqueá‑la, na verdade a fazem funcionar mais. O trabalho foca em um par de proteínas que ajuda a ajustar como os ribossomos leem a informação genética, oferecendo uma nova forma de regular a produção de proteínas com grande precisão.
Por Que a Mistura de Proteínas Importa
Nossos cerca de 20.000 genes dão origem a muito mais do que 20.000 entidades proteicas distintas. Após o emaranhamento do RNA, modificações químicas e montagem em máquinas multiproteicas, cada gene pode gerar muitas “proteoformas”. Uma categoria importante são as “complexoformas”—combinações diferentes de proteínas que formam complexos relacionados, porém distintos. Uma pequena proteína adaptadora chamada TRMT112 é um exemplo marcante. Ela atua como um hub, ligando‑se a várias metiltransferases que acrescentam pequenos marcadores químicos ao RNA, ao DNA ou a proteínas. Porque o TRMT112 se associa a muitos enzimas, desligá‑lo geneticamente ou com uma droga de efeito amplo embaralharia múltiplas vias de uma vez. Os autores perguntaram, em vez disso: podemos encontrar um composto que só se liga a uma única parceria de TRMT112 e mude o comportamento apenas desse enzima?
Desenhando Sondas Químicas Sutis
Para explorar essa ideia, os pesquisadores construíram uma nova família de moléculas compactas e tridimensionais chamadas acrilamidas biciclopirrolidina. Esses compostos foram projetados para reagir covalentemente com cisteína, um aminoácido contendo enxofre que frequentemente fica em bolsões reativos das proteínas. Usando um método quimio‑proteômico conhecido como profileamento de proteínas baseado em atividade, expuseram células cancerígenas vivas a pares de versões em imagem espelhada desses compostos e então usaram espectrometria de massa para ver quais proteínas foram marcadas. Ao comparar o quanto cada imagem espelhada se ligava, puderam identificar interações altamente dependentes da forma. Apesar de serem menos reativos de forma geral do que famílias de sondas anteriores, os novos compostos atingiram um conjunto distinto de proteínas, incluindo TRMT112.
Encontrando Uma Única Parceria Favorecida
Análises mais detalhadas revelaram uma discrepância curiosa. Um ensaio que observa proteínas inteiras sugeria que as sondas praticamente impediam o TRMT112 de ser rotulado por um reagente padrão. Contudo, um segundo ensaio, mais direto, que examina sítios individuais de cisteína mostrou apenas um efeito modesto em uma cisteína específica do TRMT112. Isso indicou que os compostos estavam reconhecendo apenas uma fração de todas as moléculas de TRMT112—a fração ligada a um parceiro específico. Separando extratos celulares por tamanho e coexpressando diferentes parceiros conhecidos de TRMT112, a equipe mostrou que a ligação da sonda aparecia somente quando o TRMT112 estava pareado com uma enzima, METTL5, que modifica uma adenina específica no pequeno RNA ribossômico da célula. A deleção de METTL5 eliminou a interação, e variar os níveis de METTL5 entre linhagens celulares alterou quanto TRMT112 era engajado, confirmando que a sonda reconhece uma complexoforma TRMT112:METTL5.
Vendo e Ajustando a Interface Molecular
Tendo identificado essa parceria, os autores refinaram suas moléculas para se ligarem com maior afinidade e seletividade. Um composto otimizado, FWG‑33B, reagiu com uma única cisteína no TRMT112 localizada exatamente na interface com o METTL5. Cristalografia de raio X do complexo mostrou o FWG‑33B encravado em um bolsão formado conjuntamente por ambas as proteínas, distante do sítio ativo do METTL5, mas próximo o suficiente para desencadear uma reconfiguração sutil de uma alça flexível perto da região de ligação do cofator da enzima. Esse bolsão composto existe apenas no complexo TRMT112:METTL5 e não em complexos similares que o TRMT112 forma com outras enzimas. Ensaios bioquímicos com fragmentos de RNA sintético revelaram o desfecho funcional: após a ligação covalente do FWG‑33B, o METTL5 ligou‑se ao seu substrato de RNA com mais facilidade e metilou‑o cerca de duas vezes mais eficientemente, enquanto uma mutação de controle que removeu a cisteína alvo aboliu esse aumento.
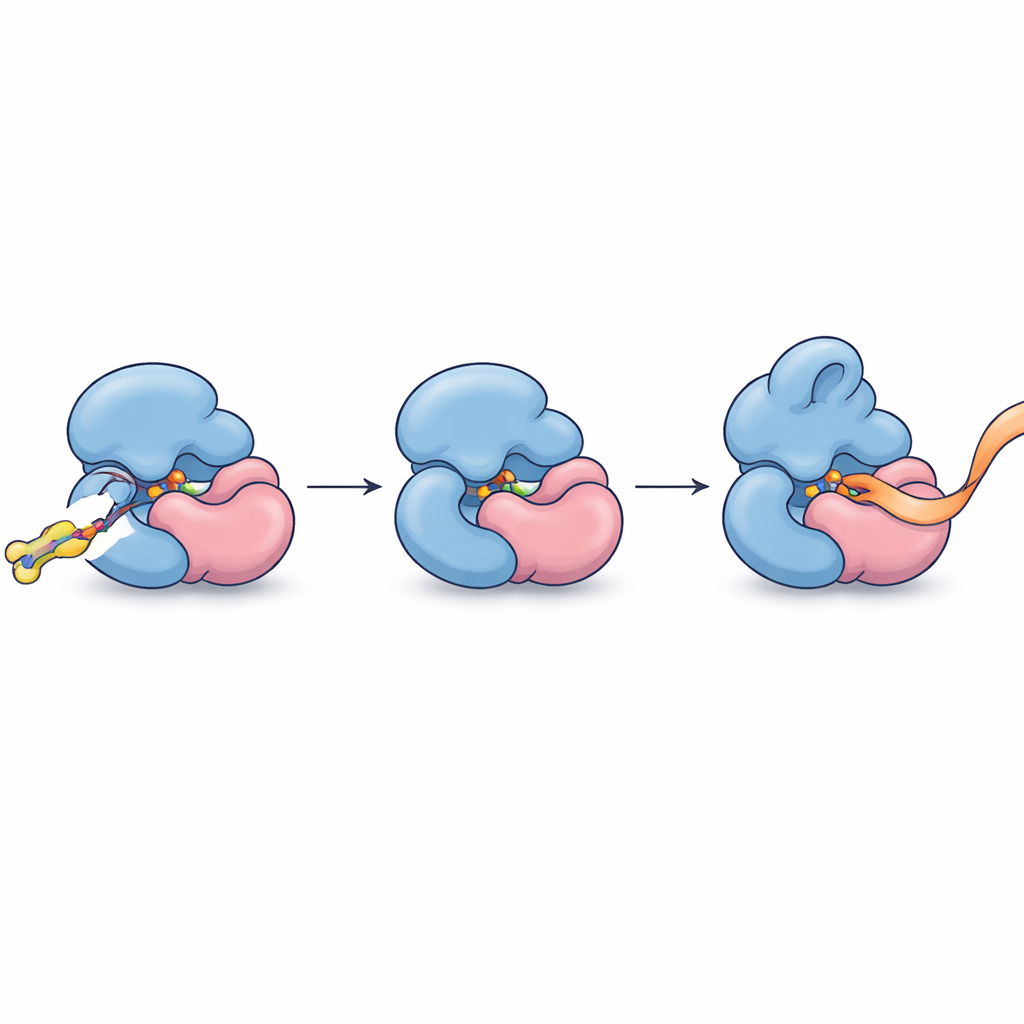
Transformando Ligação Precisa em Controle Preciso
Em termos cotidianos, os pesquisadores descobriram uma maneira de inserir uma pequena cunha molecular na emenda entre duas partes proteicas para apertar e remodelar sutilmente sua aderência ao RNA, fazendo com que um enzima metilante específico trabalhe mais rápido sem perturbar seus parentes. Isso demonstra que mesmo proteínas adaptadoras altamente conectadas, antes consideradas alvos muito grosseiros, podem ser abordadas ao nível de complexos individuais usando química covalente e profileamento em toda a proteoma. Além de fornecer os primeiros agonistas químicos alostéricos para METTL5—uma enzima cada vez mais ligada ao desenvolvimento cerebral, ao metabolismo e ao câncer—o estudo delineia um roteiro geral para descobrir pequenas moléculas que reconhecem e modulam membros únicos de famílias proteicas lotadas dentro de seu ambiente celular nativo.
Citação: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Palavras-chave: complexos proteicos, sondas químicas, metilação de RNA, modulação alostérica, quimio‑proteômica