Clear Sky Science · ja
Complexoformに制限された共有結合性TRMT112リガンドがMETTL5をアロステリックにアゴナイズする
混み合った細胞内で一つの担い手を狙う
ヒトのあらゆる細胞の内部では、何千もの異なるタンパク質機械が場所を争い、オン/オフを切り替えてエネルギー利用から脳の配線までを制御しています。これらの機械の多くは複数のタンパク質部品がさまざまな組み合わせで結合して構成され、類似した複合体のファミリーを生み出します。本稿は、化学者がそのような複合体のうち特定のバージョンだけに結びつく小分子を作り出し、それによって複合体を停止させるのではなくむしろ機能を高めることができることを示します。研究はリボソームが遺伝情報を読み取る仕方を微調整するタンパク質のペアに焦点を当て、タンパク質合成を高精度で調節する新たな手法を提示します。
タンパク質の組み合わせが重要な理由
私たちの約2万個の遺伝子は、2万をはるかに超える多様なタンパク質実体を生みます。RNAのスプライシング、化学的修飾、そして多タンパク質機械への組み立てを経て、各遺伝子は多数の「プロテオフォーム」を生み出す可能性があります。その重要なカテゴリの一つが「complexoform」です――関連するが異なる複合体を形成するタンパク質の様々な組み合わせです。小さなアダプタータンパク質TRMT112はその顕著な例です。TRMT112はハブとして働き、RNA、DNA、あるいはタンパク質に小さな化学タグを付ける複数のメチルトランスフェラーゼ酵素と結合します。TRMT112は多くの酵素とパートナーを組むため、遺伝学的に、あるいは強力な薬剤でそれをオフにすれば複数の経路が同時に乱れます。著者らは代わりに問いを立てました:TRMT112の一つのパートナーにだけ結合し、その一つの酵素の挙動だけを変える化合物を見つけられるだろうか?
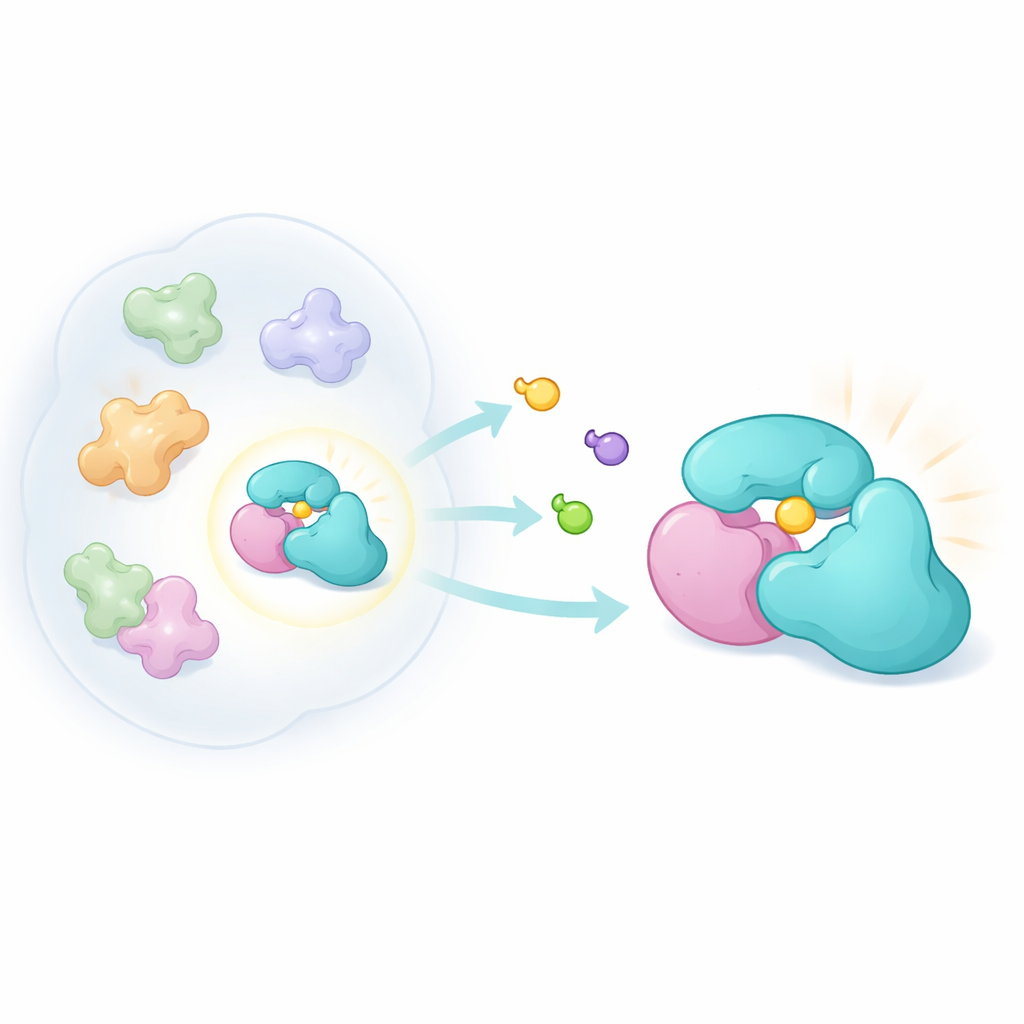
微妙な化学プローブの設計
この着想を探るため、研究者たちは二環性ピロリジン化アクリラミドと呼ばれる新しい小型の立体的分子群を構築しました。これらの化合物はシステインと共有結合的に反応するよう設計されており、システインはしばしばタンパク質の反応性ポケットに位置します。アクティビティベースドプロテインプロファイリングとして知られるケモプロテオミクス法を用い、生きた癌細胞にこれらの化合物の鏡像対を暴露し、どのタンパク質が標識されたかを質量分析で検出しました。鏡像体ごとの結合強度を比較することで、形状依存性の高い相互作用を見分けられます。以前のプローブ群より一般的な反応性は低いにもかかわらず、新しい化合物はTRMT112を含む独自のタンパク質セットに働きかけました。
一つの好まれるパートナーを見つける
より詳しい解析は奇妙な不一致を明らかにしました。全タンパク質を監視するアッセイの一つは、これらのプローブが標準的な標識試薬によるTRMT112の標識をほとんど完全に阻害することを示唆しました。しかし、個々のシステイン部位を直接見る二つ目のアッセイでは、TRMT112の特定の一つのシステインに対してのみ穏やかな影響しか示しませんでした。これは化合物が全TRMT112分子のごく一部、すなわち特定のパートナーに結合しているTRMT112のサブフラクションのみを識別していることを示唆しました。細胞抽出物をサイズで分離し、既知の異なるTRMT112パートナーを共発現させることで、プローブ結合はTRMT112がMETTL5という酵素とペアを組んでいる場合にのみ現れることが示されました。METTL5は小型リボソームRNAの特定のアデニンを修飾します。METTL5をノックアウトすると相互作用は消え、細胞株間でMETTL5の量を変えるとTRMT112の関与量が変化し、プローブがTRMT112:METTL5 complexoformを認識することが確かめられました。
分子インターフェースの可視化と調整
このパートナー関係を特定したうえで、著者らは分子をさらに改良してより強く選択的に結合するようにしました。最適化された化合物FWG‑33Bは、METTL5との界面に位置するTRMT112上の単一のシステインと反応しました。複合体のX線結晶構造は、FWG‑33Bが両タンパク質によって共同で形成されるポケットに嵌り込んでいることを示しました。このポケットはMETTL5の触媒部位からは遠いものの、補酵素結合領域近傍の柔軟なループのわずかな再配列を誘導するのに十分近接していました。この複合ポケットはTRMT112が他の酵素と形成する類似複合体には存在しません。合成RNA断片を用いた生化学的アッセイは機能的帰結を示しました:FWG‑33Bが共有結合した後、METTL5はそのRNA基質に対してより容易に結合し、メチル化効率は約2倍に上昇しました。一方、標的としたシステインを除去する対照変異はこの増強を失わせました。
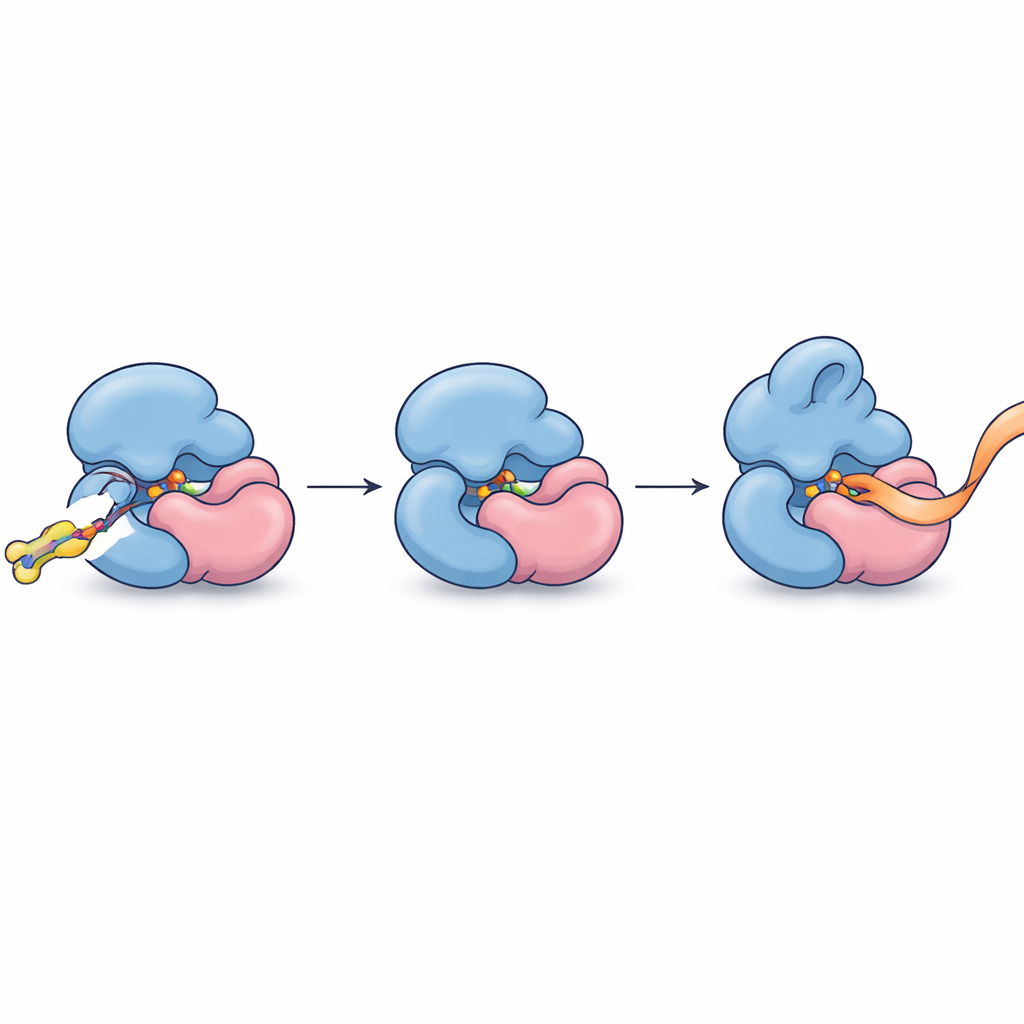
精密な結合を精密な制御へ
日常語で言えば、研究者らは二つのタンパク質部品の継ぎ目に小さな分子のくさびを差し込み、RNAへの結びつきをわずかに締めて形を変えることで、一つの特定のメチル化酵素をその類縁を乱すことなくより速く働かせる方法を見つけたことになります。これは、かつては標的にするには粗すぎると考えられていた高結合性のアダプタータンパク質であっても、共有結合化学とプロテオーム規模のプロファイリングを用いれば個々の複合体レベルで扱えることを示しています。METTL5に対する最初のアロステリック化学的アゴニストを提供したことに加え(METTL5は脳発達、代謝、がんにますます関連づけられている)、本研究はネイティブな細胞環境内で混み合ったタンパク質ファミリーの単一メンバーを認識し調節する小分子を発見するための一般的な設計図を示しています。
引用: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
キーワード: タンパク質複合体, 化学プローブ, RNAメチル化, アロステリック調節, ケモプロテオミクス