Clear Sky Science · sv
Complexoform‑begränsade kovalenta TRMT112‑ligander som allosteriskt agoniserar METTL5
Att rikta in sig på en aktör i en trång cell
Inne i varje mänsklig cell trängs tusentals olika proteinmaskiner, som slås på och av för att styra allt från energianvändning till hjärnans kopplingar. Många av dessa maskiner är uppbyggda av flera protein‑delar som kan sättas ihop i olika kombinationer och bilda familjer av snarlika komplex. Denna artikel visar hur kemister kan konstruera små molekyler som hakar fast vid just en specifik version av ett sådant komplex och, istället för att stänga ner det, faktiskt få det att arbeta hårdare. Arbetet fokuserar på ett proteinpar som hjälper till att finjustera hur ribosomerna läser genetisk information och erbjuder ett nytt sätt att reglera proteinproduktion med hög precision.
Varför mix‑and‑match av proteiner spelar roll
Våra ungefär 20 000 gener ger upphov till långt fler än 20 000 distinkta proteinformer. Efter RNA‑splejsning, kemiska modifieringar och montering till multiproteinmaskiner kan varje gen ge upphov till många "proteoformer." En viktig kategori är "complexoformer"—olika kombinationer av proteiner som bildar besläktade men skilda komplex. Ett litet adaptorprotein kallat TRMT112 är ett tydligt exempel. Det fungerar som en navpunkt och binder flera olika metylerande enzymer som fäster pyttesmå kemiska märkningar på RNA, DNA eller proteiner. Eftersom TRMT112 samarbetar med många enzymer skulle ett genetiskt borttagande eller ett ospecifikt läkemedel störa flera vägar samtidigt. Författarna ställde istället frågan: kan vi hitta en förening som endast binder ett enda TRMT112‑partnerskap och ändrar beteendet hos just det enzymet?
Design av subtila kemiska sonder
För att undersöka idén byggde forskarna en ny familj av kompakta, tredimensionella molekyler kallade bicyclopyrrolidin‑acrylamider. Dessa föreningar är utformade för att reagera kovalent med cystein, en svavelinnehållande aminosyra som ofta sitter i reaktiva fickor på proteiner. Med en kemoproteomisk metod känd som activity‑based protein profiling exponerade de levande cancerceller för par av spegelbildsversioner av dessa föreningar och använde sedan masspektrometri för att se vilka proteiner som markerades. Genom att jämföra hur starkt varje spegelbild band kunde de upptäcka starkt formberoende interaktioner. Trots att de nya föreningarna var mindre generellt reaktiva än tidigare sondfamiljer träffade de en distinkt uppsättning proteiner, inklusive TRMT112.
Att hitta ett enda favoristhandlag
Närmare analys avslöjade en märklig avvikelse. Ett assay som övervakar hela proteiner antydde att sonderna nästan helt blockerade TRMT112 från att märkas av ett standardmärkande reagens. Ett andra, mer direkt assay som tittar på enskilda cysteinställen visade dock endast en måttlig effekt på en viss cystein i TRMT112. Detta antydde att föreningarna kände igen endast en bråkdel av alla TRMT112‑molekyler—den fraktion som var bunden till en särskild partner. Genom att separera cellextrakt efter storlek och genom att samexprimera olika kända TRMT112‑partners visade teamet att sondbindningen endast uppträdde när TRMT112 var parat med ett enzym, METTL5, som modifierar en specifik adeninbas i cellens lilla ribosomala RNA. Att slå ut METTL5 raderade interaktionen, och variationer i METTL5‑nivåer mellan cellinjer ändrade hur mycket TRMT112 engagerades, vilket bekräftade att sonden känner igen en TRMT112:METTL5‑complexoform.
Se och finjustera det molekylära gränssnittet
När partnerskapet väl identifierats förfinade författarna sina molekyler för att binda tätare och mer selektivt. En optimerad förening, FWG‑33B, reagerade med en enskild cystein på TRMT112 belägen precis vid gränssnittet mot METTL5. Röntgenkristallografi av komplexet visade FWG‑33B kilad i en ficka som bildas gemensamt av båda proteinerna, långt från METTL5:s aktiva säte men tillräckligt nära för att utlösa en subtil omformning av en flexibel slingregion nära enzymets kofaktorbindande område. Denna sammansatta ficka existerar endast i TRMT112:METTL5‑komplexet och inte i liknande komplex som TRMT112 bildar med andra enzymer. Biokemiska analyser med syntetiska RNA‑fragment avslöjade det funktionella utfallet: efter kovalent bindning av FWG‑33B band METTL5 sitt RNA‑substrat lättare och metylerade det ungefär två gånger effektivare, medan en kontrollmutation som avlägsnade den målinriktade cysteinen eliminerade denna förstärkning.
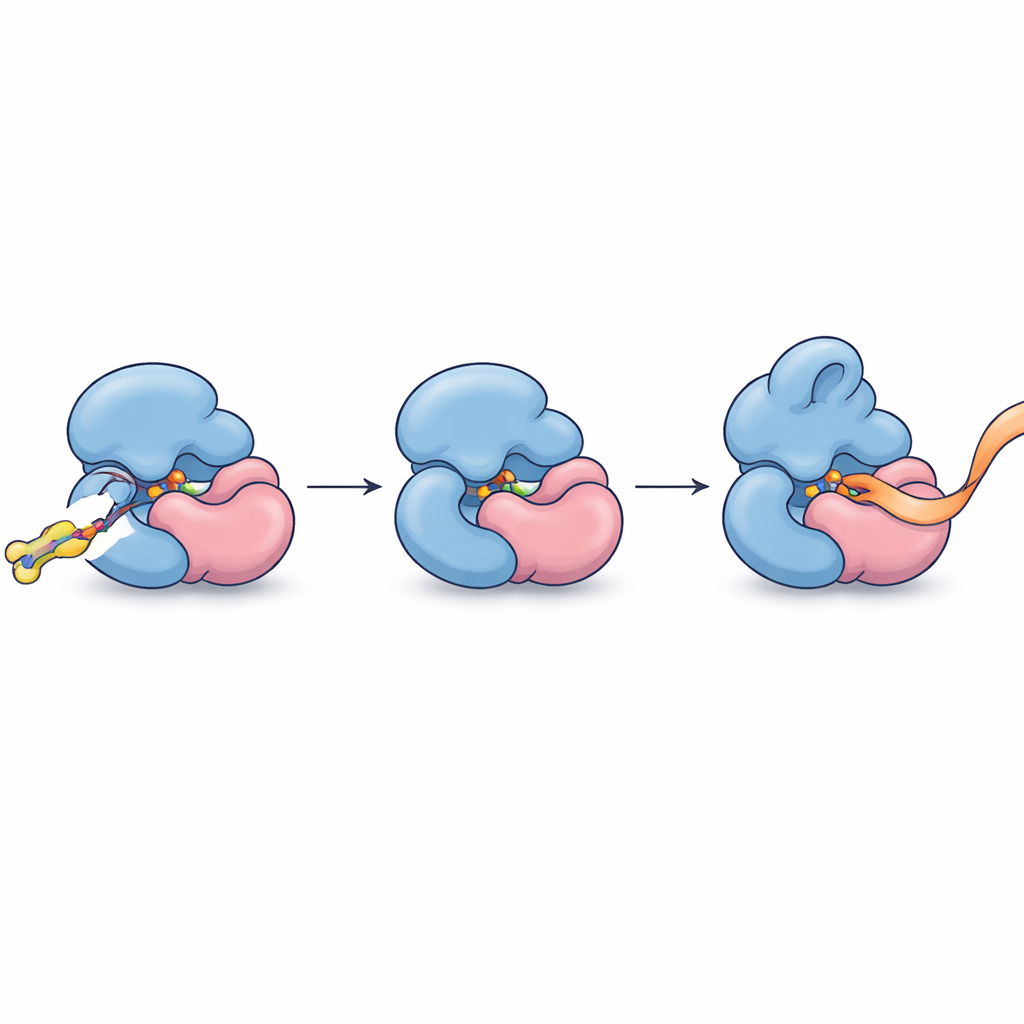
Från precis bindning till precis kontroll
I vardagliga termer har forskarna funnit ett sätt att smyga in en liten molekylär kil i skarven mellan två proteindelar för att subtilt dra ihop och forma om deras bindning till RNA, så att ett specifikt metylerande enzym arbetar snabbare utan att störa sina släktingar. Detta visar att även högt sammankopplade adaptorproteiner, som tidigare ansågs vara för trubbiga som mål, kan riktas på nivån för enskilda komplex med hjälp av kovalent kemi och proteomäckningsprofilering. Utöver att tillhandahålla de första allosteriska kemiska agonisterna för METTL5—ett enzym som i allt högre grad kopplas till hjärnans utveckling, ämnesomsättning och cancer—skisserar studien en generell blåtryck för att upptäcka små molekyler som känner igen och finjusterar enskilda medlemmar i trängda proteinfamiljer inne i deras naturliga cellulära miljö.
Citering: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Nyckelord: proteinkomplex, kemiska sonder, RNA‑metylering, allosterisk modulering, kemoproteomik