Clear Sky Science · ar
رابطات ترافدية تقييدية بواسطة الشكل المعقَّد لـ TRMT112 تُنشط METTL5 بطريقة كلوسترية
استهداف لاعب واحد في خلية مكتظة
داخل كل خلية بشرية، تتزاحم آلاف الآلات البروتينية المختلفة، تعمل وتتعطل للتحكم في كل شيء من استهلاك الطاقة إلى شبكة الدماغ. تُبنى العديد من هذه الآلات من أجزاء بروتينية متعددة تتصل معًا بتراكيب متنوعة، مكونة عائلات من المجمعات المتشابهة. تُظهر هذه الورقة كيف يمكن للكيميائيين تصميم جزيئات صغيرة تلتصق بنسخة محددة واحدة فقط من مثل هذا المجمع وبدلاً من إيقافها، تزيد من نشاطها. يركز العمل على زوج بروتيني يساعد في ضبط كيفية قراءة الريبوسومات للمعلومة الجينية، مقدمًا وسيلة جديدة للتحكم الدقيق في إنتاج البروتين.
لماذا يهم التوليف البروتيني المتنوع
تنتج نحو 20,000 جينات لدينا كائنات بروتينية أكثر بكثير من 20,000 نوع مميز. بعد قص الرنا، والتعديلات الكيميائية، والتجميع في آلات متعددة البروتينات، يمكن لكل جين أن يولد العديد من «أشكال البروتين» أو proteoforms. فئة مهمة من هذه هي «شكل-المجمع» (complexoforms)—تكوينات مختلفة من البروتينات التي تُكوّن مجمعات مرتبطة لكنها مميزة. مثال بارز هو بروتين مرافق صغير يُدعى TRMT112. يعمل كمحور، رابطًا لعدة إنزيمات ميثيلترانسفيراز تضع علامات كيميائية صغيرة على الرنا أو الدنا أو البروتينات. وبما أن TRMT112 يتشارك مع عدة إنزيمات، فإن تعطيله وراثيًا أو بواسطة دواء غير مفرِق سيشوِّش مسارات متعددة في آن واحد. طرح المؤلفون سؤالًا مختلفًا: هل يمكن إيجاد مركب يرتبط بشراكة TRMT112 واحدة فقط ويغير سلوك ذلك الإنزيم بالذات؟
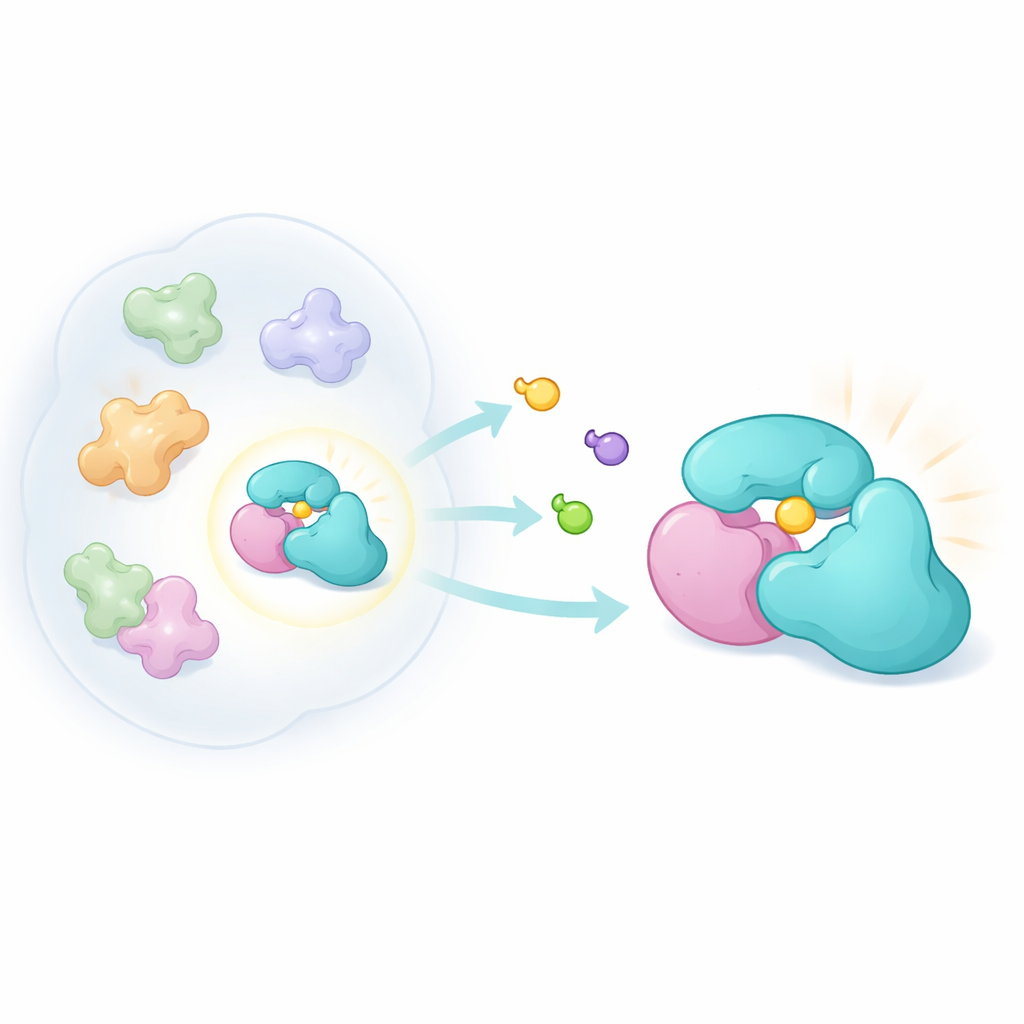
تصميم مسبارات كيميائية دقيقة
لاستكشاف هذه الفكرة، بنى الباحثون عائلة جديدة من الجزيئات المدمجة ثلاثية الأبعاد تسمى أكرلاميدات البيسكلوبيروليدين. صممت هذه المركبات لتتفاعل تساهميًا مع السيستئين، حمض أميني يحتوي على الكبريت يتواجد غالبًا في جيوب تفاعلية على البروتينات. باستخدام طريقة كيموبروتيومية تُعرف بتوصيف البروتين النشط، عرّضوا خلايا سرطانية حية لأزواج من النسخ المرآتية لهذه المركبات ثم استخدموا مطيافية الكتلة لمعرفة أي البروتينات وُسمت. بمقارنة مدى ارتباط كل صورة مرآتية، استطاعوا رصد تفاعلات حساسة للشكل ثلاثي الأبعاد. ورغم أن هذه المركبات أقل تفاعلية عمومًا من عائلات مسبارات سابقة، أصابت مجموعة مميزة من البروتينات، بينها TRMT112.
اكتشاف شراكة مفضلة واحدة
كشف تحليل أدق عن تناقض غريب. أحد الاختبارات التي تراقب البروتينات كاملة أشار إلى أن المسبارات منعت تقريبًا وسم TRMT112 بواسطة عامل وسم معياري. ومع ذلك، أظهر اختبار ثانٍ أكثر مباشرة ينظر إلى مواقع السيستئين الفردية تأثيرًا متواضعًا على سيستئين واحد معيّن في TRMT112. ألمح هذا إلى أن المركبات كانت تتعرف على جزء فقط من جزيئات TRMT112—الجزء المرتبط بشريك معين. عن طريق فصل مستخلصات الخلايا حسب الحجم ومن خلال التعبير المشترك عن شركاء معروفين لـ TRMT112، أظهر الفريق أن ارتباط المسبار ظهر فقط عندما كان TRMT112 مرتبطًا بإنزيم واحد، METTL5، الذي يعدل قاعدة أدينين محددة في رنا الريبوسوم الصغير. إلغاء METTL5 أزال التفاعل، وتغيير مستويات METTL5 عبر خطوط خلوية غيّر كمية ارتباط TRMT112، مؤكّدًا أن المسبار يتعرف على شكل-مجمع TRMT112:METTL5.
رؤية وضبط الواجهة الجزئية الجزيئية
بعد تحديد هذه الشراكة، قام المؤلفون بتحسين مركباتهم لتربط بقوة وانتقائية أكبر. تفاعل مركب محسن، FWG-33B، مع سيستئين واحد على TRMT112 يقع تمامًا عند الواجهة مع METTL5. أظهرت البلورة بالأشعة السينية للمجمع أن FWG-33B محشور داخل جيب يتكوّن مشتركًا بواسطة كلا البروتينين، بعيدًا عن موقع نشاط METTL5 لكن قريبًا بما يكفي لإحداث إعادة تشكيل طفيفة لحلقة مرنة بالقرب من منطقة ربط العامل المشارك للإنزيم. هذا الجيب المركب يوجد فقط في مجمع TRMT112:METTL5 وليس في المجمعات المشابهة التي يشكلها TRMT112 مع إنزيمات أخرى. كشفت تجارب بيوكيميائية باستخدام شظايا رنا صناعية النتيجة الوظيفية: بعد الارتباط التساهمي لـ FWG-33B، ارتبط METTL5 بمستقبله الرنوي بسهولة أكبر وميثلَه بكفاءة تقارب الضعف، بينما أدت طفرة تحكم أزالت السيستئين المستهدف إلى إلغاء هذا التعزيز.
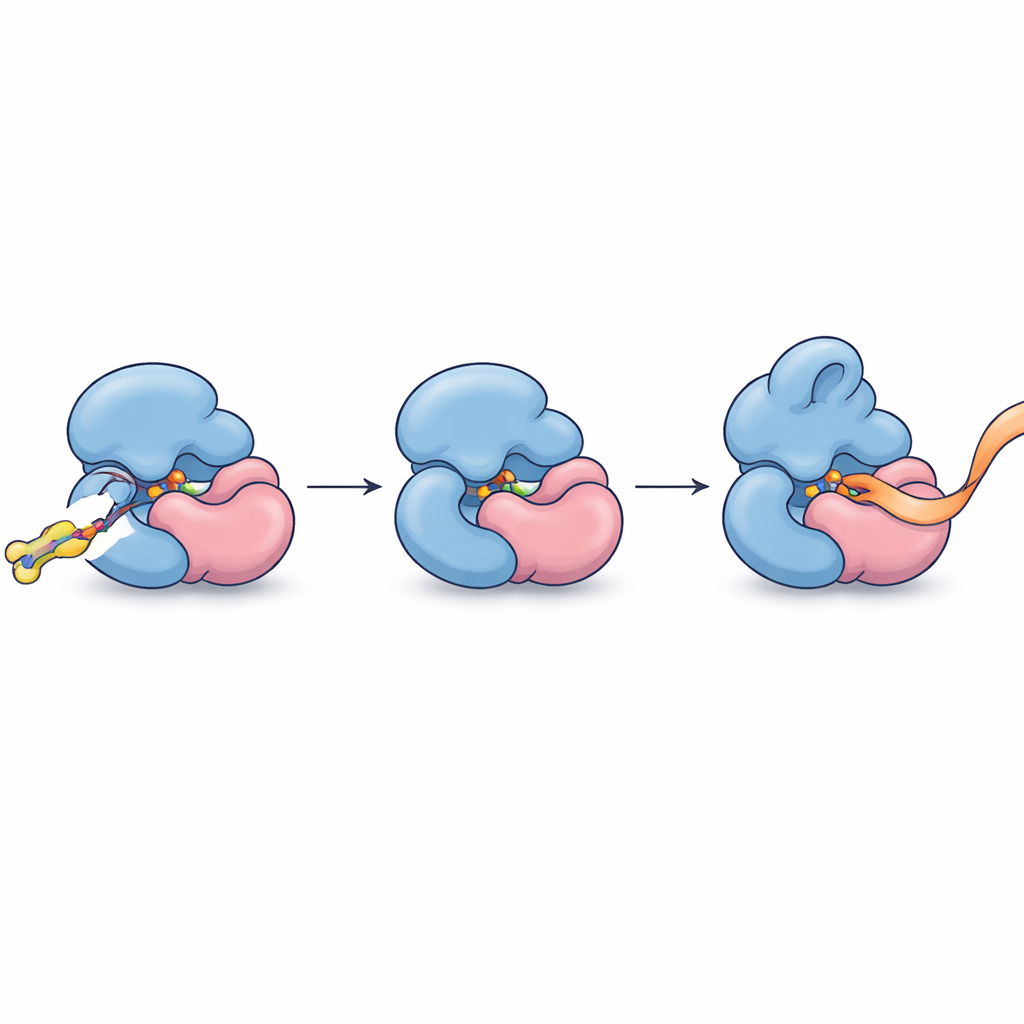
تحويل الارتباط الدقيق إلى تحكم دقيق
بعبارات بسيطة، وجد الباحثون طريقة ليدخلوا إسفينًا جزيئيًا صغيرًا في الوصلة بين جزأين بروتينيين ليشددوا ويعيدوا تشكيل قبضتهما على الرنا بشكل دقيق، مما يجعل إنزيم ميثيل واحدًا معينًا يعمل بسرعة أكبر دون إزعاج نظرائه. يبيّن هذا أنه حتى البروتينات المرافقة متصلة بشدة، والتي اعتُبرت سابقًا أهدافًا فظة، يمكن معالجتها على مستوى المجمعات الفردية باستخدام الكيمياء التساهمية وتوصيف البروتيوم ككل. بالإضافة إلى تقديم أول ناهضات كيميائية كلوسترية لـ METTL5—الذي يرتبط بشكل متزايد بتطور الدماغ، والأيض، والسرطان—تحدد الدراسة مخططًا عامًا لاكتشاف جزيئات صغيرة تتعرف على عضو واحد وتضبطه داخل عائلات البروتين المكتظة في بيئتها الخلوية الأصلية.
الاستشهاد: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
الكلمات المفتاحية: مجموعات البروتين, مسبارات كيميائية, مثيلة الرنا, تعديل كلوسترى, كيموبروتيوميكس