Clear Sky Science · it
Ligandi covalenti di TRMT112 limitati a complexoform che agonizzano allostericamente METTL5
Mirare a un protagonista in una cellula affollata
All'interno di ogni cellula umana, migliaia di diverse macchine proteiche si affollano, attivandosi e disattivandosi per controllare tutto, dall'uso dell'energia all'organizzazione del cervello. Molte di queste macchine sono costruite da più subunità proteiche che si assemblano in combinazioni diverse, creando famiglie di complessi simili nell'aspetto. Questo articolo mostra come i chimici possono progettare piccole molecole che si attaccano a una sola versione specifica di tali complessi e, invece di disattivarla, ne incrementano l'attività. Il lavoro si concentra su una coppia proteica che aiuta a regolare come i ribosomi leggono l'informazione genetica, offrendo un nuovo modo per modulare con precisione la produzione proteica.
Perché la combinatoria proteica è importante
I nostri circa 20.000 geni danno origine a molto più di 20.000 entità proteiche distinte. Dopo lo splicing dell'RNA, modificazioni chimiche e l'assemblaggio in macchine multi‑proteiche, ogni gene può generare molte «proteoforme». Una categoria importante è quella dei «complexoform»—diverse combinazioni di proteine che formano complessi correlati ma distinti. Una piccola proteina adattatrice chiamata TRMT112 è un esempio significativo. Funziona come un hub, legando diverse metiltransferasi che aggiungono piccole marche chimiche su RNA, DNA o proteine. Poiché TRMT112 si associa a molti enzimi, inattivarlo geneticamente o con un farmaco non selettivo sconvolgerebbe molte vie contemporaneamente. Gli autori si sono invece chiesti: è possibile trovare un composto che si leghi solo a una singola associazione di TRMT112 e modifichi il comportamento di quel solo enzima?
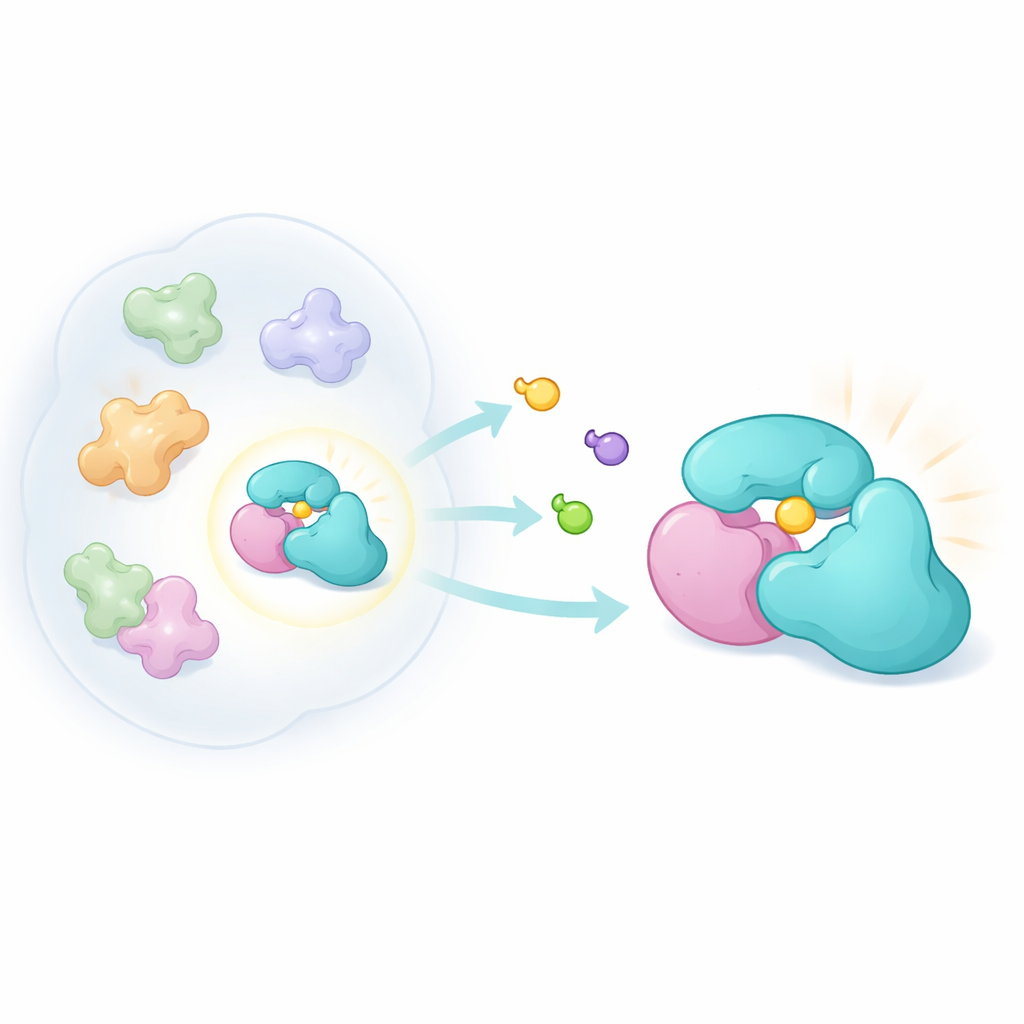
Progettare sonde chimiche sottili
Per esplorare questa idea, i ricercatori hanno costruito una nuova famiglia di molecole compatte e tridimensionali chiamate bicicclopirrolidine acrilammidi. Questi composti sono progettati per reagire covalentemente con la cisteina, un amminoacido contenente zolfo che spesso si trova in tasche reattive sulle proteine. Utilizzando un metodo chemioproteomico noto come activity‑based protein profiling, hanno esposto cellule tumorali vive a coppie di versioni speculari di questi composti e poi hanno usato la spettrometria di massa per vedere quali proteine venivano marcate. Confrontando quanto fortemente ogni immagine speculare si legava, hanno potuto identificare interazioni altamente dipendenti dalla forma. Pur essendo meno generalmente reattivi rispetto a famiglie di sonde precedenti, i nuovi composti hanno colpito un insieme distinto di proteine, inclusa TRMT112.
Trovare una singola partnership favorita
Un'analisi più approfondita ha rivelato una discrepanza curiosa. Un saggio che osserva le proteine intere suggeriva che le sonde bloccassero quasi completamente la marcatura di TRMT112 da parte di un reagente standard. Tuttavia un secondo saggio, più diretto, che esamina singoli siti di cisteina mostrava solo un effetto modesto su una particolare cisteina in TRMT112. Questo indicava che i composti riconoscevano solo una frazione di tutte le molecole di TRMT112—la frazione legata a un partner specifico. Separando gli estratti cellulari per dimensione e co‑esprimendo diversi partner noti di TRMT112, il gruppo ha dimostrato che il legame della sonda si osservava solo quando TRMT112 era associata a un enzima, METTL5, che modifica una specifica adenina nell'rRNA ribosomiale piccolo della cellula. L'eliminazione di METTL5 annullava l'interazione, e variare i livelli di METTL5 tra linee cellulari cambiava quanto TRMT112 fosse coinvolta, confermando che la sonda riconosce un complexoform TRMT112:METTL5.
Osservare e modulare l'interfaccia molecolare
Avendo identificato questa associazione, gli autori hanno raffinato le loro molecole per legarsi con maggiore affinità e selettività. Un composto ottimizzato, FWG‑33B, reagiva con una singola cisteina su TRMT112 situata proprio all'interfaccia con METTL5. La cristallografia a raggi X del complesso ha mostrato FWG‑33B incuneato in una tasca formata congiuntamente da entrambe le proteine, lontano dal sito attivo di METTL5 ma sufficientemente vicino da indurre un lieve riposizionamento di un anello flessibile vicino alla regione di legame del cofattore dell'enzima. Questa tasca composita esiste solo nel complesso TRMT112:METTL5 e non in complessi simili che TRMT112 forma con altri enzimi. Saggi biochimici con frammenti di RNA sintetico hanno rivelato l'esito funzionale: dopo il legame covalente di FWG‑33B, METTL5 si legava al suo substrato RNA più facilmente e lo metilava circa il doppio, mentre una mutazione di controllo che rimuoveva la cisteina bersaglio aboliva questo aumento.
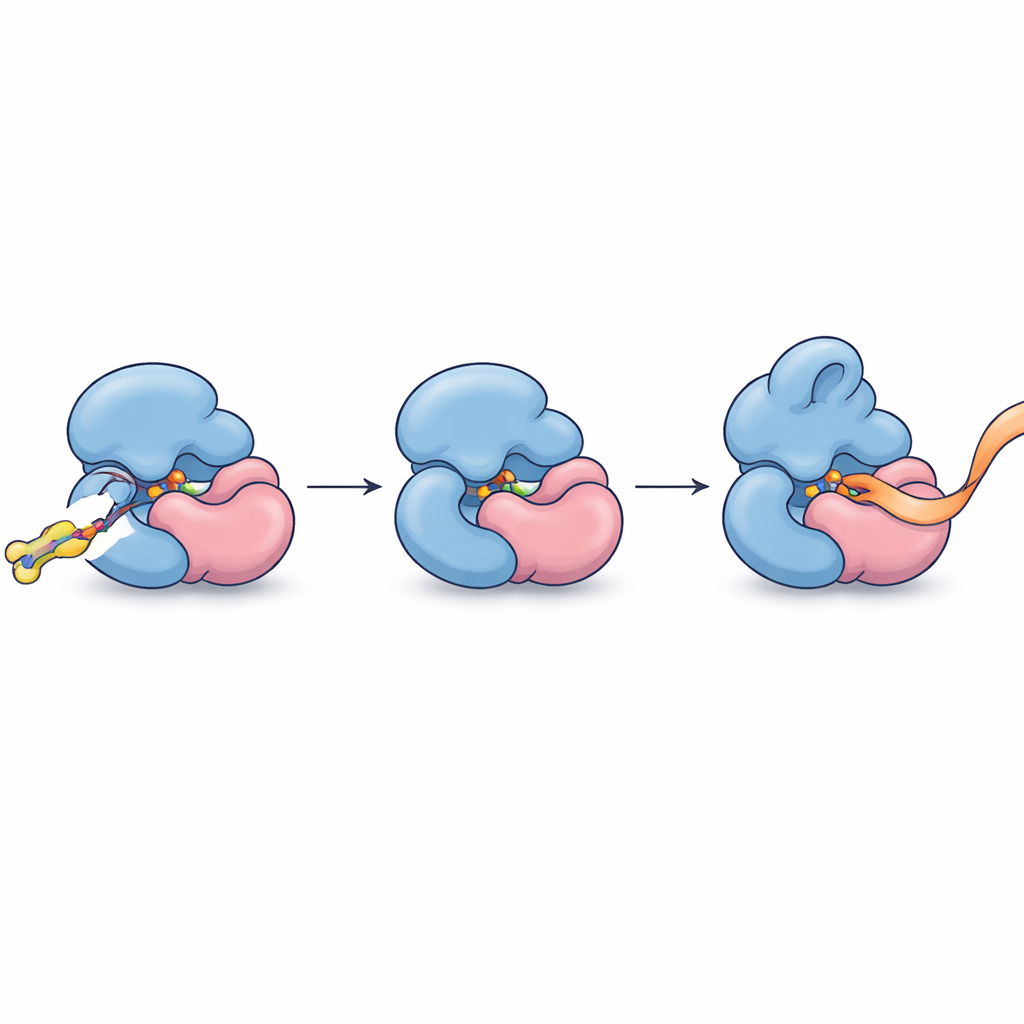
Trasformare il legame preciso in controllo preciso
In termini pratici, i ricercatori hanno trovato un modo per infilare una piccola cuneo molecolare nella giuntura tra due parti proteiche al fine di stringere e rimodellare sottilmente la loro presa sull'RNA, facendo lavorare più velocemente un enzima metilante specifico senza disturbare i suoi «cugini». Questo dimostra che anche proteine adattatrici altamente connesse, ritenute fino a ieri bersagli troppo grezzi, possono essere affrontate a livello di singoli complessi usando chimica covalente e profilazione a livello di proteoma. Oltre a fornire i primi agonisti chimici allosterici per METTL5—un enzima sempre più collegato allo sviluppo cerebrale, al metabolismo e al cancro—lo studio delinea una strategia generale per scoprire piccole molecole che riconoscono e modulano membri singoli di famiglie proteiche affollate nel loro ambiente cellulare nativo.
Citazione: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Parole chiave: complessi proteici, sonde chimiche, metilazione dell'RNA, modulazione allosterica, chemioproteomica