Clear Sky Science · de
Komplexoform‑beschränkte kovalente TRMT112‑Liganden, die METTL5 allosterisch agonisieren
Einen Spieler in einer überfüllten Zelle anvisieren
In jeder menschlichen Zelle drängen Tausende unterschiedlicher Proteinmaschinen um Raum, schalten sich ein und aus und steuern alles von Energiehaushalt bis zur Verschaltung des Gehirns. Viele dieser Maschinen bestehen aus mehreren Proteinbausteinen, die sich in verschiedenen Kombinationen zusammenfügen und Familien ähnlich aussehender Komplexe bilden. Diese Arbeit zeigt, wie Chemiker kleine Moleküle entwickeln können, die sich gezielt an genau eine spezifische Variante eines solchen Komplexes anheften und diesen nicht abschalten, sondern tatsächlich stärker arbeiten lassen. Der Fokus liegt auf einem Proteinduo, das beeinflusst, wie Ribosomen genetische Information lesen, und bietet einen neuen Weg, die Proteinproduktion mit hoher Präzision zu regulieren.
Warum Mix‑and‑Match bei Proteinen wichtig ist
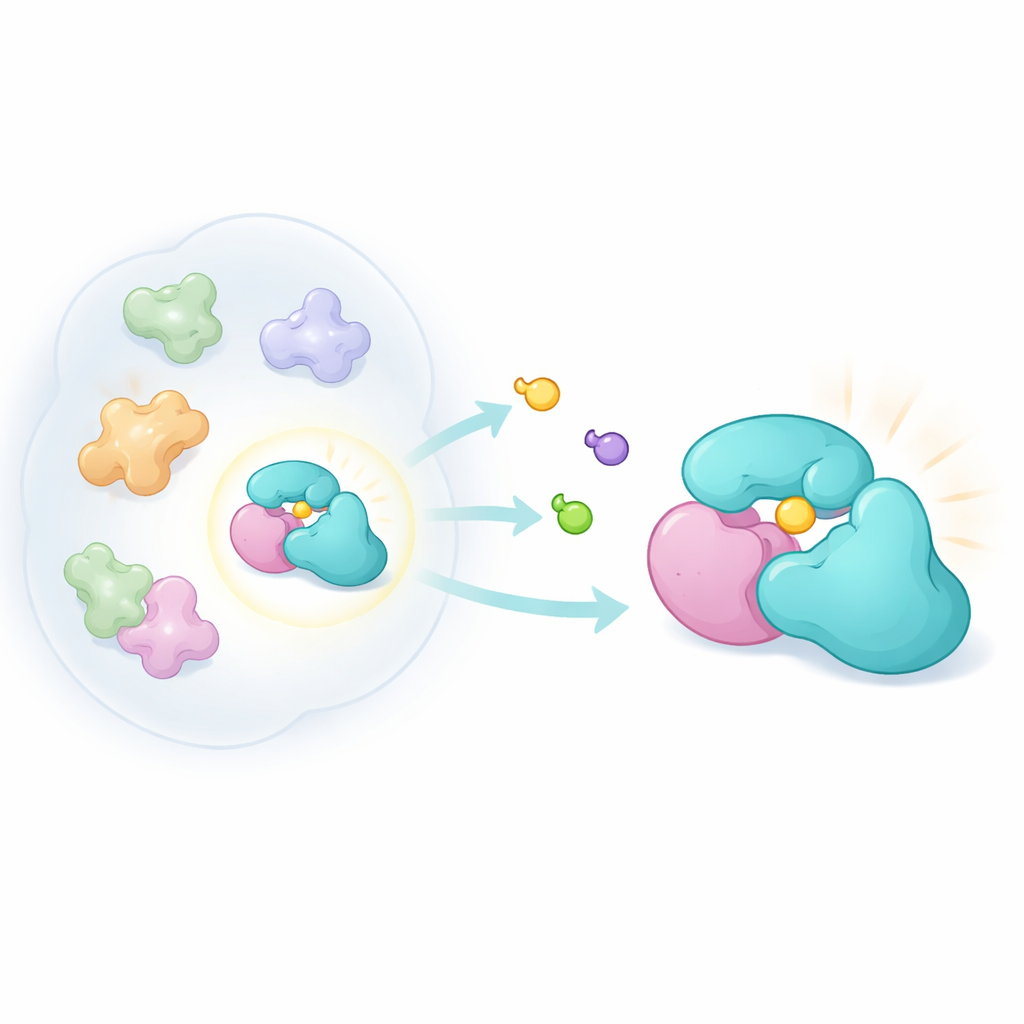
Unsere rund 20.000 Gene erzeugen weit mehr als 20.000 verschiedene Proteinentitäten. Nach RNA‑Spleißen, chemischen Modifikationen und dem Zusammenbau zu Mehrproteinmachinen kann jedes Gen viele „Proteoforme“ hervorbringen. Eine wichtige Kategorie sind „Komplexoforme“—unterschiedliche Kombinationen von Proteinen, die verwandte, aber unterscheidbare Komplexe bilden. Ein kleines Adapterprotein namens TRMT112 ist ein eindrückliches Beispiel: Es funktioniert als Knotenpunkt und bindet mehrere verschiedene Methyltransferasen, die winzige chemische Markierungen an RNA, DNA oder Proteinen anbringen. Da TRMT112 mit vielen Enzymen zusammenarbeitet, würde sein genetisches Ausschalten oder die Behandlung mit einem unspezifischen Wirkstoff mehrere Signalwege gleichzeitig durcheinanderbringen. Die Autoren fragten stattdessen: Kann man eine Verbindung finden, die nur an eine einzelne TRMT112‑Partnerschaft bindet und damit nur das Verhalten genau dieses einen Enzyms verändert?
Entwurf subtiler chemischer Sonden
Um diese Idee zu untersuchen, entwickelten die Forscher eine neue Familie kompakter, dreidimensionaler Moleküle, genannt bicyclopyrrolidin‑Acrylamide. Diese Verbindungen sind so gestaltet, dass sie kovalent mit Cystein reagieren, einer schwefelhaltigen Aminosäure, die häufig in reaktiven Taschen von Proteinen sitzt. Mittels einer chemoproteomischen Methode, bekannt als activity‑based protein profiling, setzten sie lebende Krebszellen Paaren von Spiegelbildversionen dieser Verbindungen aus und analysierten anschließend mittels Massenspektrometrie, welche Proteine markiert wurden. Durch den Vergleich, wie stark jedes Spiegelbild gebunden wurde, konnten sie hoch form‑abhängige Interaktionen aufspüren. Obwohl die neuen Verbindungen weniger allgemein reaktiv waren als frühere Sondenfamilien, trafen sie auf eine charakteristische Proteinauswahl, darunter TRMT112.
Eine einzelne bevorzugte Partnerschaft finden
Genauere Analysen offenbarten eine merkwürdige Diskrepanz. Ein Test, der ganze Proteine beobachtet, deutete darauf hin, dass die Sonden TRMT112 nahezu vollständig daran hinderten, mit einem Standard‑Markierungsreagenz versehen zu werden. Ein zweiter, direkterer Assay, der einzelne Cysteinstellen betrachtete, zeigte jedoch nur einen moderaten Effekt an einem bestimmten Cystein in TRMT112. Das ließ vermuten, dass die Verbindungen nur einen Bruchteil aller TRMT112‑Moleküle erkannten—nämlich jene, die an einen bestimmten Partner gebunden waren. Durch Fraktionierung von Zellextrakten nach Größe und durch koexpressive Experimente mit verschiedenen bekannten TRMT112‑Partnern zeigte das Team, dass die Sonde nur dann bindete, wenn TRMT112 mit einem Enzym namens METTL5 gepaart war, das eine bestimmte Adeninbase in der kleinen ribosomalen RNA der Zelle modifiziert. Das Entfernen von METTL5 beseitigte die Interaktion, und das Variieren der METTL5‑Spiegel in verschiedenen Zelllinien veränderte den Anteil der gebundenen TRMT112‑Moleküle, was bestätigte, dass die Sonde ein TRMT112:METTL5‑Komplexoform erkennt.
Die molekulare Schnittstelle sehen und feinjustieren
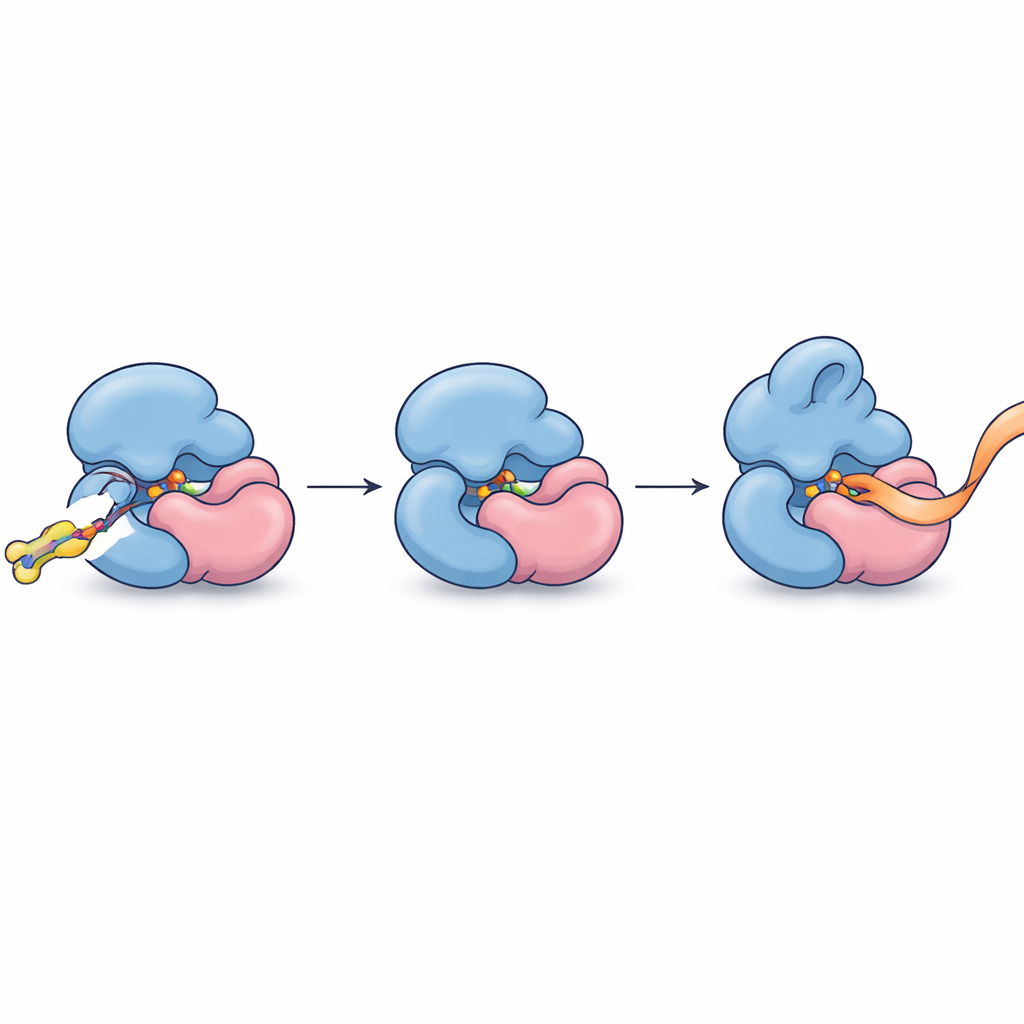
Nachdem diese Partnerschaft genau bestimmt war, verfeinerten die Autoren ihre Moleküle, um stärker und selektiver zu binden. Eine optimierte Verbindung, FWG‑33B, reagierte mit einem einzelnen Cystein auf TRMT112, das direkt an der Schnittstelle zu METTL5 liegt. Röntgenkristallographie des Komplexes zeigte FWG‑33B in einer Tasche, die gemeinsam von beiden Proteinen gebildet wird—weit entfernt von METTL5s aktiver Stelle, aber nah genug, um eine subtile Umformung einer flexiblen Schleife in der Nähe der Cofaktorbindungsregion des Enzyms auszulösen. Diese zusammengesetzte Tasche existiert nur im TRMT112:METTL5‑Komplex und nicht in ähnlichen Komplexen, die TRMT112 mit anderen Enzymen bildet. Biochemische Assays mit synthetischen RNA‑Fragmenten zeigten das funktionelle Ergebnis: Nach kovalenter Bindung von FWG‑33B setzte METTL5 sein RNA‑Substrat leichter frei und methylierte es etwa doppelt so effizient, während eine Kontrollmutation, die das angesprochene Cystein entfernte, diesen Effekt aufhob.
Präzise Bindung in präzise Kontrolle verwandeln
Alltagssprachlich gesprochen haben die Forscher eine Methode gefunden, einen winzigen molekularen Keil in die Naht zwischen zwei Proteinteilen zu schieben, um deren Griff an der RNA leicht zu straffen und umzuformen, sodass ein spezifisches Methylierungsenzym schneller arbeitet, ohne seine Verwandten zu stören. Dies zeigt, dass selbst hochvernetzte Adapterproteine, die früher als zu grobe Ziele galten, auf Ebene einzelner Komplexe mithilfe kovalenter Chemie und proteomweiter Profilierung adressierbar sind. Neben der Bereitstellung der ersten allosterischen chemischen Agonisten für METTL5—ein Enzym, das zunehmend mit Gehirnentwicklung, Stoffwechsel und Krebs in Verbindung gebracht wird—zeichnet die Studie eine allgemeine Blaupause dafür, wie kleine Moleküle entdeckt werden können, die einzelne Mitglieder überfüllter Proteinfamilien in ihrer nativen zellulären Umgebung erkennen und feinjustieren.
Zitation: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Schlüsselwörter: Proteinkomplexe, chemische Sonden, RNA‑Methylierung, allosterische Modulation, Chemoproteomik