Clear Sky Science · nl
Complexoform-beperkte covalente TRMT112-liganden die METTL5 allosterisch agoniseren
Een speler richten in een drukke cel
In elke menselijke cel schommelen duizenden verschillende eiwitmachines om ruimte, die aan- en uitgaan om alles te regelen, van energieverbruik tot hersenbedrading. Veel van deze machines bestaan uit meerdere eiwitonderdelen die in verschillende combinaties in elkaar klikken, waardoor families van op elkaar lijkende complexen ontstaan. Dit artikel toont hoe chemici kleine moleculen kunnen ontwerpen die precies op één specifieke versie van zo’n complex inhaken en, in plaats van het uit te schakelen, het juist harder laten werken. Het werk richt zich op een eiwitpaar dat helpt bij het afstemmen van hoe ribosomen genetische informatie lezen, en biedt een nieuwe manier om eiwitproductie met grote precisie bij te sturen.
Waarom mix‑en‑match van eiwitten ertoe doet
Onze ongeveer 20.000 genen geven aanleiding tot veel meer dan 20.000 verschillende eiwitentiteiten. Na RNA-splijting, chemische modificaties en assemblage in multi-eiwitmachines kan elk gen vele “proteovormen” voortbrengen. Een belangrijke categorie is “complexoformen”—verschillende combinaties van eiwitten die verwante maar onderscheidende complexen vormen. Een klein adaptor-eiwit genaamd TRMT112 is een sprekend voorbeeld. Het fungeert als een knooppunt en bindt verschillende methyltransferase-enzymen die kleine chemische labels aan RNA, DNA of eiwitten zetten. Omdat TRMT112 met veel enzymen samenwerkt, zou het genetisch uitschakelen of het gebruik van een bot middel meerdere paden tegelijk in de war sturen. De auteurs stelden in plaats daarvan de vraag: kunnen we een verbinding vinden die slechts één TRMT112‑partnerschap bindt en alleen het gedrag van dat ene enzym verandert?
Subtiele chemische probes ontwerpen
Om dit idee te verkennen, bouwden de onderzoekers een nieuwe familie compacte, driedimensionale moleculen genaamd bicyclopyrrolidine-acrylamiden. Deze verbindingen zijn ontworpen om covalent te reageren met cysteïne, een zwavelhoudend aminozuur dat vaak in reactieve pockets van eiwitten zit. Met een chemoproteomische methode bekend als activity-based protein profiling stelden ze levende kankercellen bloot aan paren van spiegelbeeldversies van deze verbindingen en gebruikten daarna massaspectrometrie om te zien welke eiwitten getagd waren. Door te vergelijken hoe sterk elk spiegelbeeld bonden, konden ze sterk vormafhankelijke interacties opsporen. Hoewel de nieuwe verbindingen minder algemeen reactief waren dan eerdere probe-families, raakten ze een onderscheidende set eiwitten, waaronder TRMT112.
Een enkele favoriete partnerschap ontdekken
Nadere analyse onthulde een opmerkelijke mismatch. Een assay die hele eiwitten in de gaten houdt suggereerde dat de probes bijna volledig voorkwamen dat TRMT112 door een standaard tagreagens werd gemarkeerd. Een tweede, directere assay die naar individuele cysteïneplaatsen keek, toonde echter slechts een bescheiden effect op één specifieke cysteïne in TRMT112. Dit wees erop dat de verbindingen slechts een fractie van alle TRMT112-moleculen herkenden—namelijk die fractie die aan een bepaalde partner gebonden is. Door celextracten op grootte te scheiden en verschillende bekende TRMT112-partners samen te expresseren, toonde het team aan dat probebinding alleen optrad wanneer TRMT112 gekoppeld was aan één enzym, METTL5, dat een specifieke adenine in het kleine ribosomale RNA van de cel modificeert. Het uitzetten van METTL5 maakte de interactie ongedaan, en variatie in METTL5-niveaus tussen cellijnen veranderde hoeveel TRMT112 betrokken was, wat bevestigt dat de probe een TRMT112:METTL5-complexoform herkent.
Het moleculaire interface zien en bijsturen
Nadat ze dit partnerschap hadden vastgesteld, verfijnden de auteurs hun moleculen om strakker en selectiever te binden. Een geoptimaliseerde verbinding, FWG‑33B, reageerde met een enkele cysteïne op TRMT112 die precies bij het interface met METTL5 ligt. Röntgendiffractie van het complex toonde FWG‑33B geklemd in een pocket die door beide eiwitten gezamenlijk wordt gevormd, ver van het actieve centrum van METTL5 maar dicht genoeg om een subtiele herschikking van een flexibele lus nabij het cofactorbindende gebied van het enzym te veroorzaken. Deze samengestelde pocket bestaat alleen in het TRMT112:METTL5-complex en niet in soortgelijke complexen die TRMT112 met andere enzymen vormt. Biochemische assays met synthetische RNA-fragmenten lieten het functionele gevolg zien: na covalente binding van FWG‑33B bond METTL5 zijn RNA-substraat gemakkelijker en methyleerde het dit ongeveer twee keer efficiënter, terwijl een controlemutatie die de doelcysteïne verwijderde deze versterking uitschakelde.
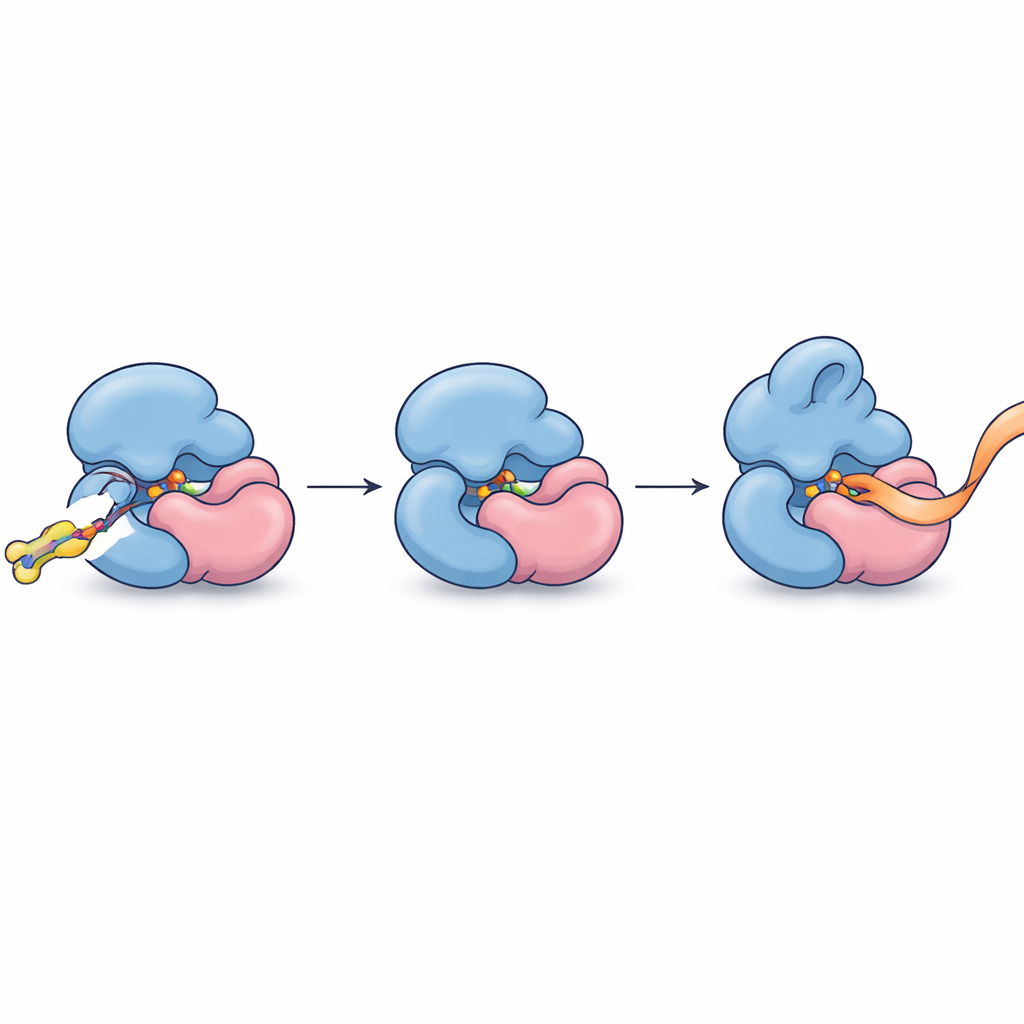
Precisiebinding omzetten in precisiebesturing
In gewone bewoordingen hebben de onderzoekers een manier gevonden om een klein moleculair wigje in de naad tussen twee eiwitdelen te schuiven om hun greep op RNA subtiel aan te spannen en te hervormen, waardoor één specifiek methylerend enzym sneller werkt zonder zijn verwanten te verstoren. Dit toont aan dat zelfs sterk verbonden adaptor-eiwitten, lange tijd gezien als te grove doelen, op het niveau van individuele complexen kunnen worden aangesproken met covalente chemie en proteoom‑brede profilering. Naast het leveren van de eerste allosterische chemische agonisten voor METTL5—een enzym dat steeds meer in verband wordt gebracht met hersenontwikkeling, stofwisseling en kanker—schetst de studie een algemeen stappenplan om kleine moleculen te ontdekken die enkelen binnen drukbezette eiwitfamilies herkennen en bijsturen in hun natuurlijke cellulaire omgeving.
Bronvermelding: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Trefwoorden: proteïnecomplexen, chemische probes, RNA-methylering, allosterische modulatie, chemoproteomica