Clear Sky Science · pl
Ligandy kowalencyjne ograniczone do complexoform, które allosterycznie agonizują METTL5
Celowanie w jednego gracza w zatłoczonej komórce
Wewnątrz każdej komórki ludzkiej tysiące różnych maszyn białkowych rywalizuje o miejsce, włączając się i wyłączając, by kontrolować wszystko, od zużycia energii po układanie połączeń w mózgu. Wiele z tych maszyn zbudowanych jest z kilku białkowych części, które zestawiają się w różnych kombinacjach, tworząc rodziny podobnych do siebie kompleksów. W artykule pokazano, jak chemicy mogą zaprojektować małe cząsteczki przyczepiające się tylko do jednej, konkretnej wersji takiego kompleksu i zamiast go wyłączać, w rzeczywistości zwiększające jego aktywność. Praca koncentruje się na parze białek, która pomaga regulować sposób, w jaki rybosomy odczytują informację genetyczną, oferując nową drogę precyzyjnej korekty produkcji białek.
Dlaczego miksowanie białek ma znaczenie
Nasze ~20 000 genów daje początek znacznie większej liczbie odrębnych form białek. Po składaniu RNA, modyfikacjach chemicznych i złożeniu w wielobiałkowe maszyny każdy gen może dawać wiele „proteoform”. Ważną kategorią są „complexoformy” — różne kombinacje białek tworzące pokrewne, lecz odmienne kompleksy. Małe białko adaptorowe TRMT112 jest tu wymownym przykładem. Działa jako węzeł, wiążąc kilka różnych metylotransferaz, które przyłączają drobne znaczniki chemiczne do RNA, DNA lub białek. Ponieważ TRMT112 współpracuje z wieloma enzymami, jego genetyczne wyłączenie lub zablokowanie za pomocą niespecyficznego leku zaburzyłoby jednocześnie wiele ścieżek. Autorzy postawili więc pytanie: czy można znaleźć związek, który wiąże tylko jedną partnerską relację TRMT112 i zmienia zachowanie tylko tego jednego enzymu?
Projektowanie subtelnych sond chemicznych
Aby sprawdzić ten pomysł, badacze zbudowali nową rodzinę zwartej, trójwymiarowej chemii — bicyclopirrolidynowe akrylamidy. Związki te zaprojektowano tak, by reagowały kowalencyjnie z cysteiną, siarkowym aminokwasem często występującym w reaktywnych kieszeniach białek. Przy użyciu metody chemoproteomicznej znanej jako profilowanie aktywności białek (activity‑based protein profiling) wystawili żywe komórki nowotworowe na pary lustrzanych wersji tych związków, a następnie użyli spektrometrii mas, aby zobaczyć, które białka zostały oznakowane. Porównując, jak silnie każda lustrzana forma wiązała się, mogli wychwycić interakcje silnie zależne od kształtu. Pomimo mniejszej ogólnej reaktywności niż wcześniejsze rodziny sond, nowe związki trafiały w odrębny zestaw białek, w tym TRMT112.
Odnalezienie pojedynczego uprzywilejowanego partnerstwa
Bliższa analiza ujawniła dziwne rozbieżności. Jeden test monitorujący całe białka sugerował, że sondy niemal całkowicie blokują znakowanie TRMT112 standardowym reagentem. Jednak drugi, bardziej bezpośredni test analizujący pojedyncze miejsca cysteinowe wykazał jedynie umiarkowany efekt na jedną konkretną cysteinę w TRMT112. To sugerowało, że związki rozpoznają tylko ułamek wszystkich cząsteczek TRMT112 — ułamek związany z konkretnym partnerem. Poprzez rozdzielenie ekstraktów komórkowych według rozmiaru i współekspresję różnych znanych partnerów TRMT112 zespół wykazał, że wiązanie sondy pojawia się tylko wtedy, gdy TRMT112 jest sparowany z jednym enzymem, METTL5, który modyfikuje określoną adeninę w małym rRNA rybosomalnym. Wyłączenie METTL5 likwidowało interakcję, a różne poziomy METTL5 w liniach komórkowych zmieniały stopień zaangażowania TRMT112, potwierdzając, że sonda rozpoznaje complexoformę TRMT112:METTL5.
Widzenie i regulacja interfejsu molekularnego
Po zidentyfikowaniu tego partnerstwa autorzy dopracowali swoje molekuły, by wiązały się mocniej i selektywniej. Zoptymalizowany związek, FWG‑33B, zareagował z jedną cysteiną w TRMT112 położoną bezpośrednio na interfejsie z METTL5. Krystalografia rentgenowska ukazała FWG‑33B klinujący się w kieszeni utworzonej wspólnie przez oba białka, daleko od miejsca aktywnego METTL5, ale wystarczająco blisko, by wywołać subtelną zmianę kształtu elastycznej pętli w okolicy miejsca wiązania kofaktora enzymu. Ta złożona kieszeń istnieje tylko w kompleksie TRMT112:METTL5, a nie w podobnych kompleksach, które TRMT112 tworzy z innymi enzymami. Testy biochemiczne z syntetycznymi fragmentami RNA ujawniły efekt funkcjonalny: po kowalencyjnym związaniu FWG‑33B METTL5 silniej wiązał swój substrat RNA i metylował go około dwa razy wydajniej, podczas gdy kontrolna mutacja usuwająca docelową cysteinę znosiła ten wzrost aktywności.
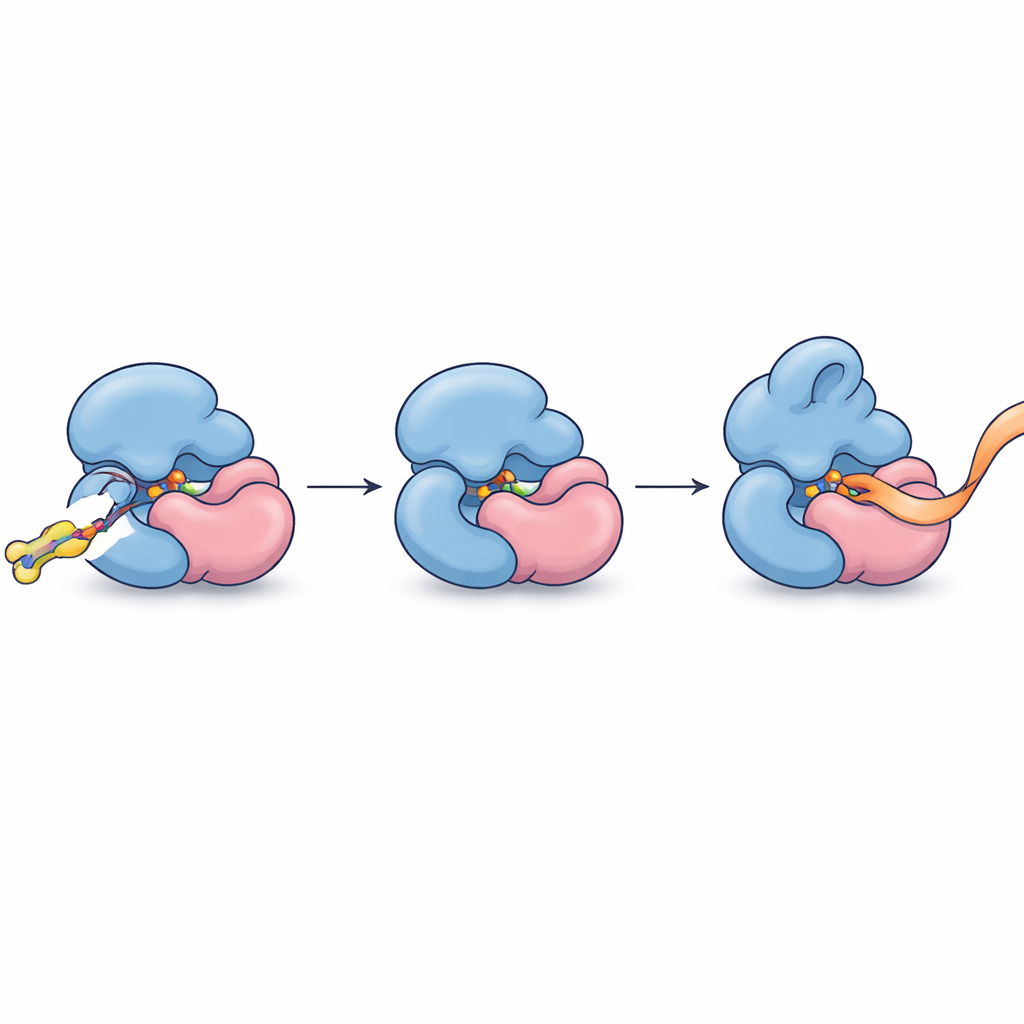
Przemienianie precyzyjnego wiązania w precyzyjną kontrolę
Mówiąc obrazowo, badacze znaleźli sposób, by wsunąć maleńką molekularną klinę w szew między dwiema częściami białkowymi, aby subtelnie usztywnić i przeformować ich uchwyt na RNA, przyspieszając pracę jednego, specyficznego enzymu metylującego bez zaburzania jego „krewniaków”. Pokazuje to, że nawet silnie powiązane białka adaptorowe, uważane wcześniej za zbyt grubiańskie cele, można adresować na poziomie poszczególnych kompleksów przy użyciu chemii kowalencyjnej i profilowania całego proteomu. Oprócz dostarczenia pierwszych allosterycznych agonistów chemicznych dla METTL5 — enzymu coraz częściej związanego z rozwojem mózgu, metabolizmem i rakiem — badanie przedstawia ogólny plan odkrywania małych cząsteczek, które rozpoznają i modulują pojedyncze człony zatłoczonych rodzin białkowych w ich natywnym środowisku komórkowym.
Cytowanie: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Słowa kluczowe: kompleksy białkowe, sondy chemiczne, metylacja RNA, modulacja allosteryczna, chemoproteomika