Clear Sky Science · ru
Ковалентные лиганды, ограниченные complexoform, для TRMT112, которые аллостерически активируют METTL5
Нацеленность на одного участника в переполненной клетке
Внутри каждой человеческой клетки тысячи различных белковых машин толкаются за место, включаясь и выключаясь, чтобы регулировать всё: от расхода энергии до организации нейронных связей. Многие из этих машин состоят из нескольких белковых частей, которые собираются в разных сочетаниях, образуя семьи похожих комплексов. В этой статье показано, как химики могут создать маленькие молекулы, захватывающие именно одну конкретную версию такого комплекса и, вместо того чтобы отключать её, фактически усиливающие её работу. Работа посвящена паре белков, которая помогает настраивать, как рибосомы считывают генетическую информацию, предлагая новый способ с высокой точностью регулировать биосинтез белка.
Почему важно смешивание белковых частей
Наши примерно 20 000 генов дают начало гораздо большему числу различных белковых сущностей. После сплайсинга РНК, химических модификаций и сборки в много‑белковые машины каждый ген может порождать многие «протеоформы». Важная категория здесь — «complexoформы» — разные комбинации белков, формирующие родственные, но разные комплексы. Маленький адаптер TRMT112 — яркий пример. Он действует как узел, связывая несколько различных метилтрансфераз, которые прикрепляют крошечные химические метки к РНК, ДНК или белкам. Поскольку TRMT112 взаимодействует со множеством ферментов, его выключение генетически или грубым лекарством повредило бы сразу несколько путей. Авторы поставили другой вопрос: можно ли найти соединение, которое связывается только с одной парой TRMT112 и меняет поведение лишь этого единственного фермента?
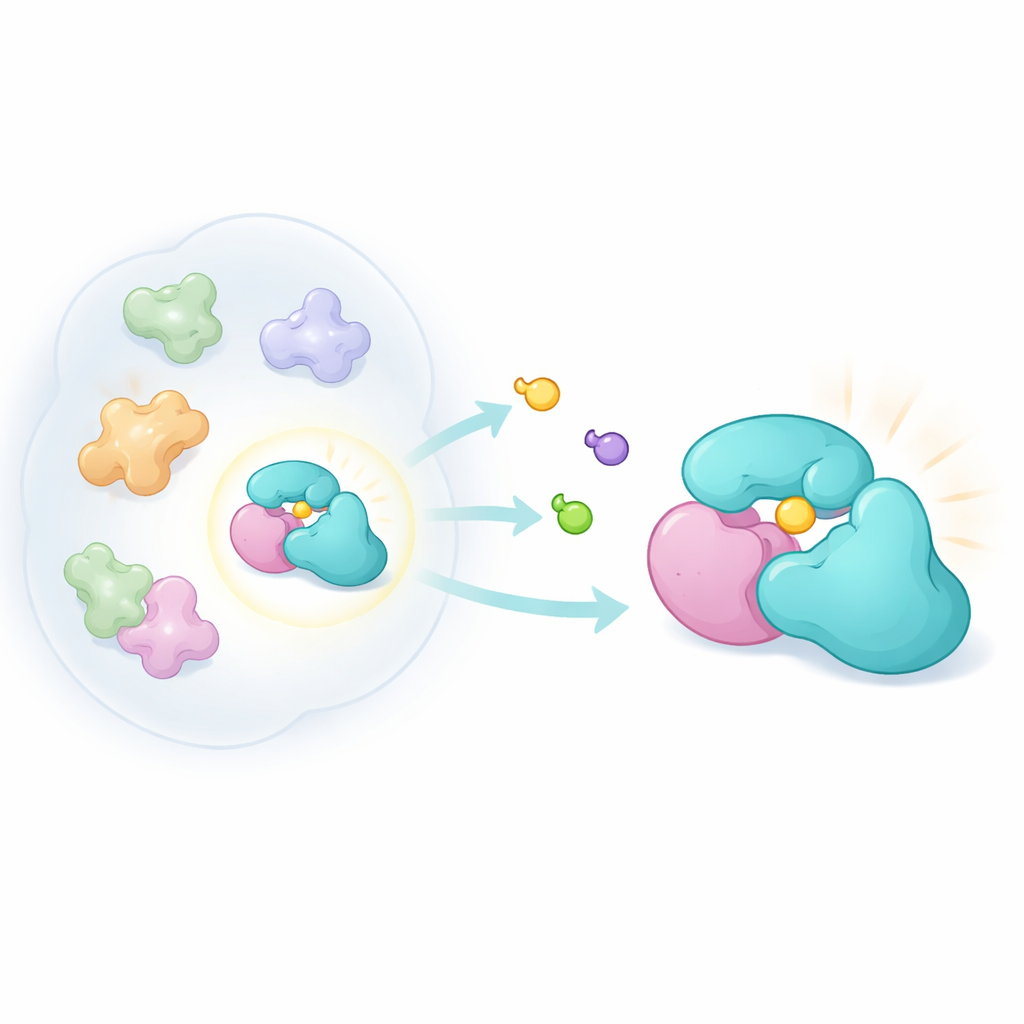
Проектирование тонких химических зондов
Чтобы исследовать эту идею, исследователи создали новую семью компактных трёхмерных молекул — бициклопирролидиновых акриламидов. Эти соединения рассчитаны на ковалентную реакцию с цистеином — серосодержащей аминокислотой, которая часто располагается в реактивных карманах белков. Используя хемопротеомный метод, известный как профилирование активности белков, они обрабатывали живые раковые клетки парами зеркальных версий этих соединений и затем с помощью масс‑спектрометрии определяли, какие белки были мечены. Сравнивая, насколько сильно связывались зеркальные изомеры, можно было выявить взаимодействия, строго зависящие от формы. Несмотря на меньшую общую реактивность по сравнению с ранними семействами зондов, новые соединения поражали специфический набор белков, включая TRMT112.
Нахождение единственной предпочтительной пары
Более тщательный анализ выявил странное несоответствие. Один тест, наблюдающий белки в целом, показал, что зонды почти полностью блокировали маркировку TRMT112 стандартным реактивом. Но второй, более прямой тест, рассматривающий отдельные сайты цистеина, показал лишь умеренный эффект на один конкретный цистеин в TRMT112. Это подсказало, что соединения узнают только часть всех молекул TRMT112 — ту долю, связанную с определённым партнёром. Разделяя клеточные экстракты по размеру и сопреэкспрессируя разные известные партнёрские белки TRMT112, команда показала, что связывание зонда проявляется только когда TRMT112 спарен с одним ферментом, METTL5, который модифицирует конкретный аденин в малой рибосомальной РНК. Удаление METTL5 устраняло взаимодействие, а варьирование уровней METTL5 в разных линиях клеток изменяло степень вовлечённости TRMT112, что подтвердило: зонд распознаёт complexoform TRMT112:METTL5.
Наблюдение и настройка молекулярного интерфейса
Выявив эту пару, авторы усовершенствовали молекулы, чтобы они связывались плотнее и селективнее. Оптимизированное соединение, FWG‑33B, реагировало с одним цистеином в TRMT112, расположенным прямо на интерфейсе с METTL5. Рентгеновская кристаллография комплекса показала, что FWG‑33B заправлен в карман, образованный совместно обоими белками — далеко от активного центра METTL5, но достаточно близко, чтобы вызвать тонкую перестройку гибкой петли рядом с участком связывания кофактора фермента. Этот составной карман существует только в комплексе TRMT112:METTL5 и отсутствует в похожих комплексах, которые TRMT112 образует с другими ферментами. Биохимические тесты с синтетическими фрагментами РНК показали функциональный результат: после ковалентного присоединения FWG‑33B METTL5 стал охотнее связывать свою РНК‑мишень и метилировал её примерно вдвое эффективнее, тогда как контрольная мутация, удаляющая целевой цистеин, устраняла такой эффект.
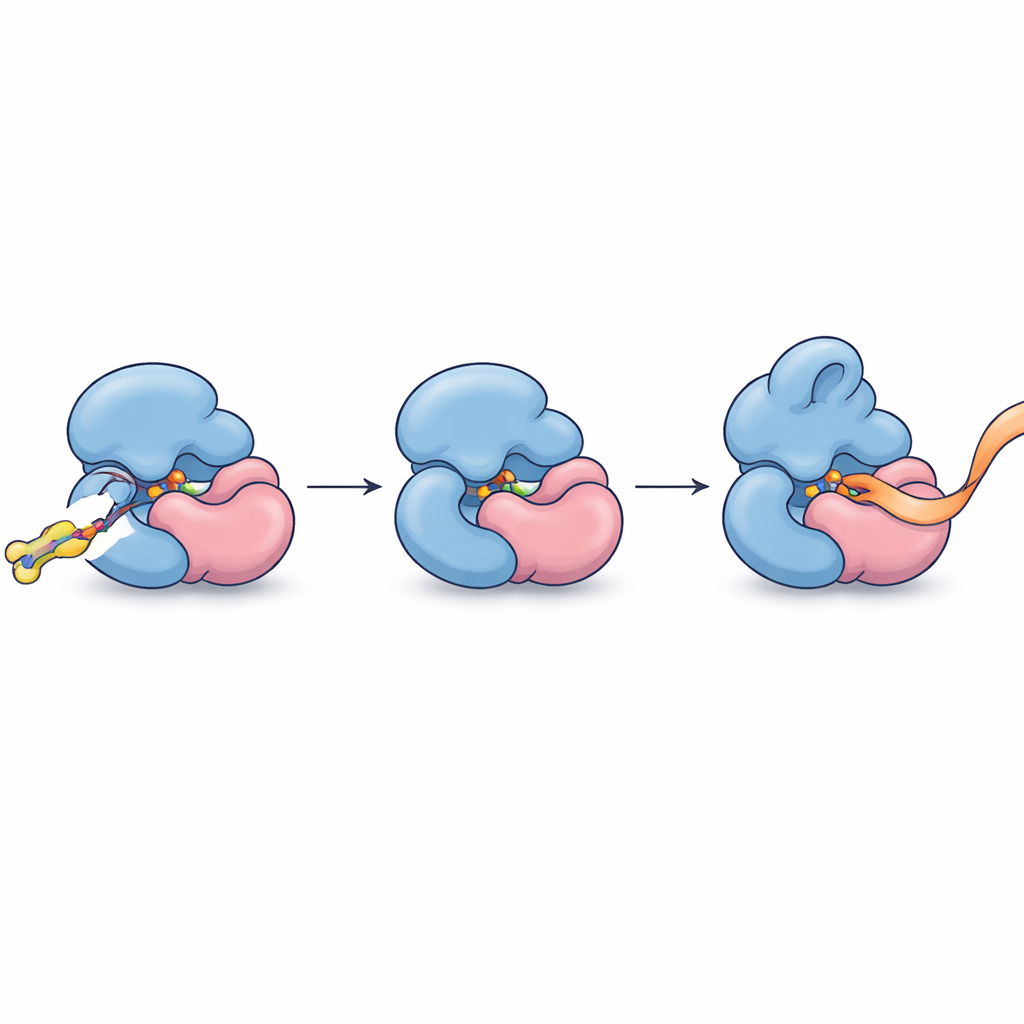
От точного связывания — к точному управлению
Проще говоря, исследователи нашли способ подсовывать крошечную молекулярную клин‑подкладку в шов между двумя белковыми частями, чтобы немного подтянуть и изменить их захват РНК, заставив один конкретный метилирующий фермент работать быстрее, не затрагивая «родственников». Это демонстрирует, что даже высокосвязанные адаптерные белки, считавшиеся слишком грубой целью, можно адресовать на уровне отдельных комплексов с помощью ковалентной химии и протеомного профилирования. Помимо того что работа представляет первые аллостерические химические агонисты для METTL5 — фермента, который всё чаще связывают с развитием мозга, метаболизмом и раком — исследование предлагает общую схему для поиска малых молекул, распознающих и настраивающих отдельных членов переполненных белковых семейств в их нативной клеточной среде.
Цитирование: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Ключевые слова: белковые комплексы, химические зонды, метилирование РНК, аллостерическая модуляция, хемопротеомика