Clear Sky Science · he
ליגנדים קוולנטיים המוגבלים לצורת קומפלקס שמפעילים אולוסטרית את METTL5
לחץ על שחקן בודד בתוך תא צפוף
בתוך כל תא אנושי, אלפי מכונות חלבוניות שונות נדחפות זו בזו, מפעילות וכבות כדי לשלוט בכל דבר מתחזוקת האנרגיה ועד חיבורי המוח. רבות מהמכונות האלה בנויות ממספר חלקים חלבוניים שמתחברים ביניהם בצירופים שונים, ויוצרים משפחות של קומפלקסים דומים זה לזה. המאמר הזה מראה כיצד כימאים יכולים לתכנן מולקולות קטנות שיתפסו רק גרסה ספציפית של קומפלקס כזה ובמקום לכבות אותה — למעשה יגרמו לה לפעול חזק יותר. המחקר מתמקד בזוג חלבונים המסייע לכוונן את אופן קריאת המידע הגנטי בריבוזומים, ומציע דרך חדשה לכוונון ייצור החלבון בדיוק גבוה.
מדוע מיקס‑וחיבור של חלבונים חשוב
יש לנו בערך 20,000 גנים, אך הם מניבים הרבה יותר מ‑20,000 ישויות חלבוניות נפרדות. אחרי החיתוך של ה‑RNA, שינויים כימיים והרכבה למכונות רב‑חלבוניות, כל גן יכול להוליד רבות "פרוטאופורמות". קטגוריה חשובה היא "קומפלקואפורמות" — צירופים שונים של חלבונים היוצרים קומפלקסים קרובים אך מובחנים. חלבון מתאם קטן בשם TRMT112 הוא דוגמה בולטת. הוא משמש כצומת, נקשר למספר שונה של אנזימי מתיל־טרנספארז שמוסיפים תגיות כימיות קטנות ל‑RNA, ל‑DNA או לחלבונים. מכיוון ש‑TRMT112 משתף פעולה עם רבים כאלה, כיבוי גנטי שלו או טיפול בתרופה כללית עלול לערבב מספר מסלולים בבת אחת. המחברים שאלו במקום זאת: האם אפשר למצוא תרכובת שנקשרת רק לשותפות ספציפית אחת של TRMT112 ומשנה את התנהגותו של אותו אנזים בלבד?
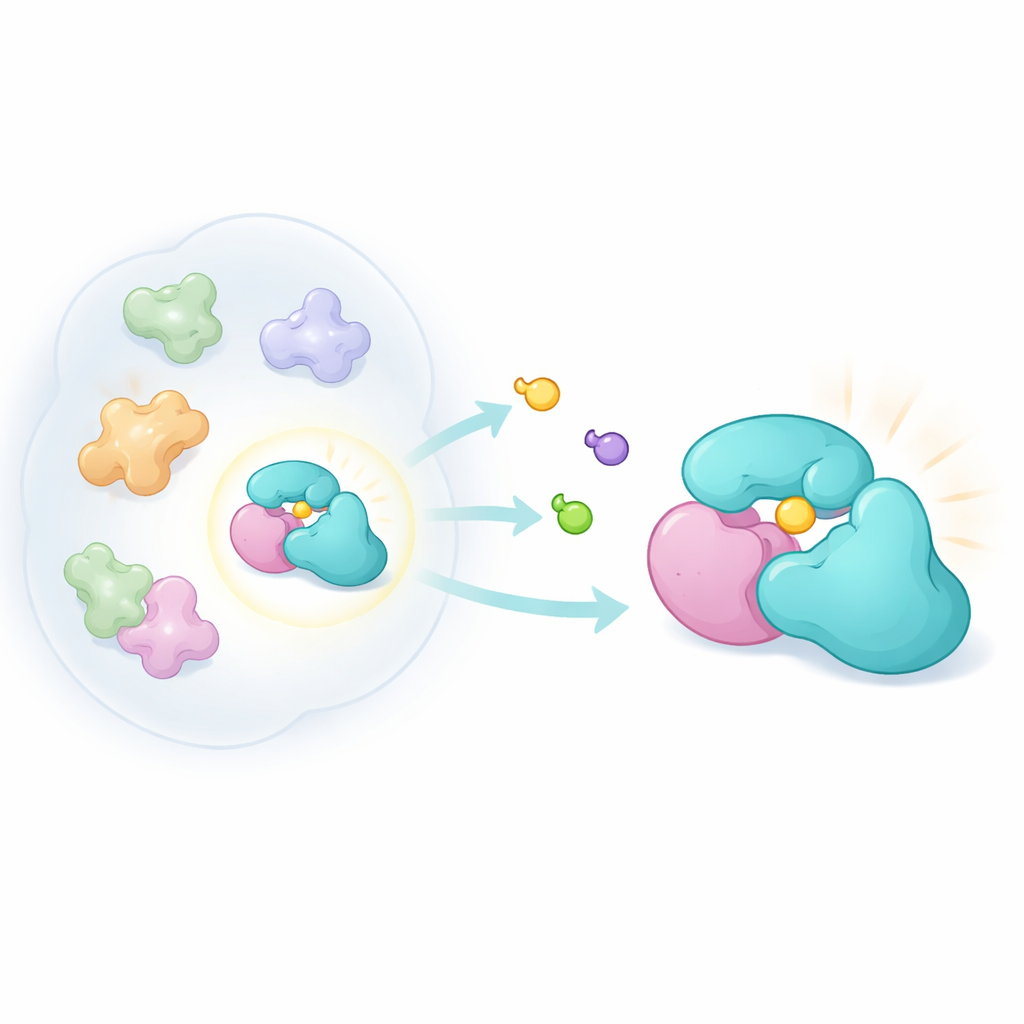
עיצוב גלאים כימיים עדינים
כדי לחקור את הרעיון הזה, החוקרים בנו משפחה חדשה של מולקולות קומפקטיות תלת‑ממדיות שנקראות ביסיקלופירולידין אקרילאמידים. תרכובות אלה מתוכננות להגיב קוולנטית עם ציסטאין, חומצת אמינו המכילה גופרית שלעתים נוטה לשבת בכיסים תגובתיים על חלבונים. באמצעות שיטה כימופרוטאומית המוכרת כפרופילינג חלבוני מבוסס פעילות, הם חשפו תאי סרטן חיים לזוגות של גרסאות מראות של התרכובות ואז השתמשו בספקטרומטריית מסה כדי לראות אילו חלבונים תויגו. על‑ידי השוואת חוזק הקשירה של כל תמונת מראה, הם יכלו לצפות באינטראקציות התלויות מאוד בצורה. למרות שהיו פחות תגובתיות כללית יחסית למשפחות גלאים קודמות, התרכובות החדשות הכו סט מובחן של חלבונים, כולל TRMT112.
מציאת שותפות יחידה מועדפת
ניתוח מעמיק גילה חוסר התאמה מעניין. בדיקה אחת שצפתה בחלבונים שלמים הציעה כי הגלאים חסמו כמעט לחלוטין את סימונו של TRMT112 על‑ידי תג חותם סטנדרטי. אך בדיקה שנייה, ישירה יותר, שחיפשה אתרי ציסטאין בודדים הראתה השפעה מתונה רק על ציסטאין מסוים אחד ב‑TRMT112. זה רמז שהתרכובות זיהו רק שבריר מהמולקולות של TRMT112 — השבריר הקשור לשותף מסוים. על‑ידי הפרדת תמציות תא לפי גודל ועל‑ידי הבעה משותפת של שותפים ידועים שונים של TRMT112, הצוות הראה שקשר הגלאי הופיע רק כאשר TRMT112 היה מזווג עם אנזים אחד, METTL5, שמתווך שינוי של אדנין ספציפי ב‑rRNA הקטן של הריבוזום. השחתת METTL5 ביטלה את האינטראקציה, ושינוי ברמות METTL5 בתאי שורות שונות שינה כמה TRMT112 היה קשור, ואישר שהגלאי מזהה קומפלקואפורמה של TRMT112:METTL5.
ראייה וכיוונון ממשק מולקולרי
לאחר שאיתרו את השותפות הזו, המחברים שיפרו את המולקולות כדי לקשור איתן בחוזקה ובבררנות רבה יותר. תרכובת ממוטבת, FWG‑33B, הגיבה עם ציסטאין בודד ב‑TRMT112 הממוקם ממש בממשק עם METTL5. קריסטלוגרפיית קרני־X של הקומפלקס הראתה את FWG‑33B מוחדר בכיס שנוצר במשותף על‑ידי שני החלבונים, רחוק מאתר הפעילות של METTL5 אך מספיק קרוב כדי לעורר עיוות עדין של לולאה גמישה בצמוד לאזור קישור המקורן של האנזים. הכיס המשותף הזה קיים רק בקומפלקס TRMT112:METTL5 ולא בקומפלקסים דומים ש‑TRMT112 יוצר עם אנזימים אחרים. ניסויים ביוכימיים עם רסיסי RNA סינתטיים חשפו את התוצאה התפקודית: אחרי קשירה קוולנטית של FWG‑33B, METTL5 קישר את תת‑הסרטן RNA שלו ביתר קלות ומתיל אותו בערך פי שניים ביעילות, בעוד שמוטציה בקרתית שהסירה את הציסטאין המיועד ביטלה את ההגברה הזו.
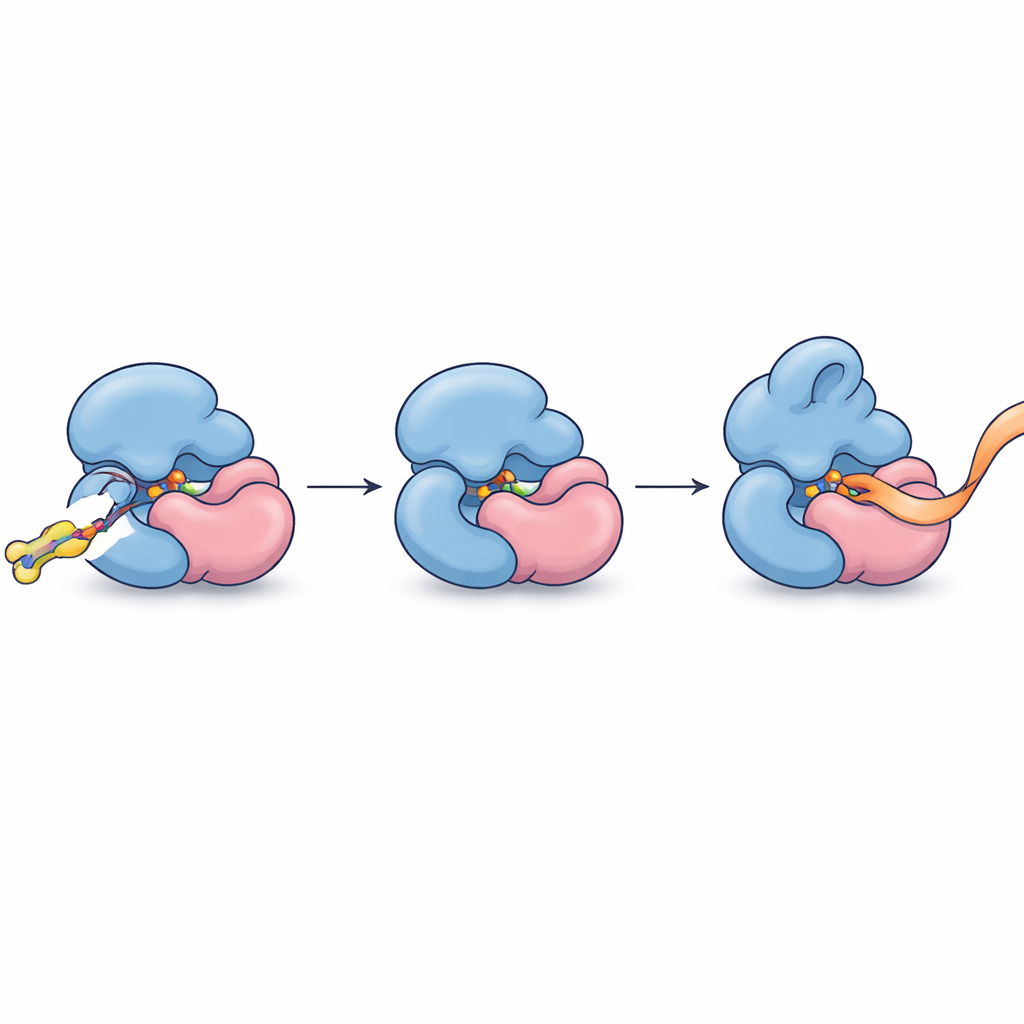
הפיכת קשירה מדויקת לשליטה מדויקת
במונחים יום‑יומיים, החוקרים מצאו דרך להחליק כלי־שיפוע מולקולרי קטן לתפר בין שני חלקי חלבון כדי להדק ולעצב במעט את אחיזתם על ה‑RNA, ולהפוך אנזים מתילציה ספציפי אחד למהיר יותר מבלי להפריע לקרוביו. זה ממחיש שגם חלבוני מתאם בעלי חיבורים רבים, שלפני כן נחשבו ליעד גס מדי, ניתנים לגישה ברמת קומפלקס יחיד באמצעות כימיה קוולנטית ופרופיילינג פרוטאומי ברמת הפרוטאום כולו. מעבר לכך שהוא מספק את הגלאים האלוסטריים הכימיים הראשונים ל‑METTL5 — אנזים שמתקשר יותר ויותר להתפתחות המוח, למטבוליזם ולסרטן — המחקר מתווה תבנית כללית לגילוי מולקולות קטנות שמזהות ומכוונות חבר יחיד מתוך משפחות חלבוניות צפופות בתוך סביבת התא הטבעית שלו.
ציטוט: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
מילות מפתח: קומפלקסי חלבון, גלאי כימי, מתילציה של RNA, מודולציה אלוסטרית, כימופרוטאומיקה