Clear Sky Science · es
Ligandos covalentes restringidos a complexoformas de TRMT112 que agonizan alostéricamente METTL5
Apuntar a un actor en una célula congestionada
Dentro de cada célula humana, miles de máquinas proteicas distintas compiten por el espacio, activándose y desactivándose para controlar desde el uso de energía hasta el cableado cerebral. Muchas de estas máquinas se ensamblan a partir de varias piezas proteicas que se combinan de diferentes maneras, creando familias de complejos que se parecen entre sí. Este artículo muestra cómo los químicos pueden diseñar pequeñas moléculas que se enganchan a una versión específica de ese tipo de complejo y, en lugar de apagarla, en realidad la hacen funcionar más. El trabajo se centra en un par de proteínas que ayudan a ajustar cómo los ribosomas leen la información genética, ofreciendo una nueva forma de modular la producción proteica con gran precisión.
Por qué importa el mezclar y emparejar proteínas
Nuestros aproximadamente 20.000 genes dan lugar a muchas más de 20.000 entidades proteicas distintas. Tras el empalme del ARN, las modificaciones químicas y el ensamblaje en máquinas multiproteicas, cada gen puede generar muchas “proteoformas”. Una categoría relevante son las “complexoformas”: combinaciones distintas de proteínas que forman complejos relacionados pero no idénticos. Una proteína adaptadora pequeña llamada TRMT112 es un ejemplo llamativo. Actúa como un núcleo, uniéndose a varias metiltransferasas que añaden pequeñas etiquetas químicas al ARN, al ADN o a proteínas. Dado que TRMT112 se asocia con muchas enzimas, desactivarla genéticamente o con un fármaco contundente alteraría múltiples vías a la vez. Los autores, en cambio, se preguntaron: ¿es posible encontrar un compuesto que sólo se una a una asociación concreta de TRMT112 y cambie el comportamiento de esa única enzima?
Diseñar sondas químicas sutiles
Para explorar esta idea, los investigadores construyeron una nueva familia de moléculas compactas y tridimensionales denominadas acrilamidas biciclopirrolidina. Estos compuestos están diseñados para reaccionar covalentemente con cisteína, un aminoácido que contiene azufre y que a menudo se sitúa en bolsillos reactivos de las proteínas. Empleando un método quimoproteómico conocido como perfilado de proteínas basado en actividad, expusieron células cancerosas vivas a pares de versiones en imagen especular de estos compuestos y luego usaron espectrometría de masas para ver qué proteínas quedaban etiquetadas. Al comparar cuánto se unía cada isómero, podían detectar interacciones muy dependientes de la forma. A pesar de ser menos reactivos en general que familias de sondas anteriores, los nuevos compuestos golpearon un conjunto distinto de proteínas, incluida TRMT112.
Encontrar una asociación favorecida única
Un análisis más detallado reveló una discrepancia curiosa. Un ensayo que observa proteínas completas sugirió que las sondas casi bloqueaban por completo la marcación de TRMT112 por un reactivo estándar. Sin embargo, un segundo ensayo más directo que examina sitios de cisteína individuales mostraba sólo un efecto modesto sobre una cisteína particular en TRMT112. Esto indicaba que los compuestos reconocían sólo una fracción de todas las moléculas de TRMT112: la fracción unida a un socio concreto. Separando extractos celulares por tamaño y coexpresando distintos socios conocidos de TRMT112, el equipo demostró que la unión de la sonda aparecía solo cuando TRMT112 estaba emparejada con una enzima, METTL5, que modifica una adenina específica en el ARN ribosómico pequeño. La eliminación de METTL5 abolió la interacción, y variar los niveles de METTL5 entre líneas celulares cambió cuánto TRMT112 estaba comprometida, confirmando que la sonda reconoce una complexoforma TRMT112:METTL5.
Ver y ajustar la interfaz molecular
Tras identificar esta asociación, los autores refinaron sus moléculas para que se unieran con mayor fuerza y selectividad. Un compuesto optimizado, FWG‑33B, reaccionó con una única cisteína en TRMT112 situada justo en la interfaz con METTL5. La cristalografía de rayos X del complejo mostró a FWG‑33B encajado en un bolsillo formado conjuntamente por ambas proteínas, lejos del sitio activo de METTL5 pero lo bastante cerca como para provocar una sutil remodelación de un bucle flexible cercano a la región de unión del cofactor de la enzima. Este bolsillo compuesto existe solo en el complejo TRMT112:METTL5 y no en complejos similares que TRMT112 forma con otras enzimas. Ensayos bioquímicos con fragmentos de ARN sintético revelaron el resultado funcional: tras la unión covalente de FWG‑33B, METTL5 se unió más fácilmente a su sustrato de ARN y lo metiló aproximadamente el doble de eficiente, mientras que una mutación de control que eliminaba la cisteína objetivo abolió este aumento.
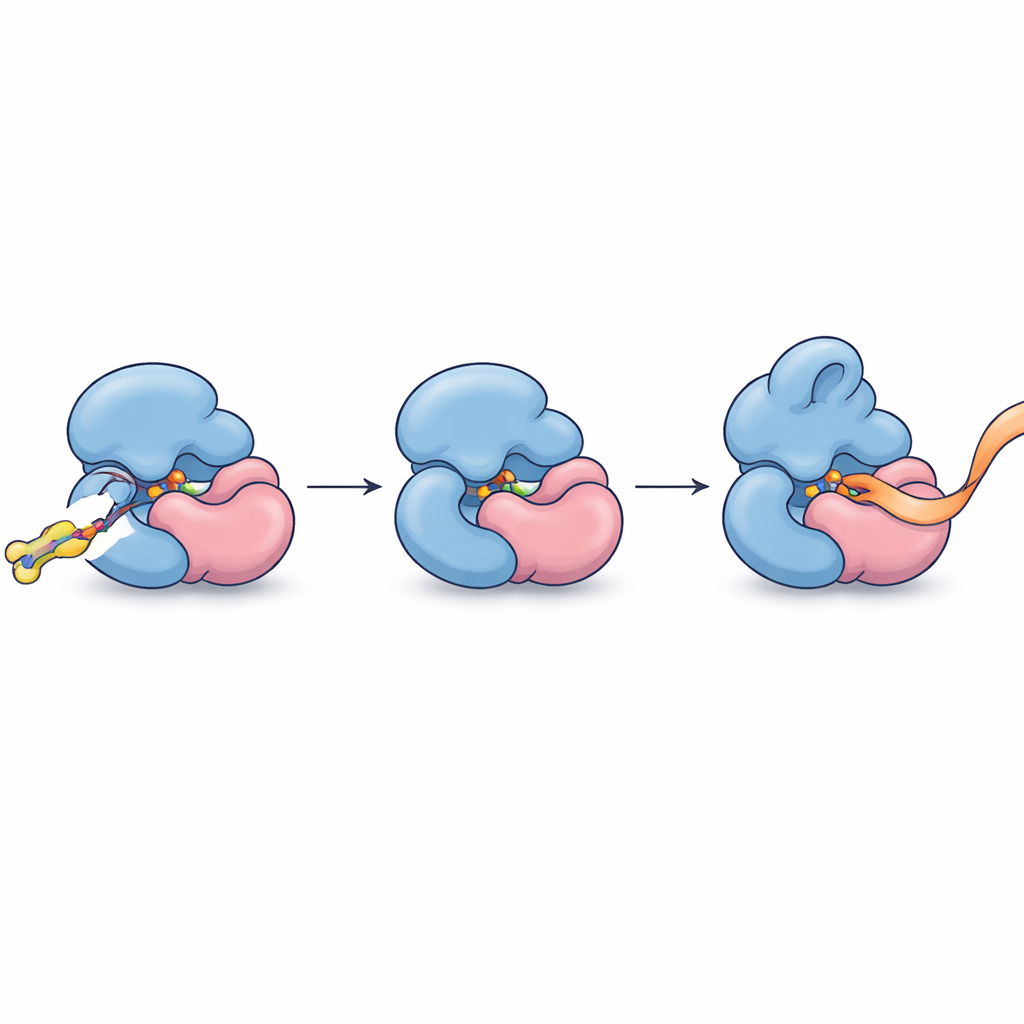
Convertir una unión precisa en control preciso
En términos cotidianos, los investigadores han encontrado una forma de deslizar una pequeña cuña molecular en la unión entre dos partes proteicas para apretar y remodelar sutilmente su agarre sobre el ARN, haciendo que una enzima metiladora específica trabaje más deprisa sin perturbar a sus parientes. Esto demuestra que incluso proteínas adaptadoras altamente conectadas, antaño consideradas objetivos demasiado burdos, pueden atacarse al nivel de complejos individuales usando química covalente y perfilado a escala del proteoma. Además de proporcionar los primeros agonistas químicos alostéricos para METTL5—una enzima cada vez más vinculada al desarrollo cerebral, el metabolismo y el cáncer—el estudio traza un plan general para descubrir pequeñas moléculas que reconozcan y ajusten miembros singulares de familias proteicas congestionadas dentro de su entorno celular nativo.
Cita: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Palabras clave: complejos proteicos, sondas químicas, metilación de ARN, modulación alostérica, quimoproteómica