Clear Sky Science · fr
Ligands covalents restreints aux complexoformes de TRMT112 qui agonisent allostériquement METTL5
Cibler un acteur au milieu de la foule cellulaire
À l'intérieur de chaque cellule humaine, des milliers de machines protéiques différentes se côtoient, s'activant et se désactivant pour réguler tout, de l'utilisation d'énergie à la mise en place des circuits cérébraux. Nombre de ces machines sont assemblées à partir de plusieurs sous‑unités protéiques qui s'associent en combinaisons variées, formant des familles de complexes aux allures semblables. Cet article montre comment des chimistes peuvent concevoir de petites molécules qui se lient à une version spécifique d'un tel complexe et, au lieu de l'inhiber, augmentent effectivement son activité. Le travail se concentre sur une paire de protéines qui ajuste la façon dont les ribosomes lisent l'information génétique, offrant une nouvelle façon de moduler la production protéique avec une grande précision.
Pourquoi l'association protéique importe
Nos quelque 20 000 gènes donnent naissance à bien plus de 20 000 entités protéiques distinctes. Après l'épissage de l'ARN, les modifications chimiques et l'assemblage en machines multi‑protéiques, chaque gène peut engendrer de nombreux « protéoformes ». Une catégorie importante est celle des « complexoformes » — des combinaisons différentes de protéines qui forment des complexes apparentés mais distincts. Une petite protéine adaptatrice nommée TRMT112 en est un exemple marquant. Elle agit comme un centre, se liant à plusieurs méthyltransférases qui ajoutent de petites marques chimiques à l'ARN, à l'ADN ou aux protéines. Parce que TRMT112 s'associe à de nombreuses enzymes, l'éteindre génétiquement ou par un médicament non sélectif perturberait simultanément plusieurs voies. Les auteurs se sont donc demandé : peut‑on trouver un composé qui ne se lie qu'à une seule association de TRMT112 et modifie le comportement de cette seule enzyme ?
Concevoir des sondes chimiques subtiles
Pour explorer cette idée, les chercheurs ont construit une nouvelle famille de petites molécules tridimensionnelles appelées acrylamides bicyclopyrrolidines. Ces composés sont conçus pour réagir de manière covalente avec la cystéine, un acide aminé contenant du soufre qui se trouve souvent dans des poches réactives des protéines. En utilisant une méthode chimio‑protéomique connue sous le nom de profilage d'activité basé sur les protéines, ils ont exposé des cellules cancéreuses vivantes à des paires d'énantiomères de ces composés puis ont utilisé la spectrométrie de masse pour identifier les protéines marquées. En comparant l'affinité des deux images miroir, ils ont pu repérer des interactions fortement dépendantes de la forme. Bien que moins réactifs de façon générale que des familles de sondes antérieures, les nouveaux composés ont ciblé un ensemble distinct de protéines, y compris TRMT112.
Identifier un partenariat privilégié
Une analyse plus approfondie a révélé une discordance étonnante. Un essai global observant les protéines entières suggérait que les sondes empêchaient presque complètement TRMT112 d'être marqué par un réactif standard. Pourtant, un second essai plus direct, ciblant des sites cystéine individuels, montrait seulement un effet modeste sur une cystéine particulière de TRMT112. Cela indiquait que les composés reconnaissaient seulement une fraction des molécules de TRMT112 — la fraction associée à un partenaire spécifique. En séparant les extraits cellulaires par taille et en co‑exprimant différents partenaires connus de TRMT112, l'équipe a montré que la liaison de la sonde se produisait uniquement lorsque TRMT112 était apparié à une enzyme, METTL5, qui modifie une adénine particulière dans le petit ARN ribosomique de la cellule. L'ablation de METTL5 supprimait l'interaction, et la variation des niveaux de METTL5 entre lignées cellulaires modifiait la proportion de TRMT112 engagée, confirmant que la sonde reconnaît un complexoforme TRMT112:METTL5.
Observer et ajuster l'interface moléculaire
Après avoir identifié ce partenariat, les auteurs ont affiné leurs molécules pour les rendre plus serrées et plus sélectives. Un composé optimisé, FWG‑33B, a réagi avec une seule cystéine de TRMT112 située justement à l'interface avec METTL5. La cristallographie aux rayons X du complexe a montré FWG‑33B coinçant dans une poche formée conjointement par les deux protéines, éloignée du site actif de METTL5 mais suffisamment proche pour provoquer un remodelage subtil d'une boucle flexible près de la région de liaison du cofacteur de l'enzyme. Cette poche composite n'existe que dans le complexe TRMT112:METTL5 et pas dans des complexes similaires que TRMT112 forme avec d'autres enzymes. Des essais biochimiques avec des fragments d'ARN synthétiques ont révélé le résultat fonctionnel : après la liaison covalente de FWG‑33B, METTL5 se liait plus facilement à son substrat ARN et le méthylait environ deux fois plus efficacement, tandis qu'une mutation témoin supprimant la cystéine ciblée abolissait ce gain.
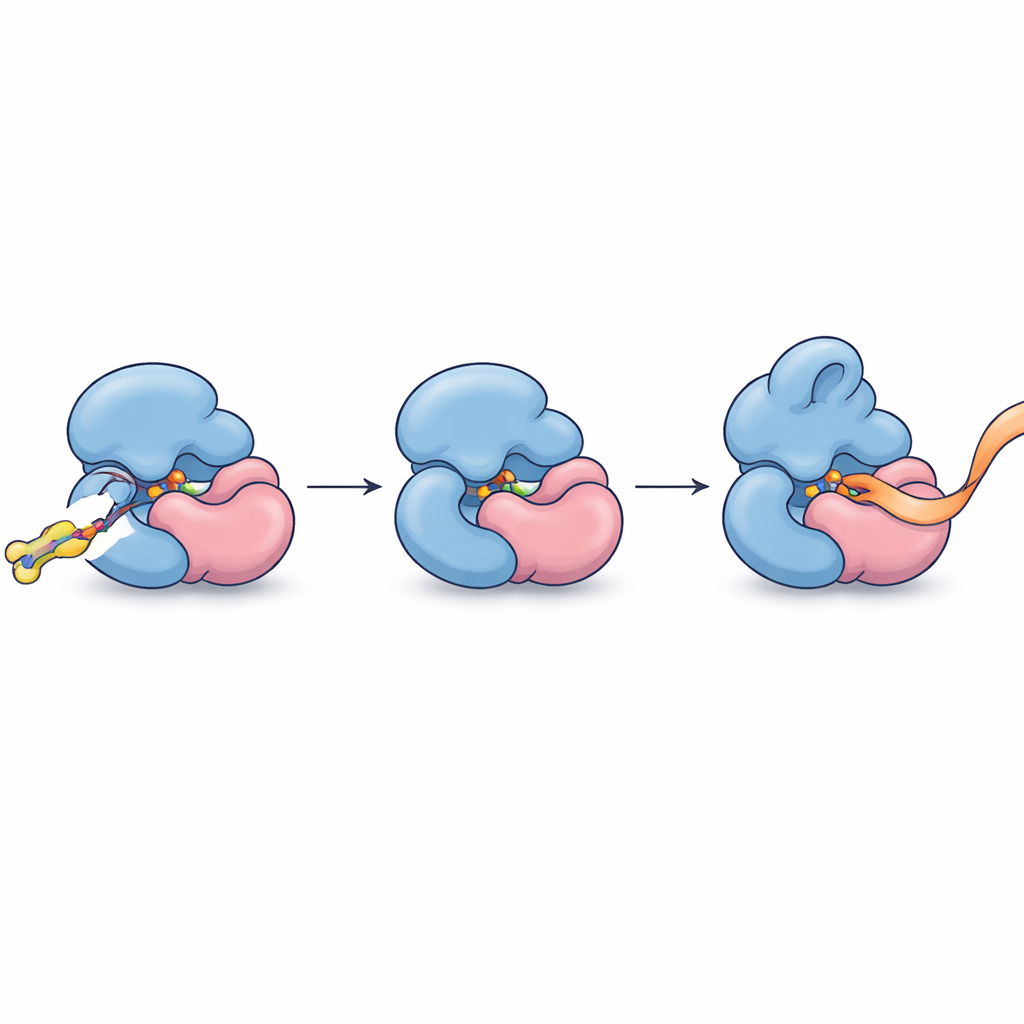
Transformer une liaison précise en un contrôle précis
En termes simples, les chercheurs ont trouvé un moyen d'insérer un petit coin moléculaire dans la jonction entre deux parties protéiques afin de resserrer et remodeler subtilement leur interaction avec l'ARN, faisant fonctionner plus rapidement une enzyme méthylante spécifique sans perturber ses parentes. Cela démontre que même des protéines adaptatrices fortement connectées, longtemps jugées trop grossières comme cibles, peuvent être abordées au niveau de complexes individuels en utilisant la chimie covalente et le profilage à l'échelle du protéome. Au‑delà de fournir les premiers agonistes chimiques allostériques pour METTL5 — une enzyme de plus en plus associée au développement cérébral, au métabolisme et au cancer — l'étude propose un plan général pour découvrir de petites molécules qui reconnaissent et ajustent des membres individuels de familles protéiques encombrées dans leur environnement cellulaire natif.
Citation: Goetzke, F.W., Bernard, S.M., Ju, CW. et al. Complexoform-restricted covalent TRMT112 ligands that allosterically agonize METTL5. Nat Chem Biol 22, 770–782 (2026). https://doi.org/10.1038/s41589-025-02099-5
Mots-clés: complexes protéiques, sondes chimiques, méthylation de l'ARN, modulation allostérique, chimio‑protéomique