Clear Sky Science · tr
Fajlarla supramoleküler montaj yoluyla bakteriyel bağışıklık aktivasyonu
Bakterilerin Viral İstilacılara Karşı Üstün Gelme Yolu
Bakteriler, birkaç dakika içinde gelişen bir mikrobiyal topluluğu mezarlığa çevirebilen faj adı verilen virüslerin sürekli hedefidir. Bu çalışma, bazı bakterilerin karşı koymak için kullandığı şaşırtıcı yeni bir yolu ortaya koyuyor: gelen fajları algılayan ve ardından enfekte hücreyi içten kasten kapatan devasa moleküler halkalar inşa etmek. Bu iş yalnızca bakteriyel özsavunmanın kurnaz bir biçimini ortaya çıkarmakla kalmıyor, aynı zamanda bizim doğuştan gelen bağışıklık sistemimizin kullandığı stratejileri yankılıyor ve hayatın enfeksiyonları algılaması ve durdurmasında ortak temalara işaret ediyor.
Çifte Hayata Sahip Küçük Bir Koruyucu
Makale, yazarların RAZR olarak yeniden adlandırdığı, Escherichia coli ve birçok başka türde bulunan bakteriyel bir proteine odaklanıyor. Tek başına RAZR zararsızdır: hücreler onu yüksek düzeyde üretebilir ve olumsuz bir etki görülmez. Ancak belirli fajlar enfekte ettiğinde, RAZR aniden hem konak hücre hem de virüs için öldürücü hâle gelir. Sistem “abortif enfeksiyon” yoluyla çalışır: RAZR açıldığında, enfekte bakteri büyümeyi durdurur ve etkili bir şekilde kendini feda ederek virüsün daha fazla kopya yapmasını ve popülasyona yayılmasını engeller. RAZR’ın sessiz bir izleyiciden hücresel cellatına ne zaman ve nasıl geçiş yaptığını anlamak çalışmanın merkezindeki sorudur. 
Anahtarı Çeviren Viral Halkalar
Araştırmacılar, RAZR’ın ilgisiz birçok faj tarafından üretilen belirli proteinlerle aktive edildiğini keşfettiler. Bir fajda, muhtemelen viral genomu onarmada veya daireselleştirmede görevli olan Gp77 adlı bir protein tetikleyici olarak görev yaptı. Diğer fajlarda ise tetikleyiciler, viral kabuğun önemli bir kapısında bulunan ve DNA’yı konağa enjekte etmeye yardımcı olan “portal” proteinlerdi. Bu proteinler bireysel moleküller olarak dizilim ve şekil bakımından çok farklı görünseler de hepsinin çarpıcı bir ortak özelliği var: hemen hemen aynı çapa sahip büyük halkalar halinde toplanmaları. Kriyo–elektron mikroskobu kullanarak ekip, Gp77’nin 24 parçalı bir halka oluşturduğunu, portal proteinlerin ise 12 parçalı halkalar oluşturduğunu gösterdi. Normalde gevşek doğrusal zincirler oluşturan RAZR, bu viral halkaların etrafını sararak 25 nanometreden daha geniş çok katmanlı dev bir dairesel kompleks inşa eder.
Moleküler Bir Kıyamet Aygıtı İnşa Etmek
Bu kompleks içinde RAZR iki işlevsel bölgeyi bir araya getirir: viral halkayı kavrayan bir çinko parmak “sensör” ve RNA’yı kesen bir HEPN “bıçak”. Komşu RAZR moleküllerinden iki çinko parmak segmenti her viral protein birimine bağlanır ve böylece RAZR’ın halkayı kesin ve yüksek derecede işbirlikçi bir şekilde kaplamasını sağlar. Bu halka şeklindeki iskelet, RAZR’ın RNA kesen bölgelerini eğimli, sıkı paketlenmiş bir düzenlemeye zorlar; bu sayede çok sayıda kesme bölgesi dış kenarda bir testere dişleri gibi hizalanır. RAZR ile faj proteinleri arasındaki temas yüzeylerini bozan veya RAZR moleküllerinin birbirine yapışma biçimini zayıflatan mutasyonlar savunmayı çökertir. Sensör ile kesici parçayı bağlayan küçük esnek bir bağlantı parçası da hayati önem taşır; protein viral halkayı kavradığında doğru geometrinin benimsenmesine yardımcı olur.
Viral Yayılmayı Durdurmak İçin RNA’yı Parçalamak
Faj kaynaklı iskeleti üzerine monte olduğunda, RAZR güçlü bir RNA yok edici makineye dönüşür. Yazarlar, aktive olmuş RAZR’ın DNA’ya dokunmadığını ancak tek iplikli birçok RNA türünü parçaladığını gösteriyor: transfer RNA’lar, ribozomal RNA’lar ve hem bakteri hem de enfekte eden faj kaynaklı haberci RNA’lar. Canlı hücrelerde bu yaygın RNA kesilmesi hızla protein üretimini engellerken DNA replikasyonu ve transkripsiyonu büyük ölçüde sağlam bırakır. Deney tüpü deneylerinde, saflaştırılmış RAZR’ı viral tetikleyicileri ile karıştırmak protein sentezini kısa sürede durdurmaya yeterlidir. Bu kaba, özgül olmayan şekilde çeviriyi durdurarak sistem enfekte hücreyi mahkûm eder ama aynı zamanda fajı üremek için ihtiyaç duyduğu moleküler araçlardan mahrum bırakır. 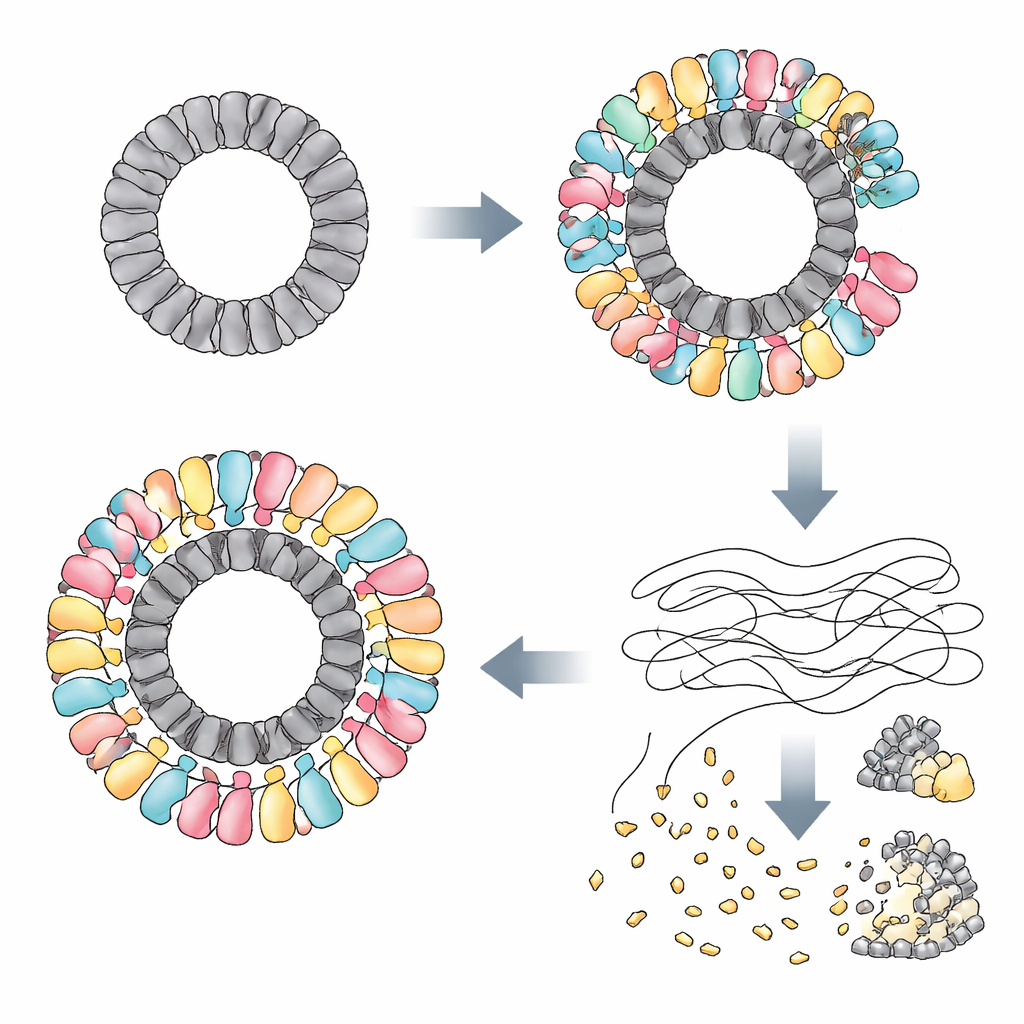
Farklı Virüslere Göre Savunmayı Özelleştirmek
Farklı bakterilerden RAZR proteinleri benzer bir kesme bölgesi paylaşsa da çalışma, çinko parmak sensörlerinin büyük farklılıklar gösterdiğini buluyor. Bu sensör segmentlerini E. coli ve Klebsiella variicola kaynaklı iki RAZR versiyonu arasında değiştirmek, hangi fajları durdurabildiklerini büyük ölçüde değiştiriyor. İki RAZR varyantı aynı faja karşı hedef alsa bile, viral portal proteininin üzerinde biraz farklı temas noktalarına dayanıyorlar; bu durum farklı viral kaçış mutasyonlarıyla gösterildi. Bu, bakterilerin antiviral yelpazesini RAZR’ın sensör kısmını evrimleştirerek ince ayar yapabileceğini, güçlü RNA kesme makinesini ise koruyabileceğini düşündürüyor.
Yaşam Ağacı Boyunca Paylaşılan Fikirler
Sonunda yazarlar, RAZR’ın belirli bir viral “şifre”yi değil yapısal bir imzayı algıladığını öne sürüyor: yalnızca faj enfeksiyonu sırasında ortaya çıkan ve konak makinerisinde bulunmayan belirli boyuttaki büyük protein halkaları. Bu halkaların etrafını sarıp kendi montajı için kalıp olarak kullanarak RAZR, zayıf bir viral sinyali tümüyle açık ya da kapalı bir bağışıklık yanıtına yükseltir. Bu strateji, hayvanlarda, insanlarda da dahil olmak üzere birçok doğuştan bağışıklık kompleksinin patojenleri algılamak ve yıkıcı enzimleri aktive etmek için dev filamentöz veya halka şeklinde montajlar oluşturmasına yakın bir paralellik gösterir. Çalışma böylece çarpıcı bir yakınsama ortaya koyuyor: bakterilerden memelilere, yaşam defalarca istilacı virüslerin geometrisini aleyhlerine çevirecek dev protein yapıları inşa etme yolları evrimleştirmiştir.
Atıf: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Anahtar kelimeler: bakteriyofaj bağışıklığı, bakteriyel doğuştan savunma, supramoleküler protein kompleksi, RNA kesilmesi, RAZR sistemi