Clear Sky Science · it
Attivazione immunitaria batterica tramite assemblaggio supramolecolare con proteine fagiche
Come i batteri ingannano i loro invasori virali
I batteri sono continuamente bersagliati da virus detti fagi, che possono trasformare una comunità microbica fiorente in un cimitero nel giro di pochi minuti. Questo studio svela un modo sorprendente in cui alcuni batteri reagiscono: costruendo enormi anelli molecolari che rilevano i fagi in arrivo e poi spengono deliberatamente la cellula infetta dall’interno. Il lavoro non solo rivela una forma ingegnosa di autodifesa batterica, ma riecheggia anche strategie usate dal nostro sistema immunitario innato, suggerendo temi profondi e comuni su come gli organismi rilevano e arrestano le infezioni.
Un piccolo guardiano con doppia vita
Il articolo si concentra su una proteina batterica che gli autori rinominano RAZR, presente in Escherichia coli e in molte altre specie. Da sola, RAZR è innocua: le cellule possono produrla a livelli elevati senza effetti negativi. Tuttavia, quando certi fagi infettano, RAZR diventa improvvisamente letale — sia per la cellula ospite sia per il virus. Il sistema agisce tramite un’“infezione abortiva”: una volta che RAZR viene attivata, il batterio infetto smette di crescere e si sacrifica efficacemente, impedendo al virus di produrre nuove copie e di diffondersi nella popolazione. Capire come RAZR sappia quando passare da spettatore silenzioso a esecutore cellulare è la questione centrale dello studio. 
Anelli virali che azionano l’interruttore
I ricercatori hanno scoperto che RAZR viene attivata da proteine specifiche prodotte da diversi fagi non correlati. In un fagò, una proteina chiamata Gp77 — probabilmente coinvolta nella riparazione o circolarizzazione del genoma virale — fungeva da innesco. In altri fagi, gli inneschi erano proteine “portal” che si trovano in un punto chiave del guscio virale e aiutano a iniettare il DNA nell’ospite. Sebbene queste proteine appaiano molto diverse nella sequenza e nella forma come molecole singole, condividono tutte una caratteristica notevole: si assemblano in grandi anelli di diametro quasi identico. Tramite crio-microscopia elettronica, il team ha mostrato che Gp77 forma un anello a 24 componenti, mentre le proteine portal formano anelli a 12 componenti. RAZR, che normalmente forma catene lineari sciolte, si avvolge attorno a questi anelli virali per costruire un enorme complesso circolare multistrato di oltre 25 nanometri di diametro.
Costruire un dispositivo molecolare dell’apocalisse
All’interno di questo complesso, RAZR mette insieme due regioni funzionali: un “sensore” a dito di zinco che afferra l’anello virale e una “lama” HEPN che taglia l’RNA. Due segmenti a dito di zinco di molecole RAZR adiacenti legano ciascuna unità proteica virale, garantendo che RAZR rivesta l’anello in modo preciso e altamente cooperativo. Questo impalcatura ad anello costringe i domini tagliatori di RNA di RAZR in un assetto curvo e compatto, permettendo a molti siti di taglio di allinearsi sul bordo esterno come denti di una sega circolare. Mutazioni che interrompono le superfici di contatto tra RAZR e le proteine fagiche, o che indeboliscono l’adesione tra molecole RAZR, compromettono la difesa. Un piccolo collegamento flessibile che congiunge le parti sensoriale e catalitica di RAZR si rivela anch’esso essenziale, aiutando la proteina ad assumere la geometria corretta quando abbraccia l’anello virale.
Fare a pezzi l’RNA per arrestare la diffusione virale
Una volta assemblata sul suo impalcatura prodotta dal fago, RAZR si trasforma in una potente macchina distruttrice di RNA. Gli autori dimostrano che RAZR attivata lascia intatto il DNA ma taglia molti tipi di RNA a singolo filamento: transfer RNA, RNA ribosomiale e RNA messaggeri sia del batterio sia del fagò infettante. Nelle cellule vive, questa vasta scissione dell’RNA blocca rapidamente la produzione proteica pur lasciando in gran parte intatte la replicazione del DNA e la trascrizione. In esperimenti in vitro, miscelare RAZR purificata con i suoi inneschi virali è sufficiente a fermare bruscamente la sintesi proteica. Interrompendo la traduzione in questo modo netto e non specifico, il sistema condanna la cellula infetta ma allo stesso tempo priva il fago degli strumenti molecolari necessari per riprodursi. 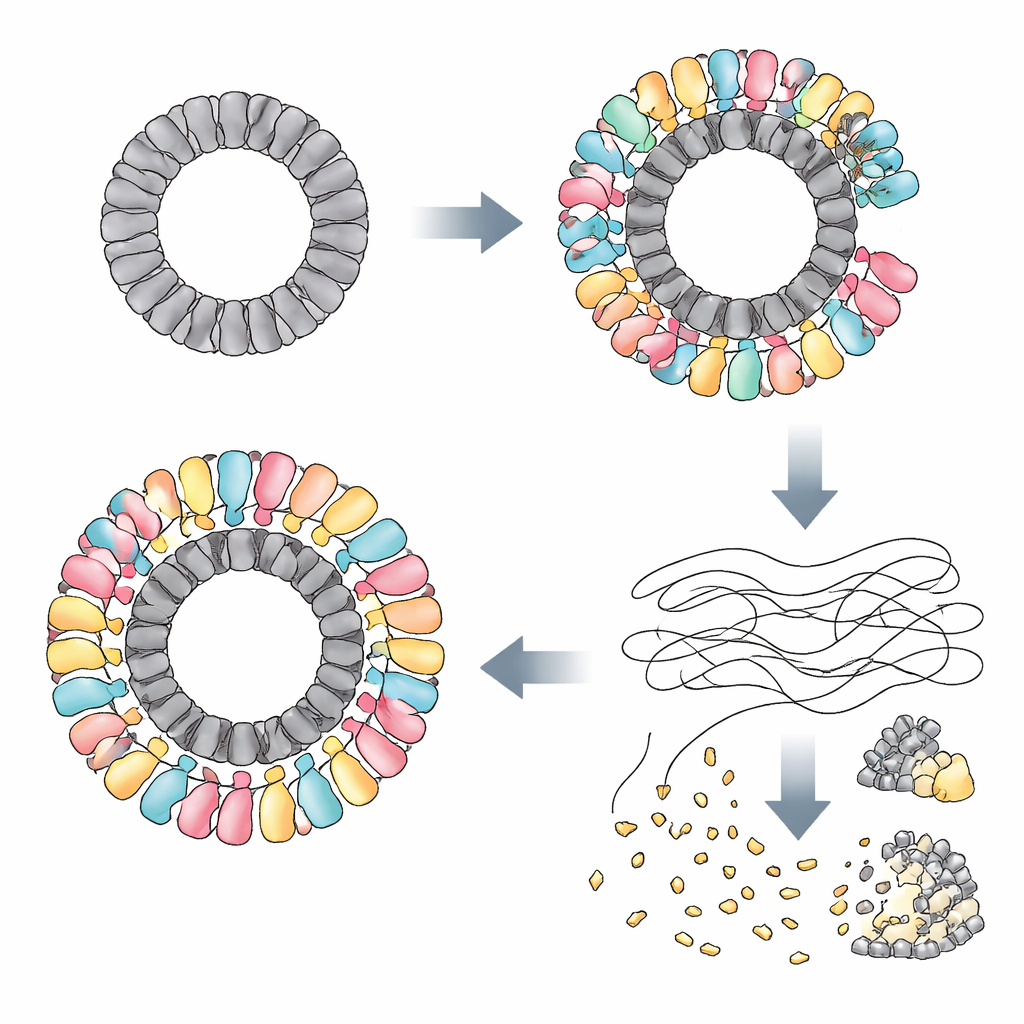
Adattare la difesa a virus diversi
Sebbene le proteine RAZR di batteri diversi condividano un dominio tagliente simile, lo studio trova che i loro sensori a dito di zinco variano ampiamente. Scambiando questi segmenti sensoriali tra due versioni di RAZR, da E. coli e Klebsiella variicola, si cambia in larga misura anche l’elenco dei fagi che possono bloccare. Anche quando due varianti di RAZR prendono di mira lo stesso fagò, si basano su punti di contatto leggermente diversi sulla proteina portal virale, come mostrano distinte mutazioni virali di fuga. Ciò suggerisce che i batteri possono regolare finemente il loro raggio antivirale evolvendo la porzione sensoriale di RAZR, mantenendo però intatta la potente macchina di taglio dell’RNA.
Idee condivise attraverso l’albero della vita
In conclusione, gli autori propongono che RAZR non riconosca una “password” virale specifica ma una firma strutturale: grandi anelli proteici di una certa dimensione che compaiono solo durante l’infezione da fagi e sono assenti dalla macchina della cellula ospite. Avvolgendosi attorno a questi anelli e usandoli come stampi per il proprio assemblaggio, RAZR amplifica un segnale virale debole in una risposta immunitaria tutto-o-nulla. Questa strategia rispecchia da vicino il modo in cui molti complessi immunitari innati negli animali, compresi gli esseri umani, formano grandi strutture filamentose o ad anello per rilevare i patogeni e attivare enzimi distruttivi. Il lavoro rivela così una convergenza sorprendente: dai batteri ai mammiferi, la vita ha evoluto ripetutamente modi per costruire enormi strutture proteiche che voltano la geometria dei virus invasori contro di loro.
Citazione: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Parole chiave: immunità da batteriofagi, difesa innata batterica, complesso proteico supramolecolare, scissione dell'RNA, sistema RAZR