Clear Sky Science · he
הפעלה חיסונית חיידקית באמצעות הרכבה סופראמולקולרית עם פאג שמפעילה
כיצד חיידקים מפתיעים את פולשיהם הויראליים
חיידקים נרדפים כל הזמן על ידי וירוסים שנקראים פאגים, שיכולים להפוך קהילה מיקרוביאלית משגשגת לבית קברות בתוך דקות. המחקר חושף דרך מפתיעה שבה חלק מהחיידקים מתגוננים: הם בונים טבעות מולקולריות ענקיות החושות פאגים פולשים ואז מכבות במודע את התא הנגוע מבפנים. העבודה מציגה לא רק צורה חכמה של הגנה עצמית חיידקית, אלא גם מהדהדת אסטרטגיות שמשתמש בהן המערכת החיסונית המולדת שלנו, ומרמזת על מוטיבים משותפים עמוקים באופן שבו החיים מזהים ומעצרים זיהומים.
שומר זעיר עם כפילות תפקידים
המאמר מתמקד בחלבון חיידקי שהמחברים קוראים לו RAZR, שנמצא בEscherichia coli ובמינים רבים אחרים. לבדו RAZR אינו מזיק: תאים יכולים לייצר אותו ברמות גבוהות ללא השפעות מזיקות. אך כאשר פאגים מסוימים תוקפים, RAZR פתאום נעשה קטלני — גם כלפי התא המארח וגם כלפי הווירוס. המערכת פועלת באמצעות "הדבקה נכשלת" (abortive infection): ברגע ש־RAZR מופעל, החיידק הנגוע מפסיק לגדול ומקריב את עצמו ביעילות, ובכך מונע מהווירוס להעתיק את עצמו ולהתפשט באוכלוסייה. הבנת האופן שבו RAZR מזהה מתי לעבור מתפקיד הצופה השקט לרוצח תאי היא שאלת המפתח של המחקר. 
טבעות ויראליות שמדליקות את המתג
החוקרים גילו ש־RAZR מופעל על ידי חלבונים ספציפיים שיוצרים מספר פאגים בלתי קשורים. באחד הפאגים, חלבון בשם Gp77 — שסביר שהיה מעורב בתיקון או בסיבוב של הגנום הויראלי — שימש כטריגר. בפאגים אחרים הטריגרים היו חלבוני "שער" (portal) שנמצאים בשער מפתח בקופסת הוירוס ועוזרים להזריק DNA אל התא המארח. למרות שחלבונים אלה נראים שונים מאוד ברצף ובצורה כמולקולות יחידניות, יש להם תכונה בולטת משותפת: הם מתארגנים לטבעות גדולות בקוטר כמעט זהה. באמצעות קריו־מיקרוסקופ אלקטרונים, הצוות הראה ש־Gp77 יוצר טבעת בת 24 חלקים, וחלבוני השער יוצרים טבעות בת 12 חלקים. RAZR, שבמצב רגיל יוצר שרשרות לינאריות רפויות, כרוך סביב טבעות ויראליות אלה כדי לבנות קומפלקס מעגלי רב־שכבתי ומאסיבי ברוחב של יותר מ־25 ננומטר.
בניית "מכשיר יום הדין" מולקולרי
בתוך קומפלקס זה, RAZR מאחד שני אזורים פונקציונליים: חיישן בצורת "אצבע אבץ" שמחזיק את הטבעת הויראלית, ו"להב" HEPN שמחתך RNA. שני מקטעי אצבע אבץ משתי מולקולות RAZR שכנות נקשרים לכל יחידת חלבון ויראלית, ובכך מבטיחים ש־RAZR מצפה את הטבעת בצורה מדויקת ושיתופית מאוד. התבנית המעגלית הזו מאלצת את דומייני חיתוך ה־RNA של RAZR לסדר מעוקל וצפוף, מה שמאפשר לאתרים רבים לחתוך להימצא על הקצה החיצוני כמו שיניים על מסור מעגלי. מוטציות ההורסות את משטחי המגע בין RAZR לחלבוני הפאג, או שמחלישות את האופן שבו מולקולות RAZR נדבקות זו לזו, משתקות את ההגנה. מקשר גמיש קטן שמחבר בין חלק החישה לחלק החיתוך של RAZR גם הוא חיוני, והוא עוזר לחלבון לאמץ את הגאומטריה הנכונה כשהוא מחבק את טבעת הוירוס.
קריעת RNA כדי לעצור את התפשטות הווירוס
ברגע שמתאסף על התבנית שמייצר הפאג, RAZR הופך למכונה הרסנית למחיקה של RNA. המחברים מראים ש־RAZR המופעל משאיר את ה־DNA ללא פגע אך חותך סוגים רבים של RNA חד־גדילי: tRNA, rRNA ו־mRNA הן של החיידק והן של הפאג התוקף. בתאים חיים, חיתוך נרחב זה של RNA חוסם במהירות את ייצור החלבונים בעוד שהעתקת ה־DNA והטרנסקריפציה נשארות ברובן תקינות. בניסויי מבחנה, ערבוב RAZR מזוקק עם הטריגרים הויראליים שלו מספיק כדי לעצור את התרגום לחלוטין. בעזרת עצירת התרגום בדרך ברוטלית ולא ספציפית זו, המערכת מגלה את גורל התא הנגוע אך גם מרעיבה את הפאג מכלים המולקולריים הדרושים לו לשכפול. 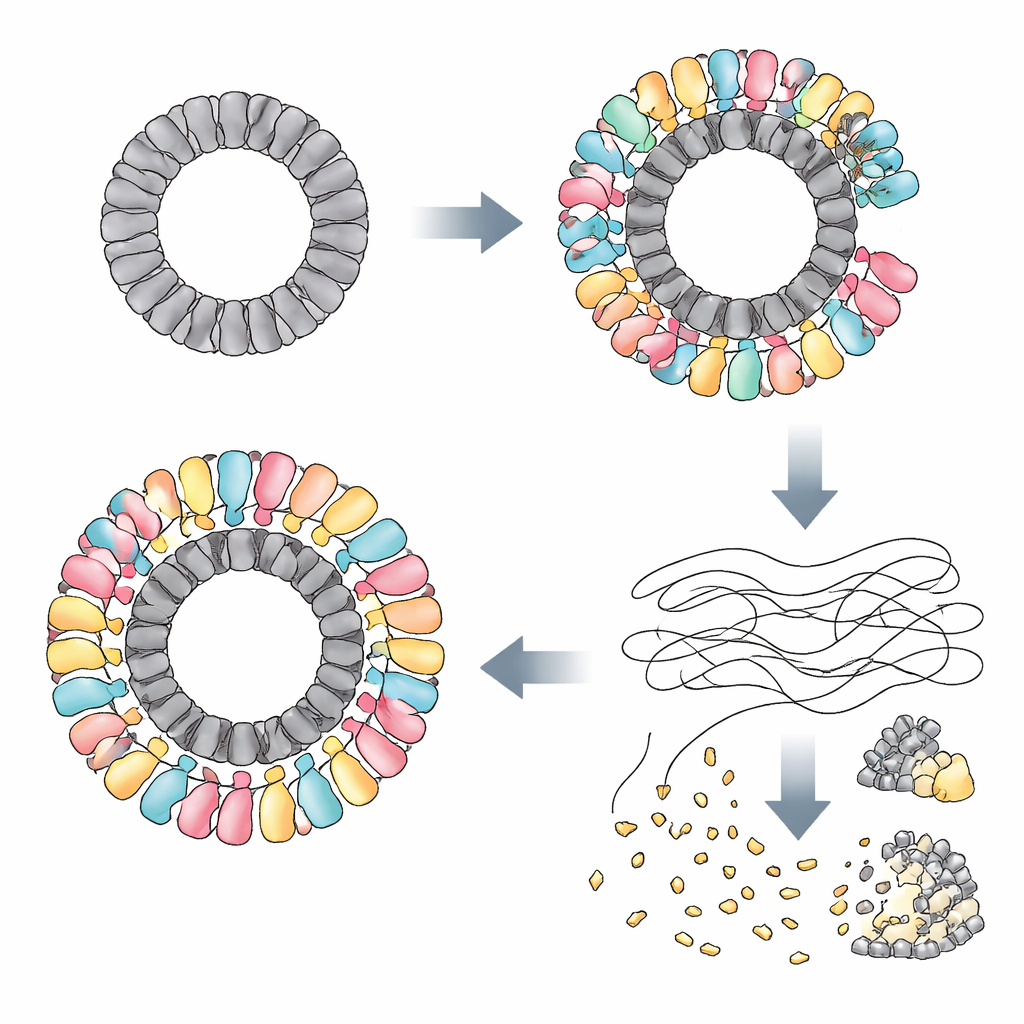
התאמת ההגנה לוירוסים שונים
למרות שלחלבוני RAZR ממקורות חיידקיים שונים יש דומיין חיתוך דומה, המחקר מראה שחיישני אצבע האבץ שלהם משתנים במידה רבה. החלפת מקטעי החיישן האלה בין שתי גרסאות RAZR, מאי־קולי ו־Klebsiella variicola, משנה במידה רבה אילו פאגים הן יכולות לעצור. אפילו כאשר שתי וריאנטים של RAZR פוגעות באותו פאג, הן תלויות בנקודות מגע שונות במקצת על חלבון השער הויראלי, כפי שמודגם במוטציות בריחה ויראליות שונות. ממצא זה מציע שחיידקים יכולים לכוונן את טווח האנטי־ויראליות שלהם על ידי אבולוציה של חלק החיישן ב־RAZR, בעוד שמכונת חיתוך ה־RNA העוצמתית נשארת שלמה.
רעיונות משותפים ברחבי מעץ החיים
בסופו של דבר, המחברים מציעים ש־RAZR לא מזהה "סיסמת" וירוס ספציפית אלא חתימה מבנית: טבעות חלבוניות גדולות בגודל מסוים שמופיעות רק במהלך זיהום על־ידי פאג ונעדרות ממכונותיו של המארח. על ידי כריכה סביב טבעות אלה ושימוש בהן כתבניות להרכבה משלה, RAZR ממגבר איתות ויראלי חלש לתגובה חיסונית דיכוטומית — הכל או כלום. אסטרטגיה זו משקפת באופן הדוק כיצד קומפלקסים רבים של המערכת המולדת בחיות, כולל בני אדם, יוצרים מבנים גדולים פתיליים או מעגליים כדי לזהות פתוגנים ולהפעיל אנזימים הרסניים. העבודה חושפת אפוא התכנסות מרשימה: מחיידקים עד יונקים, החיים פיתחו שוב ושוב דרכים לבנות מבני חלבון ענקיים שהופכים את הגאומטריה של הווירוסים הפולשים נגדם.
ציטוט: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
מילות מפתח: חיסון בבקטריופאג׳, הגנה מולדת חיידקית, קומפלקס חלבוני סופראמולקולרי, חיתוך RNA, מערכת RAZR