Clear Sky Science · ru
Активация бактериального иммунитета посредством супрамолекулярной сборки с фагом
Как бактерии перехитривают своих вирусных захватчиков
Бактерии постоянно подвергаются нападению вирусов, называемых фагами, которые могут за считанные минуты превратить процветающее микробное сообщество в пустыню. В этом исследовании раскрыт неожиданный механизм, которым некоторые бактерии дают отпор: они строят огромные молекулярные кольца, которые распознают вторжение фага и затем целенаправленно выключают заражённую клетку изнутри. Работа не только выявляет хитрую форму бактериальной самообороны, но и отзывается к стратегиям нашего врождённого иммунитета, указывая на глубинные общие принципы в обнаружении и остановке инфекций.
Крошечный страж с двойной ролью
Статья сосредоточена на бактериальном белке, который авторы переименовывают в RAZR, найденном в Escherichia coli и во многих других видах. Сам по себе RAZR безвреден: клетки могут продуцировать его в больших количествах без вредных последствий. Однако при инфекции некоторыми фагами RAZR внезапно становится смертоносным — как для хозяина, так и для вируса. Система действует через «абортивную инфекцию»: как только RAZR включается, заражённый бактериальный организм прекращает рост и фактически жертвует собой, не давая вирусу размножаться и распространяться по популяции. Понимание того, как RAZR узнаёт, когда перейти от тихого наблюдателя к исполнителю в клетке, — центральный вопрос исследования. 
Вирусные кольца, которые переключают систему
Исследователи обнаружили, что RAZR активируется специфическими белками, производимыми несколькими неродственными фагами. У одного фага белок под названием Gp77 — предположительно участвующий в ремонте или циркуляризации вирусного генома — оказался триггером. У других фагов триггерами выступали «портальные» белки, расположенные в ключевом шлюзе вирусной оболочки и помогающие вводить ДНК в хозяина. Хотя эти белки как отдельные молекулы сильно различаются по последовательности и форме, у них есть одна поразительная общая черта: они собираются в крупные кольца практически одинакового диаметра. С помощью крио-электронной микроскопии команда показала, что Gp77 образует кольцо из 24 частей, а портальные белки — из 12 частей. RAZR, который в покое образует рыхлые линейные цепочки, обвивает эти вирусные кольца, собирая массивный многослойный круглый комплекс диаметром более 25 нанометров.
Создание молекулярного устройства Судного дня
Внутри этого комплекса RAZR объединяет две функциональные области: цинк-пальцевый «датчик», который захватывает вирусное кольцо, и HEPN «лезвие», которое разрезает РНК. Два цинк-пальцевых сегмента соседних молекул RAZR связываются с каждым белковым модулем вируса, обеспечивая точное и высококооперативное покрытие кольца RAZR. Эта кольцевая опора заставляет РНК-резаки RAZR принять изогнутую, тесно упакованную конфигурацию, позволяя множеству режущих сайтов выстроиться по наружному краю подобно зубьям циркулярной пилы. Мутации, разрушающие контактные поверхности между RAZR и белками фага или ослабляющие взаимодействие между самими молекулами RAZR, парализуют защиту. Небольшой гибкий линкер, соединяющий сенсорную и режущую части RAZR, также оказывается жизненно важным, помогая белку принять нужную геометрию при облегании вирусного кольца.
Измельчение РНК, чтобы остановить распространение вируса
После сборки на вирусном остове RAZR превращается в мощную машину по разрушению РНК. Авторы показывают, что активированный RAZR не затрагивает ДНК, но расщепляет многие типы одноцепочечной РНК: транспортные РНК, рибосомные РНК и матричные РНК как бактерии, так и вторгшегося фага. В живых клетках такое широкомасштабное расщепление РНК быстро блокирует синтез белка, оставляя при этом репликацию ДНК и транскрипцию в основном нетронутыми. В экспериментах в пробирке смешение очищенного RAZR с его вирусными триггерами достаточно, чтобы надолго остановить синтез белка. Путём грубой неспецифичной остановки трансляции система приговаривает заражённую клетку и одновременно лишает фаг молекулярных инструментов, необходимых для размножения. 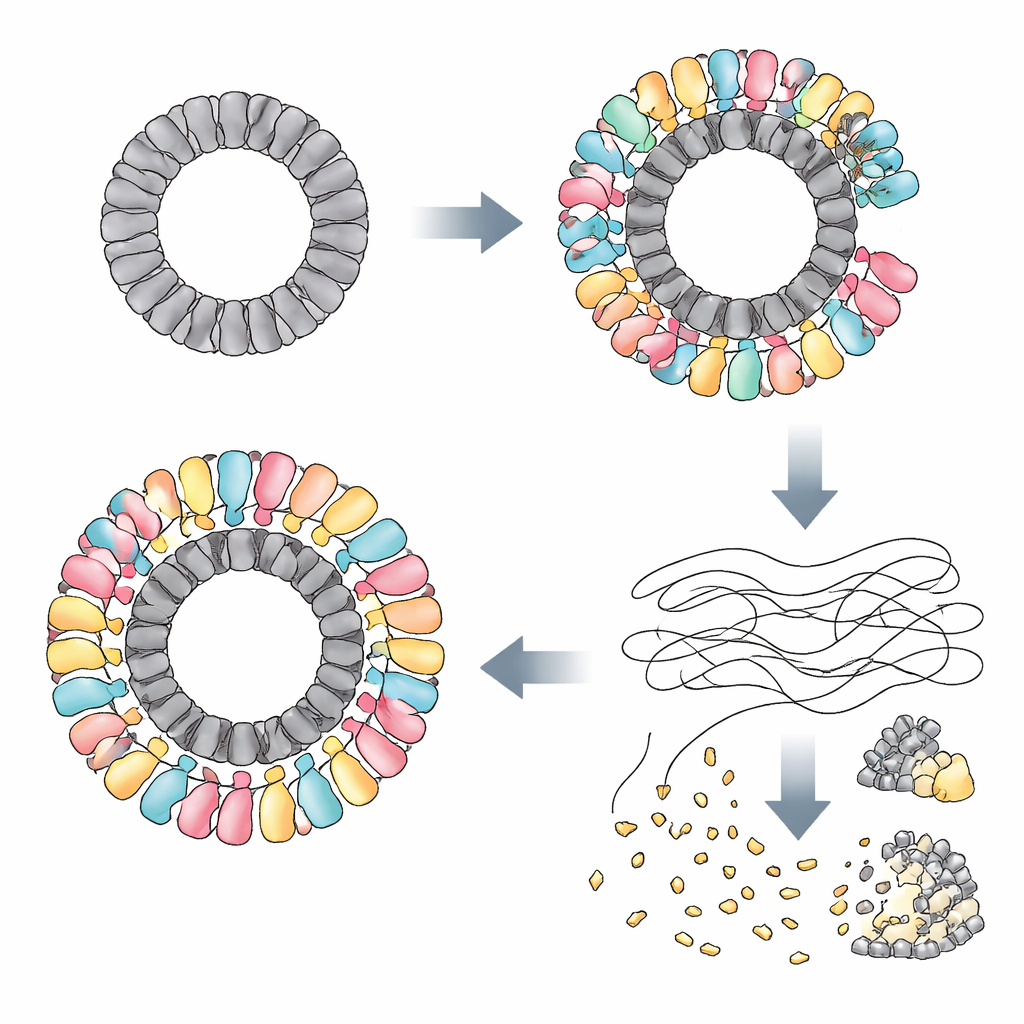
Адаптация обороны к разным вирусам
Хотя у белков RAZR из разных бактерий сходна режущая домен, исследование показывает, что их цинк-пальцевые сенсоры сильно различаются. Замена этих сенсорных сегментов между двумя версиями RAZR из E. coli и Klebsiella variicola по сути переставляет спектр фагов, которые они могут остановить. Даже если две версии RAZR нацелены на одного и того же фага, они опираются на слегка разные контактные точки на портальном белке вируса, что видно по различающимся мутациям вируса, обеспечивающим побег. Это указывает на то, что бактерии могут тонко настраивать свой антивирусный диапазон, эволюционируя сенсорную часть RAZR, сохраняя при этом мощный механизм расщепления РНК.
Общие идеи по всему дереву жизни
В конечном счёте авторы предлагают, что RAZR распознаёт не конкретный вирусный «пароль», а структурную сигнатуру: большие белковые кольца определённого размера, которые появляются только при фаговой инфекции и отсутствуют в собственных машинах хозяина. Обвивая эти кольца и используя их как шаблоны для собственной сборки, RAZR усиливает слабый вирусный сигнал до реакции «всё или ничего». Эта стратегия тесно перекликается с тем, как многие комплексы врождённого иммунитета у животных, включая человека, формируют гигантские филаментозные или кольцеобразные структуры для обнаружения патогенов и активации деструктивных ферментов. Работа таким образом выявляет поразительное сближение: от бактерий до млекопитающих жизнь многократно развивала способы строить крупные белковые структуры, превращая геометрию вторгающихся вирусов против них самих.
Цитирование: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Ключевые слова: иммунитет к бактериофагам, внутренние защитные механизмы бактерий, супрамолекулярный белковый комплекс, расщепление РНК, система RAZR