Clear Sky Science · pt
Ativação imune bacteriana via montagem supramolecular com fagos desencadeia resposta
Como as bactérias ludibriam seus invasores virais
As bactérias são constantemente caçadas por vírus chamados fagos, que podem transformar uma comunidade microbiana próspera em um cemitério em questão de minutos. Este estudo revela uma maneira surpreendente pela qual algumas bactérias reagem: construindo enormes anéis moleculares que detectam fagos invasores e então deliberadamente desativam a célula infectada por dentro. O trabalho não só revela uma forma engenhosa de autodefesa bacteriana, como também ecoa estratégias utilizadas pelo nosso próprio sistema imune inato, sugerindo temas comuns profundos sobre como a vida detecta e interrompe infecções.
Um pequeno guardião com dupla vida
O artigo foca em uma proteína bacteriana que os autores renomeiam RAZR, encontrada em Escherichia coli e em muitas outras espécies. Sozinha, a RAZR é inofensiva: as células podem produzi‑la em altos níveis sem efeitos adversos. No entanto, quando certos fagos infectam, a RAZR de repente se torna letal — tanto para a célula hospedeira quanto para o vírus. O sistema atua por meio de “infecção abortiva”: uma vez que a RAZR é ativada, a bactéria infectada para de crescer e efetivamente se sacrifica, impedindo o fago de fabricar mais cópias e se espalhar pela população. Entender como a RAZR sabe quando mudar de espectadora silenciosa para algoz celular é a questão central do estudo. 
Anéis virais que acionam a chave
Os pesquisadores descobriram que a RAZR é ativada por proteínas específicas produzidas por vários fagos não relacionados. Em um fago, uma proteína chamada Gp77 — provavelmente envolvida na reparação ou circularização do genoma viral — serviu como gatilho. Em outros fagos, os gatilhos foram proteínas “portal” que se situam em um ponto de passagem chave na cápside viral e ajudam a injetar o DNA no hospedeiro. Embora essas proteínas pareçam muito diferentes em sequência e forma como moléculas individuais, todas compartilham uma característica marcante: elas se montam em grandes anéis de diâmetro quase idêntico. Usando criomicroscopia eletrônica, a equipe mostrou que Gp77 forma um anel de 24 partes, e que as proteínas portal formam anéis de 12 partes. A RAZR, que normalmente forma cadeias lineares frouxas, envolve esses anéis virais para construir um complexo circular massivo e em múltiplas camadas com mais de 25 nanômetros de diâmetro.
Construindo um dispositivo molecular do juízo final
Dentro desse complexo, a RAZR reúne duas regiões funcionais: um “sensor” com dedo de zinco que agarra o anel viral, e uma “lâmina” HEPN que corta RNA. Dois segmentos de dedo de zinco de moléculas RAZR vizinhas ligam cada unidade da proteína viral, assegurando que a RAZR cubra o anel de maneira precisa e altamente cooperativa. Essa estrutura em forma de anel força os domínios cortadores de RNA da RAZR a adotarem um arranjo curvado e compactado, permitindo que muitos sítios de corte se alinhem na borda externa como dentes de uma serra circular. Mutations que perturbam as superfícies de contato entre RAZR e as proteínas do fago, ou que enfraquecem a forma como as moléculas RAZR se aderem umas às outras, comprometem a defesa. Um pequeno conector flexível que liga as partes de detecção e corte da RAZR também se mostra essencial, ajudando a proteína a assumir a geometria correta quando abraça o anel viral.
Despedaçando RNA para interromper a disseminação viral
Uma vez montada em seu andaime feito pelo fago, a RAZR se transforma em uma poderosa máquina destruidora de RNA. Os autores mostram que a RAZR ativada deixa o DNA intacto, mas fatia muitos tipos de RNA de fita simples: RNAs de transferência, RNAs ribossomais e RNAs mensageiros tanto da bactéria quanto do fago infectante. Em células vivas, essa clivagem generalizada de RNA bloqueia rapidamente a produção de proteínas enquanto deixa a replicação e a transcrição do DNA em grande parte intactas. Em experimentos em tubo de ensaio, misturar RAZR purificada com seus gatilhos virais é suficiente para deter completamente a síntese de proteínas. Ao paralisar a tradução de forma contundente e não específica, o sistema condena a célula infectada, mas também priva o fago das ferramentas moleculares necessárias para se reproduzir. 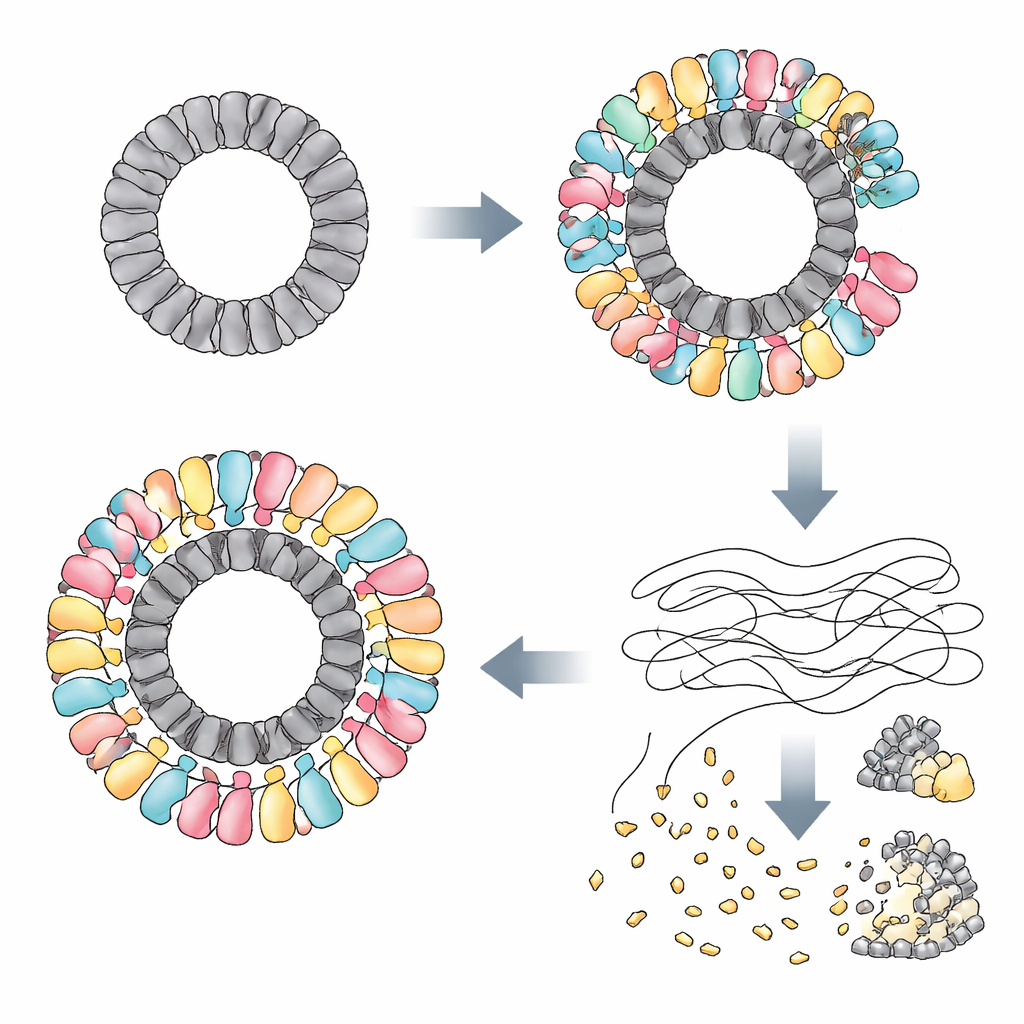
Adaptando a defesa a diferentes vírus
Embora proteínas RAZR de bactérias diferentes compartilhem um domínio de corte semelhante, o estudo mostra que seus sensores de dedo de zinco variam amplamente. Trocar esses segmentos sensores entre duas versões de RAZR, de E. coli e Klebsiella variicola, basicamente troca quais fagos elas conseguem deter. Mesmo quando duas variantes de RAZR miram o mesmo fago, elas dependem de pontos de contato ligeiramente diferentes na proteína portal viral, como demonstrado por distintas mutações de escape viral. Isso sugere que as bactérias podem ajustar finamente seu alcance antiviral evoluindo a porção sensor da RAZR, enquanto mantêm intacta a poderosa maquinaria de corte de RNA.
Ideias compartilhadas através da árvore da vida
No fim, os autores propõem que a RAZR não detecta uma “senha” viral específica, mas sim uma assinatura estrutural: grandes anéis proteicos de um tamanho particular que aparecem apenas durante a infecção por fagos e estão ausentes da própria maquinaria do hospedeiro. Ao envolver esses anéis e usá‑los como moldes para sua própria montagem, a RAZR amplifica um sinal viral fraco em uma resposta imune do tipo tudo ou nada. Essa estratégia espelha de perto como muitos complexos imunes inatos em animais, incluindo humanos, formam grandes montagens filamentosas ou em forma de anel para detectar patógenos e ativar enzimas destrutivas. O trabalho, assim, revela uma convergência impressionante: de bactérias a mamíferos, a vida evoluiu reiteradamente maneiras de construir enormes estruturas proteicas que voltam a geometria dos vírus invasores contra eles.
Citação: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Palavras-chave: imunidade a bacteriófagos, defesa inata bacteriana, complexo proteico supramolecular, clivagem de RNA, sistema RAZR