Clear Sky Science · de
Bakterielle Immunaktivierung durch supramolekulare Assemblierung mit Phagen als Auslöser
Wie Bakterien ihre viralen Eindringlinge überlisten
Bakterien werden ständig von Viren, sogenannten Phagen, gejagt, die eine blühende mikrobielle Gemeinschaft innerhalb von Minuten in ein Ödland verwandeln können. Diese Studie enthüllt eine überraschend neue Art, wie einige Bakterien zurückschlagen: indem sie riesige molekulare Ringe bauen, die eingehende Phagen erkennen und dann gezielt die infizierte Zelle von innen stilllegen. Die Arbeit zeigt nicht nur eine clevere Form bakterieller Selbstverteidigung, sondern spiegelt auch Strategien unseres eigenen angeborenen Immunsystems wider und deutet auf tief liegende gemeinsame Prinzipien darin hin, wie Leben Infektionen erkennt und stoppt.
Ein winziger Wächter mit Doppelleben
Die Arbeit konzentriert sich auf ein bakterielles Protein, das die Autoren RAZR nennen, und das in Escherichia coli und vielen anderen Arten vorkommt. Für sich allein ist RAZR harmlos: Zellen können es in hohen Mengen produzieren, ohne Schaden zu nehmen. Wenn jedoch bestimmte Phagen einbrechen, wird RAZR plötzlich tödlich — sowohl für die Wirtszelle als auch für das Virus. Das System wirkt über „aborted infection“ (abgebrochene Infektion): Sobald RAZR aktiviert ist, stoppt das infizierte Bakterium sein Wachstum und opfert sich effektiv, wodurch das Virus daran gehindert wird, neue Kopien zu erzeugen und sich in der Population auszubreiten. Zu verstehen, wie RAZR weiß, wann es vom stillen Beobachter zum zellulären Vollstrecker wird, ist die zentrale Frage der Studie. 
Virale Ringe, die den Schalter umlegen
Die Forscher entdeckten, dass RAZR durch spezifische Proteine aktiviert wird, die von mehreren nicht verwandten Phagen hergestellt werden. Bei einem Phagen diente ein Protein namens Gp77 — wahrscheinlich beteiligt an der Reparatur oder Zirkularisierung des viralen Genoms — als Auslöser. Bei anderen Phagen waren die Auslöser „Portal“-Proteine, die an einem wichtigen Tor in der Virushülle sitzen und beim Einspritzen der DNA in den Wirt helfen. Obwohl diese Proteine in Sequenz und Form als einzelne Moleküle sehr unterschiedlich aussehen, teilen sie alle ein auffälliges Merkmal: Sie assemblieren sich zu großen Ringen nahezu gleicher Durchmesser. Mithilfe der Kryo-Elektronenmikroskopie zeigte das Team, dass Gp77 einen 24-teiligen Ring bildet und dass Portalproteine 12-teilige Ringe bilden. RAZR, das normalerweise lockere lineare Ketten bildet, schlingt sich um diese viralen Ringe und baut so einen massiven, mehrlagigen Kreisverbund von mehr als 25 Nanometern Durchmesser.
Ein molekularer Weltuntergangsapparat entsteht
Innerhalb dieses Komplexes vereint RAZR zwei funktionelle Bereiche: einen Zinkfinger-„Sensor“, der am viralen Ring ansetzt, und eine HEPN‑„Klinge“, die RNA schneidet. Zwei Zinkfingersegmente benachbarter RAZR‑Moleküle binden jeweils eine Einheit des viralen Proteins und sorgen dafür, dass RAZR den Ring präzise und hochkooperativ überzieht. Dieses ringförmige Gerüst zwingt die RNA-schneidenden Domänen von RAZR in eine gekrümmte, dicht gepackte Anordnung, sodass viele Schnittstellen wie Zähne an einer Kreissäge am äußeren Rand aufgereiht sind. Mutationen, die die Kontaktflächen zwischen RAZR und den Phagenproteinen stören oder die Haftung der RAZR‑Moleküle untereinander abschwächen, schwächen die Abwehr. Ein kleiner flexibler Linker, der die Sensor- und Schneidedomänen von RAZR verbindet, erweist sich ebenfalls als essentiell, da er dem Protein hilft, die richtige Geometrie einzunehmen, wenn es den viralen Ring umschließt.
RNA zerfetzen, um die Virusverbreitung zu stoppen
Sobald es auf seinem phagengebauten Gerüst zusammengesetzt ist, verwandelt sich RAZR in eine kraftvolle RNA‑vernichtende Maschine. Die Autoren zeigen, dass aktiviertes RAZR die DNA unberührt lässt, aber viele Arten einzelsträngiger RNA zerschneidet: Transfer‑RNAs, ribosomale RNAs und messenger‑RNAs sowohl des Bakteriums als auch des eingreifenden Phagen. In lebenden Zellen blockiert diese weitreichende RNA‑Spaltung rasch die Proteinproduktion, während DNA‑Replikation und Transkription weitgehend intakt bleiben. In Versuchsröhrchen reicht das Mischen von gereinigtem RAZR mit seinen viralen Auslösern aus, um die Proteinsynthese vollständig zu stoppen. Indem die Translation auf diese grobe, unspezifische Weise zum Erliegen gebracht wird, opfert das System die infizierte Zelle, beraubt aber zugleich den Phagen der molekularen Werkzeuge, die er zur Reproduktion benötigt. 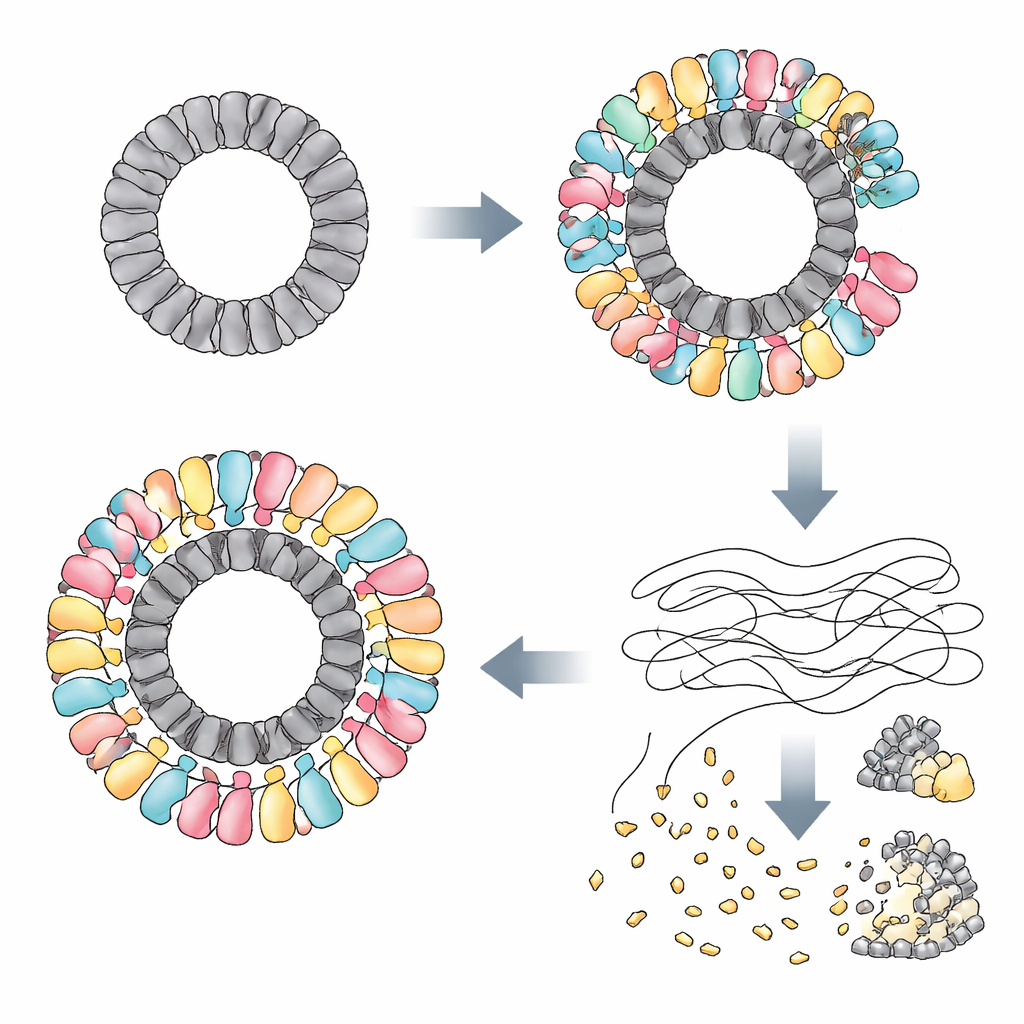
Abwehr an verschiedene Viren anpassen
Obwohl RAZR‑Proteine aus verschiedenen Bakterien eine ähnliche Schneidedomäne teilen, zeigt die Studie, dass ihre Zinkfinger‑Sensoren stark variieren. Das Austauschen dieser Sensorsegmente zwischen zwei RAZR‑Varianten aus E. coli und Klebsiella variicola verändert weitgehend, welche Phagen sie stoppen können. Selbst wenn zwei RAZR‑Varianten denselben Phagen anvisieren, stützen sie sich auf leicht unterschiedliche Kontaktstellen am viralen Portalprotein, wie durch unterschiedliche virale Fluchtmutationen gezeigt wird. Das legt nahe, dass Bakterien ihren antiviralen Wirkungsbereich feinabstimmen können, indem sie den Sensoranteil von RAZR weiterentwickeln, während die leistungsfähige RNA‑Schneidemaschine erhalten bleibt.
Geteilte Ideen über den Lebensbaum hinweg
Am Ende schlagen die Autoren vor, dass RAZR kein spezifisches virales „Passwort“ erkennt, sondern eine strukturelle Signatur: große Proteinringe einer bestimmten Größe, die nur während einer Phageninfektion auftreten und im eigenen Apparat des Wirts fehlen. Indem RAZR sich um diese Ringe schlingt und sie als Vorlage für die eigene Assemblierung nutzt, verstärkt es ein schwaches virales Signal zu einer Alles‑oder‑Nichts‑Immunantwort. Diese Strategie spiegelt sehr stark wider, wie viele angeborene Immunkomplexe bei Tieren, einschließlich des Menschen, riesige filamentöse oder ringförmige Strukturen bilden, um Krankheitserreger zu erkennen und zerstörerische Enzyme zu aktivieren. Die Arbeit zeigt damit eine eindrucksvolle Konvergenz: Von Bakterien bis zu Säugetieren hat das Leben wiederholt Wege entwickelt, große Proteinstrukturen zu bauen, die die Geometrie eindringender Viren gegen sie selbst wenden.
Zitation: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Schlüsselwörter: Bakteriophage-Immunität, Bakterielle angeborene Abwehr, supramolekularer Proteinkomplex, RNA-Spaltung, RAZR-System