Clear Sky Science · es
Activación inmune bacteriana mediante ensamblaje supramolecular con fagos como desencadenante
Cómo las bacterias vencen a sus invasores virales
Las bacterias son constantemente acosadas por virus llamados fagos, que pueden convertir una comunidad microbiana próspera en un cementerio en cuestión de minutos. Este estudio descubre una forma sorprendente en que algunas bacterias se defienden: construyendo enormes anillos moleculares que detectan fagos entrantes y luego apagan deliberadamente la célula infectada desde dentro. El trabajo no solo revela una forma ingeniosa de autodefensa bacteriana, sino que también refleja estrategias usadas por nuestro propio sistema inmune innato, sugiriendo temas comunes profundos en cómo la vida detecta y detiene las infecciones.
Un pequeño guardián con doble vida
El artículo se centra en una proteína bacteriana que los autores renombraron RAZR, presente en Escherichia coli y muchas otras especies. Por sí sola, RAZR es inofensiva: las células pueden producirla en altos niveles sin efectos adversos. Sin embargo, cuando ciertos fagos infectan, RAZR se vuelve de repente letal—tanto para la célula hospedadora como para el virus. El sistema actúa mediante una “infección abortiva”: una vez que RAZR se activa, la bacteria infectada deja de crecer y se sacrifica efectivamente, impidiendo que el virus haga más copias y se propague por la población. Entender cómo RAZR sabe cuándo pasar de espectador silencioso a ejecutor celular es la cuestión central del estudio. 
Anillos virales que activan el interruptor
Los investigadores descubrieron que RAZR se activa por proteínas específicas fabricadas por varios fagos no relacionados. En un fago, una proteína llamada Gp77—probablemente implicada en reparar o circularizar el genoma viral—sirvió como el desencadenante. En otros fagos, los disparadores fueron proteínas “portal” que se sitúan en una puerta clave de la cápside viral y ayudan a inyectar el ADN en el hospedador. Aunque estas proteínas parecen muy diferentes en secuencia y forma como moléculas individuales, todas comparten una característica llamativa: se ensamblan en grandes anillos de diámetro casi idéntico. Mediante crio–microscopía electrónica, el equipo mostró que Gp77 forma un anillo de 24 subunidades, y que las proteínas portal forman anillos de 12 subunidades. RAZR, que normalmente forma cadenas lineales sueltas, se envuelve alrededor de estos anillos virales para construir un complejo circular masivo y multicapa de más de 25 nanómetros de diámetro.
Construyendo un dispositivo molecular del día del juicio
Dentro de este complejo, RAZR reúne dos regiones funcionales: un “sensor” con dedo de zinc que agarra el anillo viral, y una “cuchilla” HEPN que corta ARN. Dos segmentos de dedo de zinc de moléculas RAZR vecinas se unen a cada unidad proteica viral, asegurando que RAZR recubra el anillo de manera precisa y altamente cooperativa. Este andamiaje en forma de anillo fuerza a los dominios cortadores de ARN de RAZR a una disposición curva y compacta, permitiendo que muchos sitios de corte se alineen en el borde exterior como dientes de una sierra circular. Mutaciones que rompen las superficies de contacto entre RAZR y las proteínas del fago, o que debilitan la forma en que las moléculas RAZR se adhieren entre sí, incapacitan la defensa. Un pequeño enlace flexible que conecta las partes de detección y corte de RAZR también resulta esencial, ayudando a la proteína a adoptar la geometría adecuada cuando abraza el anillo viral.
Despedazando ARN para frenar la propagación viral
Una vez ensamblado sobre su andamiaje fabricado por el fago, RAZR se convierte en una potente máquina destructora de ARN. Los autores muestran que RAZR activado deja el ADN intacto pero corta muchos tipos de ARN monocatenario: ARN de transferencia, ARN ribosómicos y ARN mensajero tanto de la bacteria como del fago infectante. En células vivas, esta escisión generalizada de ARN bloquea rápidamente la producción de proteínas mientras deja en gran medida intactas la replicación del ADN y la transcripción. En experimentos de tubo de ensayo, mezclar RAZR purificado con sus desencadenantes virales es suficiente para detener la síntesis de proteínas de raíz. Al detener la traducción de manera contundente y no específica, el sistema condena a la célula infectada pero también priva al fago de las herramientas moleculares que necesita para reproducirse. 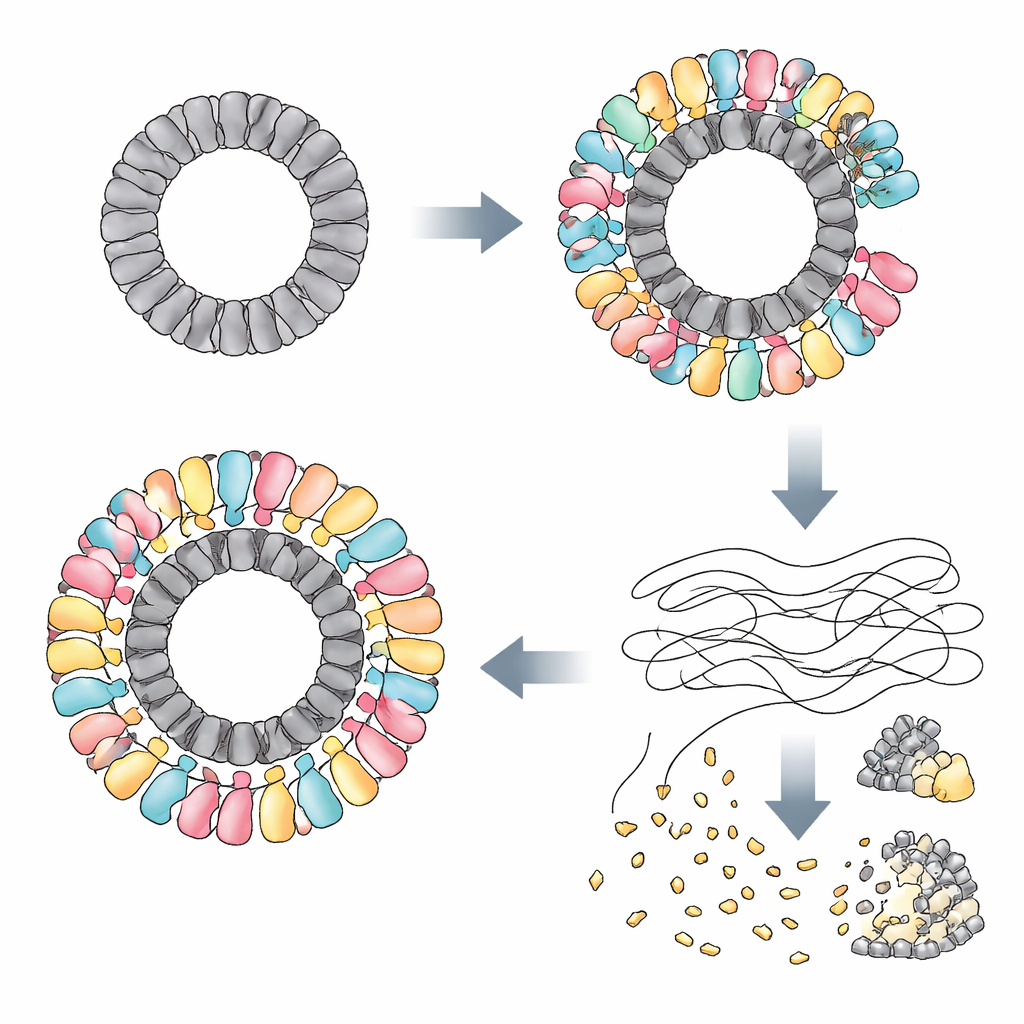
Adaptando la defensa a distintos virus
Aunque las proteínas RAZR de distintas bacterias comparten un dominio cortador similar, el estudio encuentra que sus sensores con dedo de zinc varían ampliamente. Intercambiar estos segmentos sensores entre dos variantes de RAZR, de E. coli y Klebsiella variicola, intercambia en gran medida qué fagos pueden detener. Incluso cuando dos variantes de RAZR atacan el mismo fago, dependen de puntos de contacto ligeramente distintos en la proteína portal viral, como muestran mutaciones virales de escape diferentes. Esto sugiere que las bacterias pueden afinar su rango antiviral evolucionando la porción sensor de RAZR, mientras mantienen intacta la poderosa maquinaria de corte de ARN.
Ideas compartidas a lo largo del árbol de la vida
Al final, los autores proponen que RAZR no detecta una “contraseña” viral específica sino una firma estructural: grandes anillos proteicos de un tamaño particular que aparecen solo durante la infección por fagos y están ausentes en la maquinaria propia del hospedador. Al envolverse alrededor de estos anillos y usarlos como plantillas para su propio ensamblaje, RAZR amplifica una señal viral débil hasta producir una respuesta inmune todo o nada. Esta estrategia refleja de cerca cómo muchos complejos inmunes innatos en animales, incluidos los humanos, forman ensamblajes gigantes filamentosos o en forma de anillo para detectar patógenos y activar enzimas destructivas. El trabajo revela así una convergencia notable: desde bacterias hasta mamíferos, la vida ha evolucionado repetidamente maneras de construir enormes estructuras proteicas que convierten la geometría de los virus invasores en su contra.
Cita: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Palabras clave: inmunidad frente a bacteriófagos, defensa innata bacteriana, complejo proteico supramolecular, corte de ARN, sistema RAZR