Clear Sky Science · pl
Aktywacja odporności bakterii poprzez supramolekularne zespoły z wyzwalaczami z fagów
Jak bakterie przechytrzają swoich wirusowych najeźdźców
Bakterie są nieustannie ścigane przez wirusy zwane fagami, które w ciągu kilku minut mogą przemienić kwitnącą społeczność mikrobiologiczną w pustkowie. To badanie odkrywa zaskakujący nowy sposób, w jaki niektóre bakterie się bronią: budują olbrzymie pierścienie molekularne, które wykrywają napływające fagi, a następnie świadomie wyłączają zainfekowaną komórkę od środka. Praca ta nie tylko ujawnia sprytną formę bakteryjnej samoobrony, lecz także przypomina strategie stosowane przez nasz własny układ odpornościowy wrodzony, sugerując głębokie wspólne motywy w tym, jak życie wykrywa i powstrzymuje infekcje.
Maleńki strażnik o podwójnym życiu
Artykuł koncentruje się na białku bakteryjnym, które autorzy przemianowują na RAZR, występującym w Escherichia coli i wielu innych gatunkach. Samo w sobie RAZR jest nieszkodliwe: komórki mogą produkować je w dużych ilościach bez negatywnych skutków. Jednak gdy niektóre fagi zakażają, RAZR nagle staje się zabójcze — zarówno dla komórki gospodarza, jak i dla wirusa. System działa poprzez „przedwczesne zakażenie” (abortive infection): po włączeniu RAZR zainfekowana bakteria przestaje rosnąć i faktycznie poświęca się, uniemożliwiając wirusowi tworzenie kolejnych kopii i rozprzestrzenianie się w populacji. Zrozumienie, jak RAZR rozpoznaje moment przejścia z cichego obserwatora w wykonawcę komórkowego, jest centralnym pytaniem tego badania. 
Wirusowe pierścienie, które przełączają mechanizm
Naukowcy odkryli, że RAZR jest aktywowany przez specyficzne białka wytwarzane przez kilka niespokrewnionych fagów. W jednym z fagów białko nazwane Gp77 — prawdopodobnie biorące udział w naprawie lub okrągleniu genomu wirusowego — służyło jako wyzwalacz. W innych fagach wyzwalaczami były białka „portalowe”, umieszczone w kluczowym wejściu powłoki wirusowej i pomagające wstrzykiwać DNA do gospodarza. Chociaż te białka różnią się bardzo sekwencją i kształtem jako pojedyncze cząsteczki, wszystkie mają jedną uderzającą cechę: układają się w duże pierścienie o niemal identycznej średnicy. Przy użyciu krioelektronowej mikroskopii zespół wykazał, że Gp77 tworzy 24-częściowy pierścień, a białka portalowe — 12-częściowe pierścienie. RAZR, które normalnie tworzy luźne, liniowe łańcuchy, owija się wokół tych wirusowych pierścieni, budując masywny, wielowarstwowy kompleks okrągły o średnicy przekraczającej 25 nanometrów.
Budowa molekularnej maszyny zagłady
W obrębie tego kompleksu RAZR łączy dwie funkcjonalne części: czujnik w postaci palca cynkowego, który chwytając pierścień wirusowy, oraz „ostrze” HEPN, które tnie RNA. Dwa segmenty palca cynkowego z sąsiednich cząsteczek RAZR wiążą każdą jednostkę białka wirusowego, zapewniając, że RAZR pokrywa pierścień w precyzyjny i silnie kooperatywny sposób. Ta pierścieniowa rusztownica wymusza na domenach tnących RNA RAZR zakrzywione, ciasno upakowane ustawienie, pozwalając wielu miejscom cięcia układać się na zewnętrznej krawędzi niczym zęby piły tarczowej. Mutacje, które zaburzają powierzchnie kontaktu między RAZR a białkami faga, lub które osłabiają sposób, w jaki cząsteczki RAZR ze sobą współdziałają, paraliżują obronę. Mały, elastyczny łącznik łączący część sensoryczną i tnącą RAZR okazuje się również niezbędny, pomagając białku przyjąć właściwą geometrię, gdy przylega do pierścienia wirusa.
Po zmontowaniu na wirusowej rusztownicy RAZR przekształca się w potężną maszynę niszczącą RNA. Autorzy pokazują, że aktywowany RAZR nie narusza DNA, ale tnie wiele typów jednoniciowego RNA: tRNA, rRNA i mRNA zarówno z bakterii, jak i z zakażającego faga. W żywych komórkach to rozległe cięcie RNA szybko blokuje syntezę białek, pozostawiając w dużej mierze nienaruszone replikację DNA i transkrypcję. W eksperymentach probówkowych zmieszanie oczyszczonego RAZR z jego wirusowymi wyzwalaczami wystarcza, by całkowicie zahamować syntezę białek. Poprzez zatrzymanie translacji w ten tępym, niespecyficzny sposób, system skazuje zainfekowaną komórkę na śmierć, ale jednocześnie pozbawia faga molekularnych narzędzi potrzebnych do replikacji. 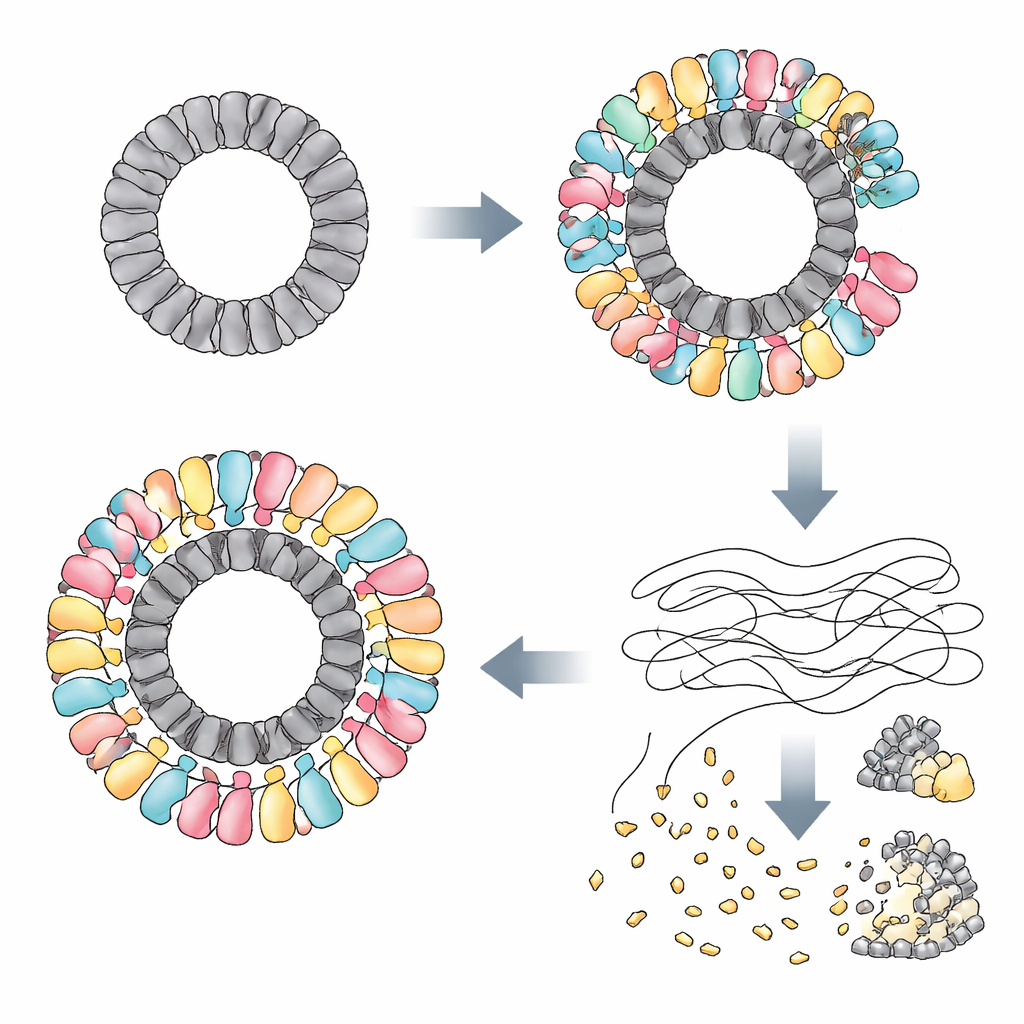
Dopasowywanie obrony do różnych wirusów
Chociaż białka RAZR z różnych bakterii mają podobną domenę tnącą, badanie wykazuje, że ich sensory palca cynkowego różnią się znacznie. Wymiana tych segmentów sensorycznych między dwiema wersjami RAZR, z E. coli i Klebsiella variicola, w dużym stopniu zamienia zakres fagów, które potrafią zatrzymać. Nawet gdy dwa warianty RAZR celują w tego samego faga, polegają na nieco innych punktach kontaktu na białku portalowym wirusa, o czym świadczą odrębne mutacje wirusa umożliwiające ucieczkę. Sugeruje to, że bakterie mogą precyzyjnie dostrajać swój zakres antywirusowy poprzez ewolucję części sensorycznej RAZR, zachowując jednocześnie potężną maszynerię tnącą RNA.
Wspólne pomysły w całym drzewie życia
Ostatecznie autorzy proponują, że RAZR nie rozpoznaje konkretnego wirusowego „hasła”, lecz sygnaturę strukturalną: duże pierścienie białkowe o określonym rozmiarze, które pojawiają się tylko podczas infekcji fagowej i nie występują w mechanizmach własnych gospodarza. Owijając się wokół tych pierścieni i wykorzystując je jako matryce do własnego składania, RAZR wzmacnia słaby sygnał wirusowy do odpowiedzi odpornościowej typu wszystko albo nic. Ta strategia jest ściśle zbliżona do tego, jak wiele kompleksów wrodzonej odporności u zwierząt, w tym u ludzi, formuje gigantyczne włókniste lub pierścieniowe struktury, by wykrywać patogeny i aktywować destrukcyjne enzymy. Praca ta ujawnia więc uderzające konwergencje: od bakterii po ssaki życie wielokrotnie wyewoluowało sposoby budowania olbrzymich struktur białkowych, które obracają geometrię najeźdźczych wirusów przeciwko nim samym.
Cytowanie: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Słowa kluczowe: odporność na bakteriofagi, wewnętrzna obrona bakteryjna, supramolekularny kompleks białkowy, rozkład RNA, system RAZR