Clear Sky Science · sv
Bakteriell immunaktivering via supramolekylär montering med bakteriofager
Hur bakterier överlistar sina virala angripare
Bakterier jagas ständigt av virus kallade fager som kan förvandla ett frodigt mikrobiellt samhälle till en död mark på bara minuter. Denna studie avslöjar ett förvånande nytt sätt som vissa bakterier slåss tillbaka på: genom att bygga stora molekylära ringar som kan känna av inkommande fager och sedan medvetet stänga ner den infekterade cellen inifrån. Arbetet visar inte bara en listig form av bakteriellt självförsvar, utan speglar även strategier som används av vårt eget medfödda immunsystem, vilket antyder djupa gemensamma teman i hur livet upptäcker och stoppar infektioner.
En liten väktare med ett dubbelliv
Artikeln fokuserar på ett bakteriellt protein som författarna döper om till RAZR, funnet i Escherichia coli och många andra arter. På egen hand är RAZR ofarligt: celler kan producera det i höga nivåer utan negativa effekter. Men när vissa fager infekterar blir RAZR plötsligt dödligt — både för värdcellen och för viruset. Systemet verkar genom så kallad “abortive infection”: när RAZR slås på slutar den infekterade bakterien att växa och offrar i praktiken sig själv, vilket förhindrar att viruset gör fler kopior och sprids i populationen. Att förstå hur RAZR vet när det ska gå från tyst åskådare till cellulär bödel är studiens centrala fråga. 
Virala ringar som slår omkopplaren
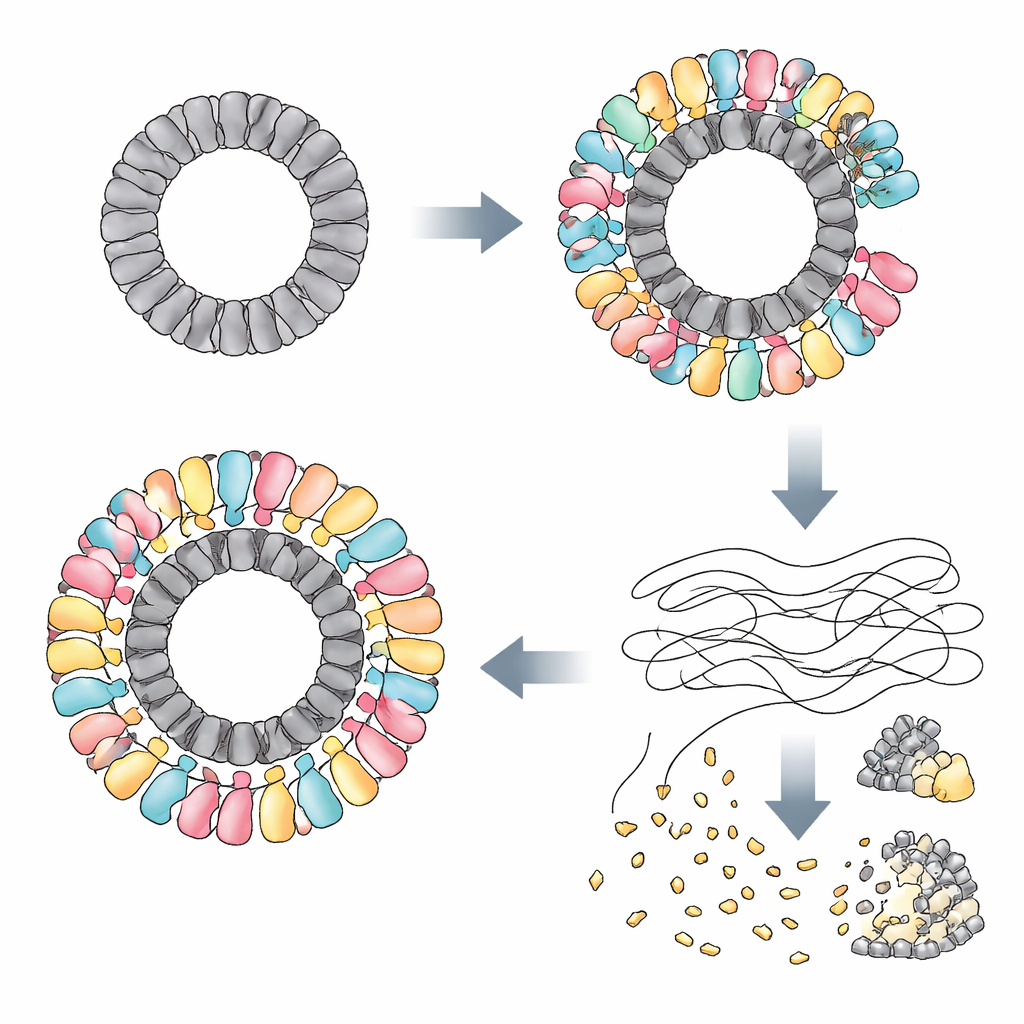
Forskarna upptäckte att RAZR aktiveras av specifika proteiner som tillverkas av flera icke närbesläktade fager. I en fag fungerade ett protein kallat Gp77 — sannolikt involverat i reparation eller cirkularisering av det virala genomet — som utlösare. I andra fager var utlösarna “portalproteiner” som sitter vid en central port i den virala kapseln och hjälper till att injicera DNA i värden. Även om dessa proteiner ser mycket olika ut i sekvens och form som individuella molekyler delar de alla en slående egenskap: de monterar sig till stora ringar med nästan identisk diameter. Med kryoelektronmikroskopi visade teamet att Gp77 bildar en 24-delad ring, och att portalproteiner bildar 12-delade ringar. RAZR, som normalt bildar lösa linjära kedjor, sveper sig runt dessa virala ringar för att bygga ett massivt, flerskiktat cirkulärt komplex över 25 nanometer i diameter.
Bygga en molekylär domedagsapparat
I detta komplex för samman RAZR två funktionella regioner: en zinkfinger-”sensor” som greppar den virala ringen, och ett HEPN-”blad” som klyver RNA. Två zinkfingerdelar från närliggande RAZR-molekyler binder varje viralt protein-enhet, vilket säkerställer att RAZR täcker ringen på ett precist och mycket kooperativt sätt. Denna ringformade ställning tvingar RAZR:s RNA-klyvande domäner till en böjd, tätt packad arrangemang, vilket tillåter många klyvningsställen att rada upp sig längs ytterkanten som tänder på en cirkelsåg. Mutationer som stör kontaktytorna mellan RAZR och fagproteinerna, eller som försvagar hur RAZR-molekyler håller ihop, försvagar försvaret. En liten flexibel länk som förbinder sensors- och klyvdelarna av RAZR visar sig också vara avgörande, eftersom den hjälper proteinet att anta rätt geometri när det omfamnar den virala ringen.
Slita sönder RNA för att stoppa viral spridning
När det väl är monterat på sitt fagframställda skelett förvandlas RAZR till en kraftfull RNA-förstörande maskin. Författarna visar att aktiverat RAZR lämnar DNA orört men skär många typer av enkelsträngat RNA: transfer-RNA, ribosomalt RNA och budbärar-RNA från både bakterien och den infekterande fagen. I levande celler blockerar denna omfattande RNA-klyvning snabbt proteinsyntesen samtidigt som DNA-replikation och transkription i stort sett lämnas intakta. I provrörsexperiment räcker det att blanda renat RAZR med dess virala utlösare för att stoppa proteinsyntesen tvärt. Genom att stoppa translationen på detta hårda, icke-specifika sätt dömer systemet den infekterade cellen men svälter också fagen på de molekylära verktyg den behöver för att reproducera sig.
Anpassa försvar mot olika virus
Även om RAZR-proteiner från olika bakterier delar en liknande klyvdomän, visar studien att deras zinkfingersensorer varierar stort. Att byta dessa sensorssegment mellan två RAZR-versioner, från E. coli och Klebsiella variicola, byter i stort sett vilka fager de kan stoppa. Även när två RAZR-varianter riktar sig mot samma fag förlitar de sig på något olika kontaktpunkter på det virala portalproteinet, vilket visas av olika virala undkomstmutationer. Detta tyder på att bakterier kan finslipa sitt antivirusområde genom att utveckla sensorportionen av RAZR, samtidigt som den kraftfulla RNA-klyvande maskineriet hålls intakt.
Delade idéer över livets träd
Sammanfattningsvis föreslår författarna att RAZR inte känner igen ett specifikt viralt “lösenord” utan ett strukturellt signum: stora proteingringar av en viss storlek som bara uppträder under faginfektioner och saknas i värdens egna maskinerier. Genom att svepa sig runt dessa ringar och använda dem som mall för sin egen montering, förstärker RAZR en svag viral signal till ett allt-eller-inget-immunsvar. Denna strategi liknar nära hur många medfödda immunkomplex hos djur, inklusive människor, bildar jättelika filamentösa eller ringformade strukturer för att upptäcka patogener och aktivera destruktiva enzymer. Arbetet avslöjar därmed en slående konvergens: från bakterier till däggdjur har livet upprepade gånger utvecklat sätt att bygga stora proteinkonstruktioner som vänder de inkräktande virusens geometri mot dem.
Citering: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Nyckelord: bakteriofag-immunitet, bakteriellt medfött försvar, supramolekylärt proteinkomplex, RNA-klyvning, RAZR-systemet