Clear Sky Science · fr
Activation immunitaire bactérienne via assemblage supramoléculaire déclenché par des phages
Comment les bactéries déjouent leurs envahisseurs viraux
Les bactéries sont constamment traquées par des virus appelés phages, capables de transformer une communauté microbienne prospère en cimetière en quelques minutes. Cette étude dévoile une façon surprenante dont certaines bactéries ripostent : elles construisent d’énormes anneaux moléculaires qui détectent l’arrivée des phages puis provoquent volontairement l’arrêt de la cellule infectée de l’intérieur. Ce travail révèle non seulement une forme ingénieuse d’autodéfense bactérienne, mais fait également écho à des stratégies employées par notre propre système immunitaire inné, suggérant des thèmes communs profonds sur la façon dont la vie détecte et stoppe les infections.
Un petit gardien à double vie
L’article se concentre sur une protéine bactérienne que les auteurs renomment RAZR, présente chez Escherichia coli et de nombreuses autres espèces. Isolée, RAZR est inoffensive : les cellules peuvent la produire en grande quantité sans effet délétère. Pourtant, lorsque certains phages infectent, RAZR devient soudainement mortelle — pour la cellule hôte autant que pour le virus. Le système fonctionne par « infection avortée » : une fois RAZR activé, la bactérie infectée cesse de croître et se sacrifie en pratique, empêchant le virus de fabriquer de nouvelles copies et de se propager dans la population. Comprendre comment RAZR sait quand basculer d’un rôle d’observateur discret à celui d’exécuteur cellulaire est la question centrale de l’étude. 
Des anneaux viraux qui actionnent l’interrupteur
Les chercheurs ont découvert que RAZR est activé par des protéines spécifiques produites par plusieurs phages non apparentés. Dans un phage, une protéine nommée Gp77 — probablement impliquée dans la réparation ou la circularisation du génome viral — joue le rôle de déclencheur. Dans d’autres phages, les déclencheurs étaient des protéines « de portail » qui se trouvent à une porte d’entrée clé de la coque virale et aident à injecter l’ADN dans l’hôte. Bien que ces protéines diffèrent fortement dans leur séquence et leur forme en tant que molécules individuelles, elles partagent toutes une caractéristique frappante : elles s’assemblent en grands anneaux d’un diamètre presque identique. Grâce à la cryo‑microscopie électronique, l’équipe a montré que Gp77 forme un anneau à 24 sous‑unités, tandis que les protéines de portail forment des anneaux à 12 sous‑unités. RAZR, qui forme normalement des chaînes linéaires lâches, s’enroule autour de ces anneaux viraux pour construire un vaste complexe circulaire multicouche de plus de 25 nanomètres de diamètre.
Construction d’un dispositif moléculaire du Jugement dernier
Au sein de ce complexe, RAZR réunit deux régions fonctionnelles : un « capteur » à doigt de zinc qui agrippe l’anneau viral, et une « lame » HEPN qui coupe l’ARN. Deux segments à doigt de zinc issus de molécules RAZR voisines se lient à chaque unité protéique virale, garantissant que RAZR enrobe l’anneau de manière précise et hautement coopérative. Cet échafaudage en forme d’anneau contraint les domaines de coupure d’ARN de RAZR à adopter une disposition courbée et très compacte, permettant à de nombreux sites de coupure de s’aligner sur le bord extérieur comme les dents d’une scie circulaire. Des mutations qui perturbent les surfaces de contact entre RAZR et les protéines de phage, ou qui affaiblissent les interactions entre molécules RAZR, compromettent la défense. Un petit lien flexible qui relie les parties sensorielle et catalytique de RAZR s’avère également essentiel, aidant la protéine à adopter la géométrie adéquate lorsqu’elle entoure l’anneau viral.
Déchiqueter l’ARN pour arrêter la propagation virale
Une fois assemblé sur son échafaudage d’origine virale, RAZR se transforme en une puissante machine destructrice d’ARN. Les auteurs montrent que RAZR activé laisse l’ADN intact mais tranche de nombreux types d’ARN simple brin : ARN de transfert, ARN ribosomiques et ARNm issus à la fois de la bactérie et du phage infectant. Dans les cellules vivantes, ce clivage généralisé de l’ARN bloque rapidement la synthèse protéique tout en laissant la réplication de l’ADN et la transcription en grande partie inchangées. En éprouvettes, le mélange de RAZR purifié avec ses déclencheurs viraux suffit à arrêter net la traduction. En suspendant la traduction de manière aussi franche et non spécifique, le système condamne la cellule infectée mais affame aussi le phage des outils moléculaires nécessaires à sa réplication. 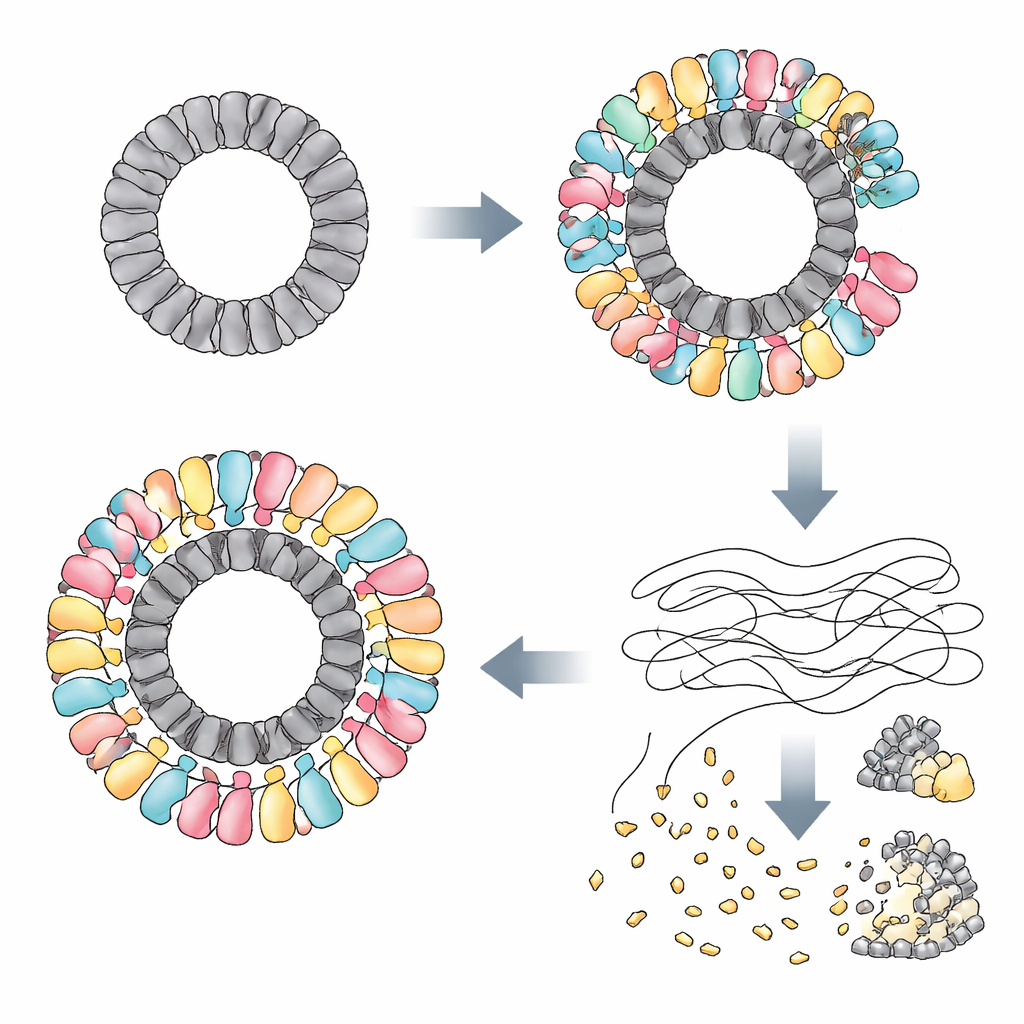
Adapter la défense à différents virus
Bien que les protéines RAZR de différentes bactéries partagent un domaine de coupure similaire, l’étude constate que leurs capteurs à doigt de zinc varient largement. L’échange de ces segments sensoriels entre deux versions de RAZR, provenant de E. coli et de Klebsiella variicola, inverse en grande partie les phages qu’elles peuvent neutraliser. Même lorsque deux variantes de RAZR ciblent le même phage, elles s’appuient sur des points de contact légèrement différents de la protéine de portail virale, comme le montrent des mutations d’échappement virales distinctes. Cela suggère que les bactéries peuvent affiner leur spectre antivirale en faisant évoluer la portion capteur de RAZR, tout en conservant intacte la puissante machinerie de coupure d’ARN.
Idées partagées à travers l’arbre de la vie
Au final, les auteurs proposent que RAZR ne détecte pas un « mot de passe » viral spécifique mais une signature structurelle : de grands anneaux protéiques d’une taille particulière qui n’apparaissent que lors de l’infection par des phages et sont absents des machineries propres à l’hôte. En s’enroulant autour de ces anneaux et en les utilisant comme modèles pour son propre assemblage, RAZR amplifie un signal viral faible en une réponse immunitaire tout ou rien. Cette stratégie reflète de près la manière dont de nombreux complexes immunitaires innés chez les animaux, y compris chez l’humain, forment d’énormes assemblages filamenteux ou annelés pour détecter les agents pathogènes et activer des enzymes destructrices. Le travail révèle ainsi une convergence frappante : des bactéries aux mammifères, la vie a évolué à plusieurs reprises pour construire d’immenses structures protéiques qui retournent la géométrie des virus envahisseurs contre eux.
Citation: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Mots-clés: immunité aux bactériophages, défense innée bactérienne, complexe protéique supramoléculaire, clivage de l’ARN, système RAZR