Clear Sky Science · nl
Bacteriële immuunactivatie via supramoleculaire assemblage met fagentriggers
Hoe bacteriën hun virale indringers te slim af zijn
Bacteriën worden voortdurend belaagd door virussen, fagenn genoemd, die een bloeiende microbiele gemeenschap binnen enkele minuten in een kerkhof kunnen veranderen. Deze studie onthult een verrassende nieuwe manier waarop sommige bacteriën terugvechten: door enorme moleculaire ringen te bouwen die binnenkomende fagen detecteren en vervolgens de geïnfecteerde cel van binnenuit opzettelijk stilleggen. Het werk onthult niet alleen een slimme vorm van bacteriële zelfverdediging, maar weerspiegelt ook strategieën die ons eigen aangeboren immuunsysteem gebruikt, wat wijst op diepe gemeenschappelijke thema’s in hoe leven infecties detecteert en stopt.
Een klein bewaker met een dubbel leven
Het artikel richt zich op een bacterieel eiwit dat de auteurs RAZR noemen, gevonden in Escherichia coli en vele andere soorten. Op zichzelf is RAZR onschadelijk: cellen kunnen het in grote hoeveelheden produceren zonder nadelige effecten. Maar wanneer bepaalde fagen infecteren, wordt RAZR plotseling dodelijk — zowel voor de gastheercel als voor het virus. Het systeem werkt via “abortieve infectie”: zodra RAZR wordt geactiveerd, stopt de geïnfecteerde bacterie met groeien en offert zich effectief op, waardoor het virus wordt verhinderd meer kopieën te maken en zich door de populatie te verspreiden. Begrijpen hoe RAZR weet wanneer het moet overschakelen van stille toeschouwer naar cellulair beul is de centrale vraag van de studie. 
Virale ringen die de schakel omzetten
De onderzoekers ontdekten dat RAZR wordt geactiveerd door specifieke eiwitten die door verschillende, niet-verwante fagen worden gemaakt. In één faag fungeerde een eiwit genaamd Gp77 — waarschijnlijk betrokken bij het repareren of circulair maken van het virale genoom — als de trigger. In andere fagen waren de triggers “portaal”eiwitten die op een sleutelpoort in de virale mantel zitten en helpen DNA in de gastheer te injecteren. Hoewel deze eiwitten als individuele moleculen qua sequentie en vorm sterk van elkaar kunnen verschillen, delen ze allemaal één opvallende eigenschap: ze assembleren tot grote ringen van vrijwel identieke diameter. Met cryo-elektronenmicroscopie toonde het team aan dat Gp77 een ring van 24 onderdelen vormt, en dat portaalproteïnen 12-delige ringen vormen. RAZR, dat normaal losse lineaire ketens vormt, wikkelt zich om deze virale ringen om een gigantisch, meerlagig circulair complex te bouwen van meer dan 25 nanometer doorsnee.
Het bouwen van een moleculair doemapparaat
Binnen dit complex brengt RAZR twee functionele regio’s samen: een zinkvinger-“sensor” die de virale ring vastgrijpt, en een HEPN-“blad” dat RNA knipt. Twee zinkvingersegmenten van naburige RAZR-moleculen binden elk virale eiwitunit, waardoor RAZR de ring op een nauwkeurige en sterk cooperatieve manier bekleedt. Dit ringvormige steigerwerk dwingt RAZR’s RNA-knipdomeinen in een gebogen, dicht opeengepakte ordening, waardoor vele knipplaatsen de buitenrand vormen als tanden op een cirkelzaag. Mutaties die de contactvlakken tussen RAZR en de faagproteïnen verstoren, of die verzwakken hoe RAZR-moleculen aan elkaar kleven, verlammen de verdediging. Een kleine flexibele schakel die de sensor- en knipdelen van RAZR verbindt blijkt ook essentieel, omdat die het eiwit helpt de juiste geometrie aan te nemen wanneer het de virale ring omhelst.
RNA versnipperen om virale verspreiding te stoppen
Eens opgebouwd op zijn door de faag gemaakte steiger, verandert RAZR in een krachtige RNA-verwoestende machine. De auteurs tonen aan dat geactiveerde RAZR DNA onaangeroerd laat maar vele soorten enkelstrengig RNA doorsnijdt: transfer-RNA’s, ribosomaal RNA en boodschapper-RNA’s van zowel de bacterie als de infecterende faag. In levende cellen blokkeert deze wijdverspreide RNA-kleuring snel de eiwitsynthese terwijl DNA-replicatie en transcriptie grotendeels intact blijven. In proefbuisexperimenten is het mengen van gezuiverd RAZR met zijn virale triggers voldoende om de eiwitsynthese volledig stil te leggen. Door translatie op deze directe, niet-specifieke manier te stoppen, veroordeelt het systeem de geïnfecteerde cel maar berooft het ook de faag van de moleculaire gereedschappen die het nodig heeft om zich te reproduceren. 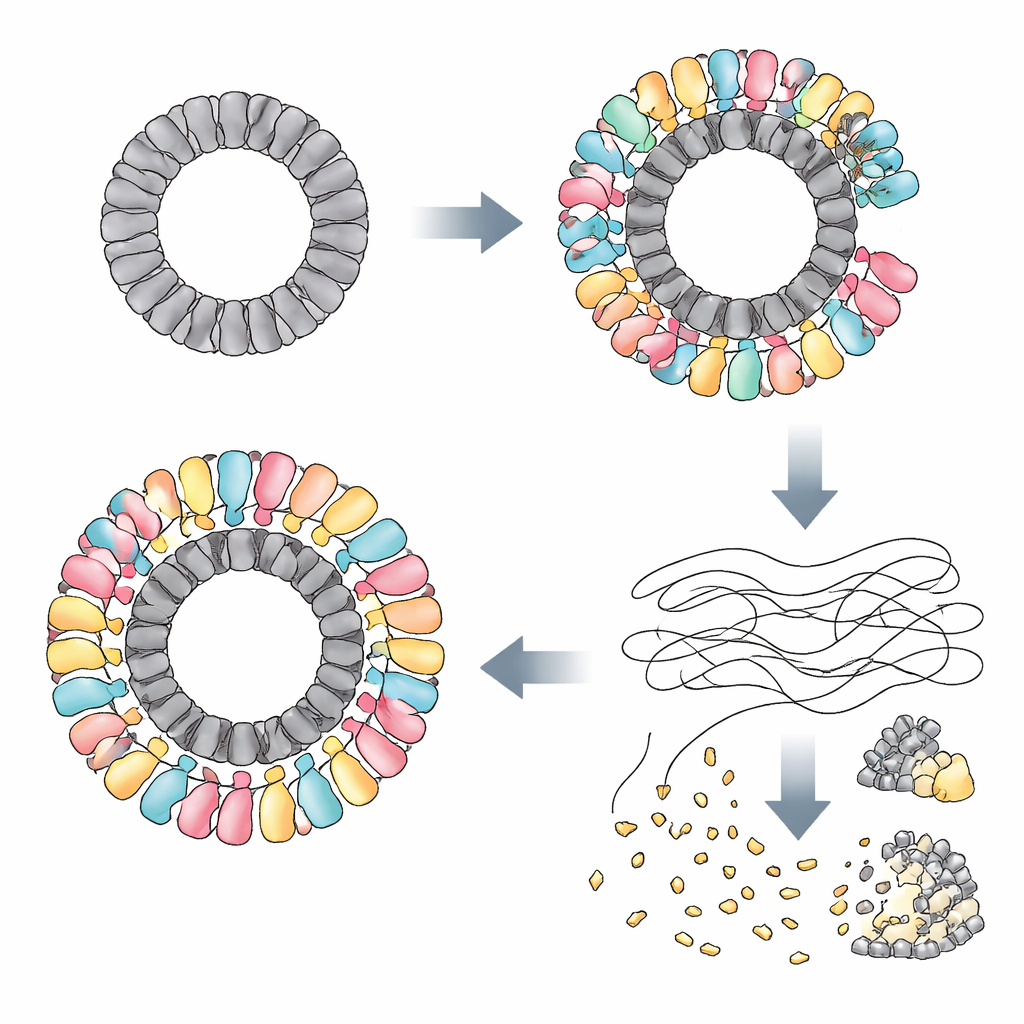
Verdediging afstemmen op verschillende virussen
Hoewel RAZR-eiwitten uit verschillende bacteriën een vergelijkbaar knipdomein delen, blijkt uit de studie dat hun zinkvingersensoren sterk variëren. Het verwisselen van deze sensorsgmenten tussen twee RAZR-versies, van E. coli en Klebsiella variicola, verwisselt grotendeels welke fagen ze kunnen stoppen. Zelfs wanneer twee RAZR-varianten zich op dezelfde faag richten, zijn ze afhankelijk van licht verschillende contactpunten op het virale portaalproteïne, zoals blijkt uit onderscheidende ontsnappingsmutaties van het virus. Dit suggereert dat bacteriën hun antivirale bereik fijn kunnen afstemmen door het sensorsgedeelte van RAZR te evolueren, terwijl ze de krachtige RNA-knipmachinerie intact houden.
Gedeelde ideeën door de levensboom heen
Uiteindelijk stellen de auteurs voor dat RAZR geen specifiek viraal “wachtwoord” herkent maar een structurele handtekening: grote proteïneringen van een bepaalde grootte die alleen tijdens faaginfectie verschijnen en afwezig zijn in het eigen machinerie van de gastheer. Door zich om deze ringen te wikkelen en ze als sjabloon voor eigen assemblage te gebruiken, versterkt RAZR een zwak viraal signaal tot een alles-of-niets immuunrespons. Deze strategie weerspiegelt nauw hoe veel aangeboren immuuncomplexen bij dieren, inclusief mensen, reusachtige filamentachtige of ringvormige assemblages vormen om pathogenen te detecteren en destructieve enzymen te activeren. Het werk onthult daarmee een opvallende convergentie: van bacteriën tot zoogdieren heeft het leven herhaaldelijk manieren ontwikkeld om enorme eiwitstructuren te bouwen die de geometrie van binnendringende virussen tegen hen keren.
Bronvermelding: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
Trefwoorden: bacteriofaagimmuniteit, bacteriële aangeboren verdediging, supramoleculair proteïnecomplex, RNA-splitsing, RAZR-systeem