Clear Sky Science · ja
ファージとの超分子集合による細菌の免疫活性化
細菌がウイルス侵入者を出し抜く仕組み
細菌はファージと呼ばれるウイルスに常に狙われており、繁栄している微生物群集が数分で死の場所に変わることさえあります。本研究は、一部の細菌が反撃する驚くべき新しい方法を明らかにします。それは、侵入するファージを感知すると巨大な分子リングを組み立て、感染した細胞を内部から意図的に停止させるというものです。この研究は巧妙な細菌の自己防御の形を示すだけでなく、私たちの自然免疫系が用いる戦略と類似点を示唆しており、感染の検出と停止における生命の普遍的なテーマを示しています。
二重の顔を持つ小さな守護者
論文は著者らがRAZRと呼び直した細菌タンパク質に焦点を当てています。RAZRはEscherichia coliや多くの他の種に見られます。単独ではRAZRは無害で、細胞は高レベルでそれを産生しても問題ありません。しかし特定のファージが感染すると、RAZRは突如として致命的になります—宿主細胞にもウイルスにも致命的です。このシステムは「中止感染(abortive infection)」を通じて働きます。RAZRが作動すると、感染した細菌は成長を止めて自らを犠牲にし、ウイルスが複製して個体群に広がるのを防ぎます。RAZRが静かな傍観者から細胞の処刑者へと切り替わる瞬間をどのように判断するかが本研究の中心的な疑問です。 
スイッチを入れるウイルスのリング
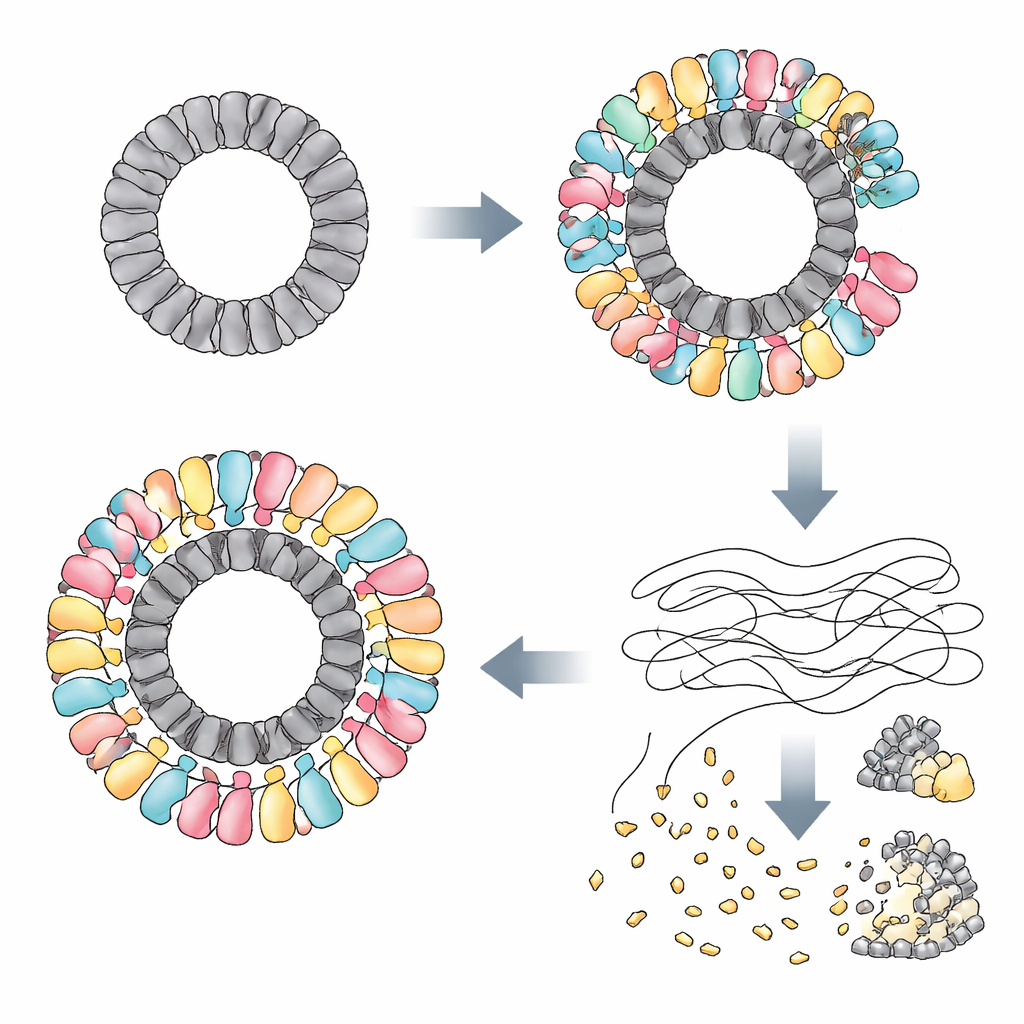
研究者たちは、RAZRがいくつかの系統の異なるファージが作る特定のタンパク質によって活性化されることを発見しました。あるファージでは、恐らくウイルスゲノムの修復や環化に関わると考えられるGp77というタンパク質が引き金として働きました。別のファージでは、ウイルスの殻の重要な出入口に位置しDNAを宿主へ注入するのを助ける「ポータル」タンパク質が引き金でした。これらのタンパク質は配列や個々の分子の形は大きく異なりますが、いずれも際立った共通点を持っています:ほぼ同じ直径の大きなリングを組み立てることです。クライオ電子顕微鏡を用いて、チームはGp77が24成分のリングを形成し、ポータルタンパク質が12成分のリングを形成することを示しました。通常は緩やかな線状鎖を作るRAZRは、こうしたウイルス由来のリングに巻きついて、直径25ナノメートルを超える巨大で多層の円形複合体を構築します。
分子規模の終末装置を組み上げる
この複合体の内部で、RAZRは二つの機能領域を結びつけます:ウイルスリングを把握する亜鉛フィンガーの「センサー」とRNAを切断するHEPNの「ブレード」です。隣接するRAZR分子からの二つの亜鉛フィンガー断片が、それぞれウイルスのタンパク質単位に結合し、RAZRがリングを正確かつ高度に協調して被覆することを保証します。このリング状の足場はRAZRのRNA切断ドメインを曲線状かつ高密度に配置させ、外周に多数の切断サイトが円鋸の歯のように並ぶことを可能にします。RAZRとファージタンパク質間の接触面を破壊する変異、あるいはRAZR分子同士の結合を弱める変異は防御を損ないます。センサーと切断部位をつなぐ小さく柔軟なリンカーも不可欠で、RAZRがウイルスリングに抱き着く際に適切な幾何学を採るのを助けます。
ウイルス拡散を止めるためのRNA粉砕
ファージ由来の足場上に組み上がると、RAZRは強力なRNA破壊装置に変わります。著者らは、活性化されたRAZRがDNAには手を付けず、多様な一本鎖RNAを切断することを示しています:tRNA、リボソームRNA、そして細菌および感染ファージ双方のメッセンジャーRNAです。生細胞では、この広範なRNA切断が迅速にタンパク質合成を阻止し、DNA複製や転写は大部分がそのまま維持されます。試験管内実験では、純化したRAZRをそのウイルス引き金と混ぜるだけでタンパク質合成が即座に止まります。このように翻訳を非選択的に止めることで、システムは感染細胞を滅ぼす一方で、ファージが複製に必要な分子機構を奪い去ります。
異なるウイルスに合わせた防御の調整
異なる細菌由来のRAZRは似た切断ドメインを共有していますが、研究は亜鉛フィンガーのセンサー部分が大きく多様であることを示しています。E. coliとKlebsiella variicola由来の二つのRAZRのセンサー断片を入れ替えると、ほぼそのまま止められるファージの範囲が入れ替わります。たとえ二つのRAZR変異体が同じファージを標的にしても、ウイルスのポータルタンパク質上の接触点はやや異なり、異なるウイルスの回避変異として現れます。これは、細菌がRAZRのセンサー部分を進化させることで抗ウイルスの範囲を微調整でき、その一方で強力なRNA切断機構は維持できることを示唆します。
生命の樹を越えた共有概念
結論として、著者らはRAZRが特定のウイルス「パスワード」ではなく、構造的な署名を感知していると提案します:ファージ感染時にのみ現れ宿主自身の機構には存在しない、特定サイズの大きなタンパク質リングです。RAZRはこれらのリングを取り巻き、自らの組み立ての鋳型として利用することで、かすかなウイルス信号を全か無かの免疫応答へと増幅します。この戦略は、動物(ヒトを含む)における多くの自然免疫複合体が病原体を検出し破壊酵素を活性化するために巨大なフィラメント状またはリング状の集合体を形成するやり方と密接に類似しています。こうして本研究は顕著な収束を明らかにします:細菌から哺乳類に至るまで、生命は侵入するウイルスの幾何学を逆手に取り巨大なタンパク質構造を構築する方法を繰り返し進化させてきたのです。
引用: Zhang, T., Lyu, Y., Beck, C.R. et al. Bacterial immune activation via supramolecular assembly with phage triggers. Nature 651, 1051–1059 (2026). https://doi.org/10.1038/s41586-025-10060-8
キーワード: バクテリオファージ免疫, 細菌の自然免疫防御, 超分子タンパク質複合体, RNA切断, RAZRシステム