Clear Sky Science · tr
PLK1 ana bağlantı motiflerinin moleküler anatomisi
Hücreler bölünme motorlarını nasıl rayında tutar
Her hücre bölünmesi sırasında, kromozomların şaşırtıcı bir doğrulukla kopyalanıp ayrılması gerekir. Bu süreçte önemli bir yardımcı, bölünen kromozomlar için trafik kontrolörü gibi davranan PLK1 adlı bir enzimdir. Bu çalışma basit ama önemli bir soruyu soruyor: PLK1 tam olarak nereye gideceğini nasıl bilir ve doğru yer ve zamanda nasıl aktive olur? Bağlanma bölgelerini atomik ayrıntıda haritalayarak, yazarlar birkaç özel “ana” iniş yerinin PLK1’e hem doğruluk hem de güç sağladığını gösteriyor.
Kromozomlarda hedefli iniş noktaları
PLK1, polo-kutusu (polo-box) adı verilen ve bir bağlanma modülü gibi davranan bir protein bölgesine sahiptir. Bu domain, diğer proteinler üzerindeki kısa fosforile olmuş dizileri tanır ve PLK1’in hücre bölünmesi sırasında etkinliğinin gerektiği yerlere tam olarak yerleşmesini sağlar. Önceki çalışmalar, kromozom bağlanma bölgesindeki iki proteinin, BUB1 ve CENP-U’nun özellikle önemli olduğunu göstermişti: bu proteinlerin bağlanma bölgeleri kaldırılırsa PLK1 artık bu yapılarda görünmez. Yazarlar, bu “ana” bağlantı motiflerinin hücrede dağınık halde bulunan birçok zayıf, geçici bağlanma yerinden ayıran özel tasarım kurallarını paylaşabileceğini düşündüler.
Süper güçlü bir iniş yeri oluşturan röle
Grup, kromozomun bağlantı noktasının iç kısmında yer alan CENP-U üzerinde yoğunlaştı. CENP-U’nun, T78 ve T98 olarak adlandırılan amino asitler etrafında yer alan iki yakın potansiyel bağlanma motifi vardır. Biyokimyasal ve kütle spektrometrisi deneyleri, ilk olarak CDK1 adlı bir enzimin T98’i fosfat grubu ile kolayca işaretlediğini gösterdi. Bu ilk işaretleme PLK1’i çeker ve PLK1 daha sonra daha elverişsiz olan T78 bölgesini bir “röle” sürecinde fosforile eder. Yapısal veriler ve bağlanma ölçümleri, T78 çevresi değiştirildiğinde, bölgenin PLK1 için olağanüstü derecede güçlü bir iniş yerinde dönüştüğünü ve T98’e göre yaklaşık 100 kat daha sıkı bağlandığını ortaya koydu.
Bir ana site, iki taneden daha iyidir
İlk bakışta, iki fosforile motifin varlığı bir çift PLK1 molekülünün yan yana bağlanıp birbirlerini stabilize ettiği izlenimini veriyordu. Kristal yapılar gerçekten tek bir CENP-U zinciri üzerinde iki polo-kutusu domaininin oturduğunu gösterdi. Ancak ayrıntılı bağlanma ölçümleri farklı bir tablo çizdi: ikinci sitenin eklenmesi genel bağlanmayı anlamlı şekilde güçlendirmedi ve hatta biraz zayıflatabiliyordu. Bunun yerine yazarlar, oluşturulduktan sonra T78 merkezli tek bir sitenin tek başına ana bağlantı noktası olarak hizmet etmeye yetecek kadar güçlü olduğunu buldular. Bu gücün kaynağı, dimerizasyondan ziyade PLK1’in birden çok cebine oturan geniş temas yüzeyiydi.
Güçlü bağlantı motiflerinin ortak tasarımı
CENP-U parçasını genişleterek ve bunu BUB1, BUBR1 ve PRC1 gibi diğer bilinen PLK1 ortaklarıyla karşılaştırarak araştırmacılar tekrarlayan bir desen gördüler. Ana motifler, merkez cebine bağlanmak için bir fosforile amino asit kullanır, ancak aynı zamanda yakın yivlere hidrofobik yan zincirler yerleştirirler; bunlar daha önce yeterince takdir edilmemiş “kriptik” bir cep ve bitişiğindeki bir hidrofobik boşluğu içerir. AlphaFold tabanlı bilgisayar modelleri, birkaç yüksek etkili PLK1 ortağının polo-kutusu etrafında benzer şekilde sarıldığını ve aynı anda birden fazla cebin doldurulduğunu öne sürer. Bu genişletilmiş iz, PLK1’i yerel hedefleri uzun süre modifiye edebilecek şekilde yakın tutabilen ana bağlantı motiflerinin ayırt edici özelliği gibi görünmektedir.
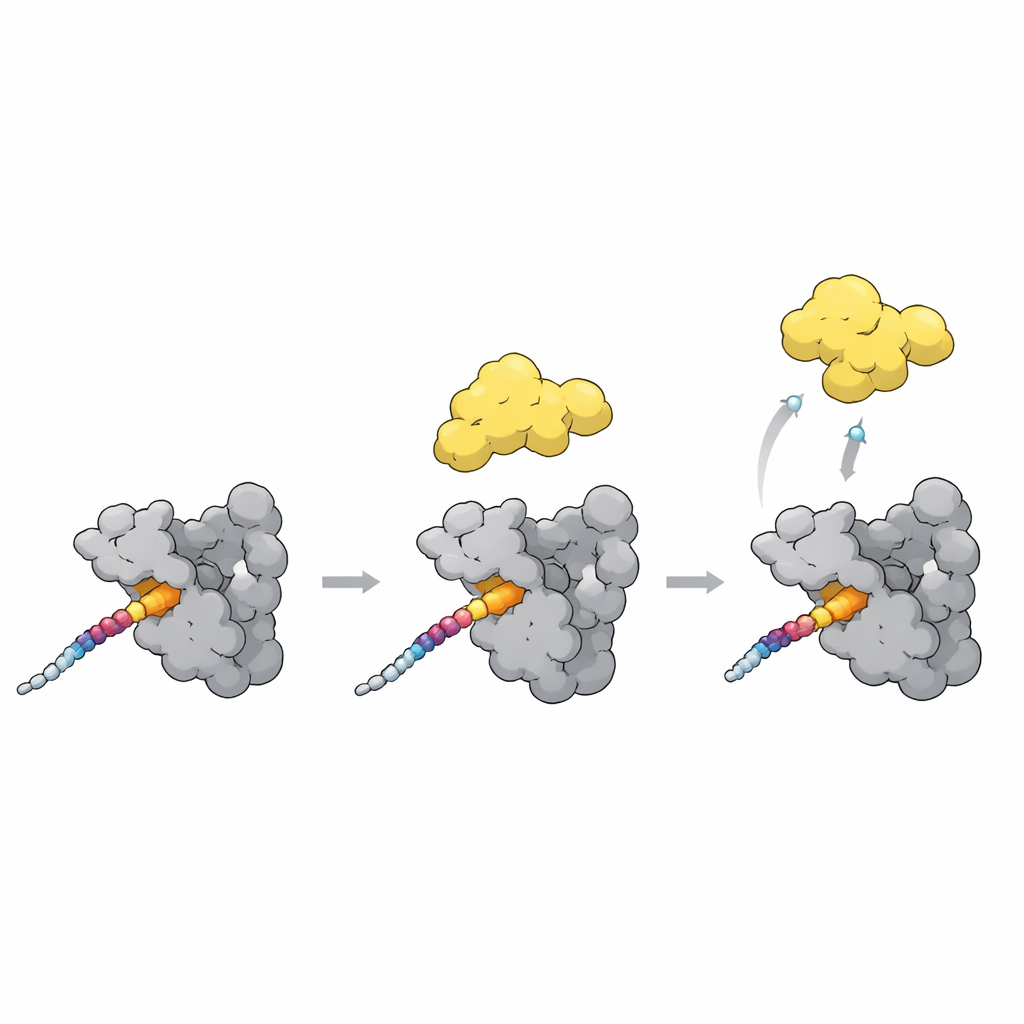
PLK1’i kapalıdan açık hale geçirmek
Bulmacanın son parçası, bağlanmanın PLK1 aktivitesini nasıl açıp kapattığıdır. Kapalı durumda polo-kutusu domaini PLK1’in kinaz kısmına yaslanır ve onu kısmen kapalı tutar. Yeni yapılar ve AlphaFold modelleri, polo-kutusundaki esnek bir döngünün anahtar bir sensör olduğunu işaret ediyor. T78 gibi güçlü bir bağlanma motifi polo-kutusu yüzeyi boyunca bağlandığında, bu döngü yer değiştirir ve kinazı yakın tutan bağlantı ile çarpışır. Bu çarpışma muhtemelen PLK1’i daha açık, aktif bir şekle doğru itmektedir. İlginç bir şekilde, doğal bir inhibitör proteinin aynı ceplere bağlanıp kapalı formu stabilize etmesi, benzer temasların PLK1’i ya açabileceğini ya da durumuna bağlı olarak kilitleyebileceğini gösterir.
Bu moleküler harita neden önemli
Basitçe söylemek gerekirse, bu çalışma PLK1’in kromozomlarda etkili olmak için çiftlenmeye gerek duymadığını gösteriyor. Bunun yerine, CDK1 ve PLK1 tarafından iki adımda oluşturulan tek, özenle inşa edilmiş bir ana bağlantı yeri PLK1’i çok sıkı tutabilir ve onu aktif duruma çevirebilir. Diğer proteinlerdeki benzer genişletilmiş bağlantı motiflerinin aynı numarayı kullandığı görülüyor. Bu güçlü iniş padlerinin moleküler anatomisini ortaya koyarak çalışma, hücrelerin önemli bir bölünme enzimi üzerindeki hassas kontrolünü nasıl sağladığını açıklıyor ve PLK1 aktivitesini daha seçici şekilde ayarlayabilecek gelecekteki ilaçların tasarımları için şablonlar sunuyor.
Atıf: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Anahtar kelimeler: PLK1, CENP-U, hücre bölünmesi, kinetokor, protein bağlanması