Clear Sky Science · nl
Moleculaire anatomie van PLK1-master-dockingsmotieven
Hoe cellen hun delingsmotoren op koers houden
Elke keer dat een cel zich deelt, moet ze haar chromosomen met verbluffende precisie kopiëren en scheiden. Een belangrijke helper in dit proces is een enzym genaamd PLK1, dat fungeert als verkeersleider voor delende chromosomen. Deze studie stelt een eenvoudige maar belangrijke vraag: hoe weet PLK1 precies waar het naartoe moet en hoe schakelt het op de juiste plaats en het juiste moment in? Door zijn dockingsites in atomair detail in kaart te brengen, laten de auteurs zien hoe enkele speciale "master"-landingsplaatsen PLK1 zowel nauwkeurigheid als kracht geven.
Gerichte landingsplekken op chromosomen
PLK1 draagt een eiwensegment dat het polo-boxdomein wordt genoemd en dat fungeert als een dockingmodule. Dit domein herkent korte gefosforyleerde reeksen op andere eiwitten, waardoor PLK1 precies kan plaatsnemen waar zijn activiteit tijdens de celdeling nodig is. Eerder werk toonde aan dat twee eiwitten bij de chromosoom-aankoppelingsplaats, BUB1 en CENP-U, bijzonder belangrijk zijn: als hun dockingsites worden verwijderd, verschijnt PLK1 niet langer op die structuren. De auteurs vermoedden dat deze "master"-dockingsmotieven gedeelde ontwerprichtlijnen kunnen hebben die hen onderscheiden van de vele zwakkere, meer tijdelijke dockingsites verspreid door de cel.
Een relais dat een supersterke dockingsplaats opbouwt
Het team richtte zich op CENP-U, dat zich in het binnenste deel van het aanhechtingspunt van het chromosoom bevindt. CENP-U heeft twee nabijgelegen potentiële dockingsmotieven, gecentreerd rond de aminozuren T78 en T98. Biochemische en massaspectrometrie-experimenten toonden aan dat een eerste enzym, CDK1, T98 gemakkelijk met een fosfaatgroep markeert. Deze initiële markering trekt PLK1 aan, dat vervolgens in een "relais"-proces de minder gunstige T78-site fosforyleert. Structurele gegevens en bindingsmetingen onthulden dat, eens gemodificeerd, het gebied rond T78 een uitzonderlijk sterke landingsplaats voor PLK1 wordt en ongeveer 100 keer strakker bindt dan de T98-site.
Een enkele masterplaats is beter dan twee
Op het eerste gezicht suggereerde de aanwezigheid van twee gefosforyleerde motieven dat een paar PLK1-moleculen naast elkaar zouden kunnen binden en elkaar stabiliseren. Kristalstructuren toonden inderdaad twee polo-boxdomeinen op een enkele CENP-U-keten. Gedetailleerde bindingsmetingen vertelden echter een ander verhaal: het toevoegen van de tweede site versterkte de totale binding niet significant en kon die zelfs iets verzwakken. In plaats daarvan vonden de auteurs dat de enkele, op T78 gecentreerde site, eenmaal gemaakt, sterk genoeg is om op zichzelf als het master-dockingspunt te dienen. Haar kracht komt voort uit een groot contactoppervlak dat in meerdere pockets op PLK1 past, in plaats van uit dimerisatie.
Gedeeld ontwerp van krachtige dockingsmotieven
Door het CENP-U-fragment uit te breiden en te vergelijken met andere bekende PLK1-partners zoals BUB1, BUBR1 en PRC1, zagen de onderzoekers een terugkerend patroon. Mastermotieven gebruiken een gefosforyleerd aminozuur om een centraal pocket te engageren, maar plaatsen ook hydrofobe zijketens in nabijgelegen groeven, inclusief een eerder ondergewaardeerd "cryptisch" pocket en een aangrenzende hydrofobe holte. Computermodellen op basis van AlphaFold suggereren dat verschillende invloedrijke PLK1-partners zich op vergelijkbare wijze om de polo-box wikkelen en meerdere pockets tegelijk bezetten. Deze uitgebreide contactzone lijkt kenmerkend voor master-dockingsmotieven die PLK1 lang genoeg in de buurt kunnen houden om veel lokale doelen te wijzigen.
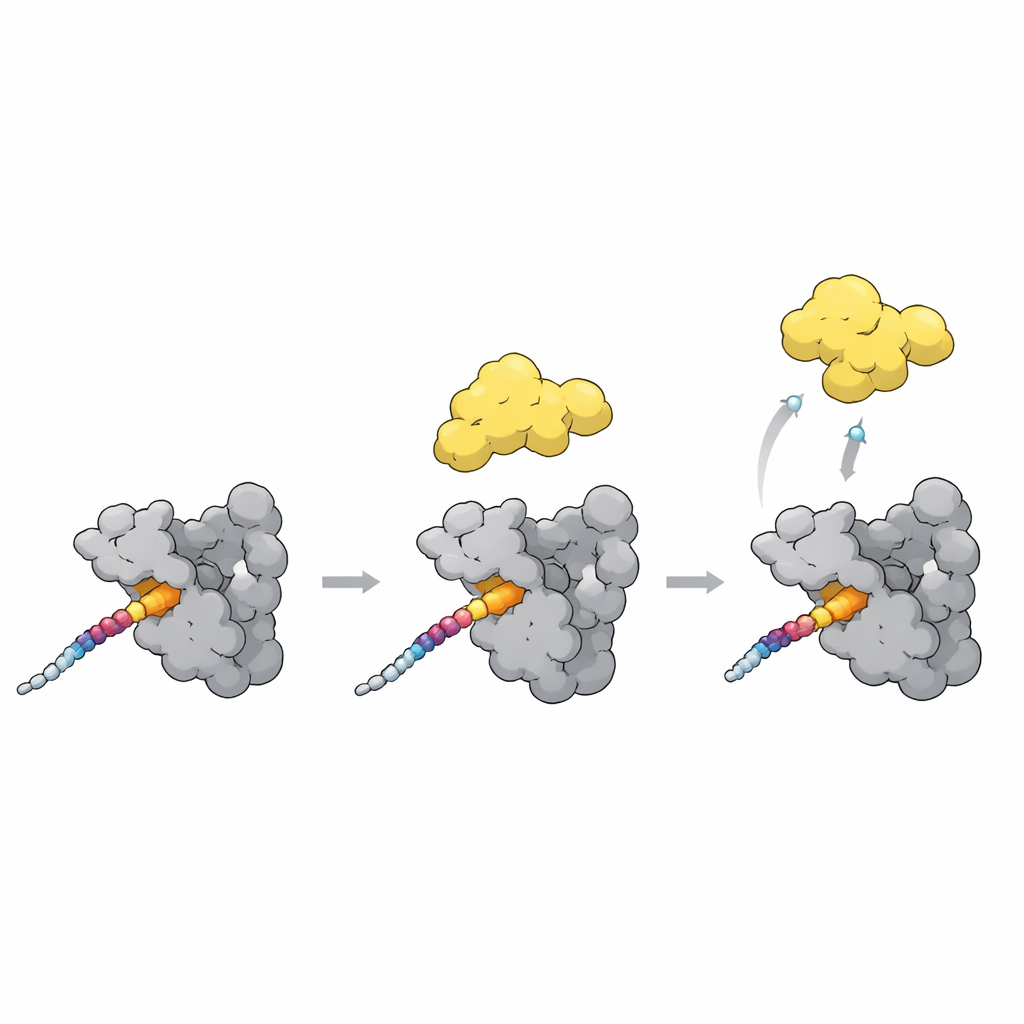
PLK1 schakelen van gesloten naar open
Een laatste puzzelstukje is hoe docking de activiteit van PLK1 omhoog of omlaag zet. In een gesloten toestand nestelt het polo-boxdomein zich tegen het kinasegedeelte van PLK1 en houdt het dat gedeeltelijk dicht. De nieuwe structuren, samen met AlphaFold-modellen, wijzen op een flexibele lus in de polo-box als een sleutelsensor. Wanneer een sterk dockingsmotief zoals de T78-site op CENP-U zich over het oppervlak van de polo-box bindt, verschuift deze lus en botst met de linker die het kinasegedeelte dicht bij zich houdt. Die botsing duwt PLK1 waarschijnlijk in een meer open, actieve vorm. Intrigerend genoeg bindt een natuurlijk remmend eiwit dezelfde pockets maar stabiliseert het in plaats daarvan de gesloten vorm, wat laat zien dat soortgelijke contacten PLK1 afhankelijk van de precieze rangschikking ofwel kunnen ontgrendelen of vastklemmen.
Waarom deze moleculaire kaart ertoe doet
In eenvoudige bewoordingen laat dit werk zien dat PLK1 niet hoeft te dubbelen om effectief op chromosomen te functioneren. In plaats daarvan kan een enkele, zorgvuldig opgebouwde master-dockingsplaats, die in twee stappen door CDK1 en PLK1 wordt gevormd, PLK1 zeer sterk vasthouden en omklappen naar een actieve toestand. Vergelijkbare uitgebreide dockingsmotieven op andere eiwitten lijken dezelfde truc te gebruiken. Door de moleculaire anatomie van deze krachtige landingsplaatsen te onthullen, verklaart de studie hoe cellen nauwkeurige controle over een belangrijk delingsenzym bereiken en biedt ze blauwdrukken voor toekomstige medicijnen die PLK1-activiteit selectiever kunnen bijsturen.
Bronvermelding: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Trefwoorden: PLK1, CENP-U, celdeling, kinetochore, proteïnedocking