Clear Sky Science · fr
Anatomie moléculaire des motifs d’amarrage maîtres de PLK1
Comment les cellules gardent leurs moteurs de division sur la bonne voie
À chaque division, une cellule doit copier et séparer ses chromosomes avec une précision remarquable. Un acteur clé de ce processus est une enzyme appelée PLK1, qui joue le rôle de contrôleur du trafic pour les chromosomes en division. Cette étude pose une question simple mais cruciale : comment PLK1 sait-il exactement où se rendre, et comment s’active-t-il au bon endroit et au bon moment ? En cartographiant ses sites d’amarrage à l’échelle atomique, les auteurs montrent comment quelques « plates-formes » maîtresses confèrent à PLK1 à la fois précision et puissance.
Des sites d’amarrage ciblés sur les chromosomes
PLK1 porte un segment protéique appelé domaine polo-box qui agit comme un module d’amarrage. Ce domaine reconnaît de courts motifs phosphorylés sur d’autres protéines, permettant à PLK1 de se positionner précisément là où son activité est nécessaire pendant la division cellulaire. Des travaux antérieurs avaient montré que deux protéines au niveau du point d’attache des chromosomes, BUB1 et CENP-U, sont particulièrement importantes : si leurs sites d’amarrage sont supprimés, PLK1 n’apparaît plus à ces structures. Les auteurs ont émis l’hypothèse que ces motifs d’amarrage « maîtres » pourraient partager des règles de conception spécifiques qui les distinguent des nombreux sites d’amarrage plus faibles et plus transitoires disséminés dans la cellule.
Un relais qui construit un site d’amarrage ultra-fort
L’équipe s’est concentrée sur CENP-U, situé dans la partie interne du point d’attache chromosomique. CENP-U possède deux motifs d’amarrage potentiels proches, centrés sur les acides aminés désignés T78 et T98. Des expériences biochimiques et de spectrométrie de masse ont montré qu’une première enzyme, CDK1, marque facilement T98 par une phosphorylation. Ce marquage initial attire PLK1, qui phosphoryle ensuite le site T78 moins favorable dans un processus de « relais ». Les données structurales et les mesures d’affinité ont révélé qu’une fois modifiée, la région autour de T78 devient une plate-forme d’amarrage exceptionnellement puissante pour PLK1, se liant environ 100 fois plus fortement que le site T98.
Un site maître unique vaut mieux que deux
À première vue, la présence de deux motifs phosphorylés suggérait qu’une paire de molécules PLK1 pourrait se lier côte à côte et se stabiliser mutuellement. Les structures cristallines montraient effectivement deux domaines polo-box posés sur une même chaîne de CENP-U. Cependant, des mesures d’affinité détaillées ont raconté une autre histoire : l’ajout du second site n’améliorait pas sensiblement la liaison globale et pouvait même l’affaiblir légèrement. Les auteurs ont plutôt découvert que le site centré sur T78, une fois formé, est suffisamment fort pour servir à lui seul de point d’amarrage maître. Sa force provient d’une vaste surface de contact qui s’insère dans plusieurs poches de PLK1, plutôt que d’une dimerisation.
Conception partagée des motifs d’amarrage puissants
En étendant le fragment de CENP-U et en le comparant à d’autres partenaires connus de PLK1 tels que BUB1, BUBR1 et PRC1, les chercheurs ont identifié un motif récurrent. Les motifs maîtres utilisent un acide aminé phosphorylé pour engager une poche centrale, mais placent aussi des chaînes latérales hydrophobes dans des sillons voisins, incluant une poche « cryptique » jusque-là sous-estimée et une cavité hydrophobe adjacente. Des modèles informatiques basés sur AlphaFold suggèrent que plusieurs partenaires de PLK1 à fort impact enrobent le polo-box de manière similaire, occupant plusieurs poches simultanément. Cette empreinte étendue semble être la signature des motifs d’amarrage maîtres capables de maintenir PLK1 à proximité assez longtemps pour modifier de nombreuses cibles locales.
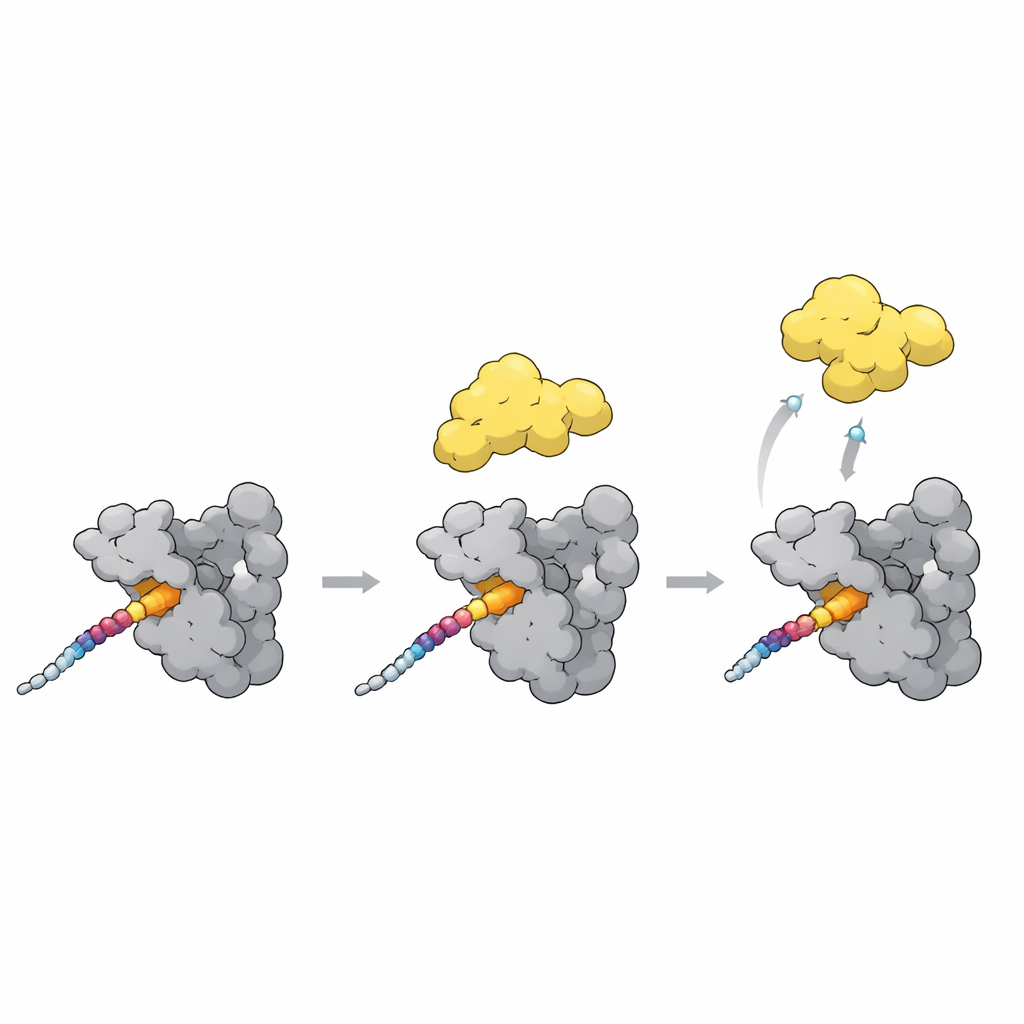
Basculer PLK1 de l’état fermé à l’état ouvert
Un dernier morceau du puzzle concerne la manière dont l’amarrage module l’activité de PLK1. À l’état fermé, le domaine polo-box se cale contre la partie kinase de PLK1 et la maintient partiellement inactivée. Les nouvelles structures, conjointement aux modèles AlphaFold, pointent vers une boucle flexible du polo-box comme capteur clé. Lorsqu’un motif d’amarrage fort, comme le site T78 de CENP-U, se lie à la surface du polo-box, cette boucle se déplace et entre en collision avec le linker qui maintient la kinase proche. Cette interaction pousse probablement PLK1 vers une conformation plus ouverte et active. Fait intéressant, une protéine inhibitrice naturelle se lie aux mêmes poches mais stabilise la forme fermée, montrant que des contacts similaires peuvent soit déverrouiller soit verrouiller PLK1 selon l’arrangement précis.
Pourquoi cette carte moléculaire est importante
En termes simples, ce travail montre que PLK1 n’a pas besoin de se doubler pour fonctionner efficacement au niveau des chromosomes. Au contraire, un seul site d’amarrage maître, construit soigneusement en deux étapes par CDK1 et PLK1, peut saisir PLK1 très fortement et le basculer en état actif. Des motifs d’amarrage étendus similaires sur d’autres protéines semblent utiliser la même astuce. En révélant l’anatomie moléculaire de ces plates-formes puissantes, l’étude explique comment les cellules obtiennent un contrôle précis d’une enzyme clé de la division et fournit des plans potentiels pour des médicaments futurs susceptibles de moduler l’activité de PLK1 de façon plus sélective.
Citation: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Mots-clés: PLK1, CENP-U, division cellulaire, kinétochore, ancrage de protéines