Clear Sky Science · he
האנאטומיה המולקולרית של מוטיבים עגינה מאסטריים של PLK1
כיצד התאים שומרים על מנועי החלוקה במסלול
בכל פעם שתא מתחלק עליו להעתיק ולהפריד את הכרומוזומים בדיוק מרשים. עוזר מרכזי בתהליך זה הוא אנזים בשם PLK1, שמתפקד כדוגמת בקר תנועה עבור הכרומוזומים במחלקה. במחקר זה נשאלה שאלה פשוטה אך חשובה: כיצד PLK1 יודע בדיוק לאיפה להגיע, וכיצד הוא נדלק במקום ובזמן הנכונים? על‑ידי מיפוי אתרי העגינה שלו ברזולוציה אטומית, המחברים חושפים כיצד כמה "משטחי נחיתה" מיוחדים מקנים ל‑PLK1 גם דיוק וגם עוצמה.
נקודות נחיתה ממוקדות על הכרומוזומים
ל‑PLK1 יש מקטע חלבוני הנקרא תחום ה‑polo‑box שפועל כמודול עגינה. תחום זה מזהה רצפים מקוצרים מפוספורלים על חלבונים אחרים, ומאפשר ל‑PLK1 להחנות בדיוק במקום שבו פעילותו נדרשת במהלך חלוקת התא. מחקרים קודמים הראו ששני חלבונים באתר שבהם הכרומוזום מתחבר — BUB1 ו‑CENP‑U — חשובים במיוחד: אם מסירים את אתרי העגינה שלהם, PLK1 כבר לא מופיע במבנים אלה. המחברים שיערו שמוטיבים עגינה "מאסטריים" אלה עשויים לשתף כללים עיצוביים מיוחדים שמבדילים אותם מהמון אתרי עגינה חלשים וזמניים הנפוצים בתא.
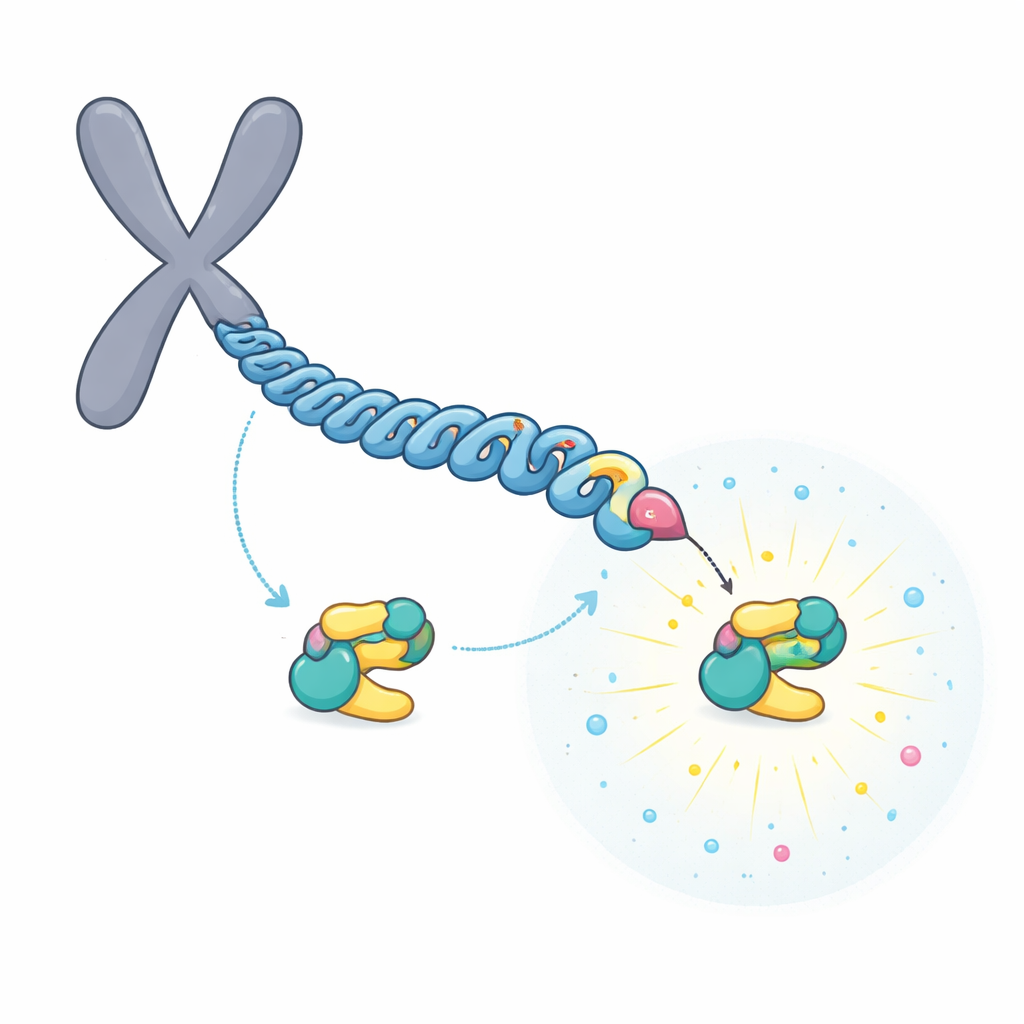
שרשרת שמשקמת אתר עגינה-על חזק במיוחד
הקבוצה התמקדה ב‑CENP‑U, הנמצא בחלקו הפנימי של נקודת ההצמדה של הכרומוזום. ל‑CENP‑U יש שני מוטיבים אפשריים לעגינה שעומדים זה לצד זה, ממוקדים סביב חומצות אמינו הידועות כ‑T78 ו‑T98. ניסויים ביוכימיים ומסות ספקטרומטריה הראו שאנזים ראשון, CDK1, מסמן בקלות את T98 בקבוצת פוספט. סימון ראשוני זה מושך את PLK1, אשר לאחר מכן מפוספורל את האתר הפחות עדיף T78 בתהליך "רדיאטיבי". נתונים מבניים ומדידות קשירה חשפו כי לאחר השינוי, האזור סביב T78 הופך למשטח נחיתה יוצא דופן לחוזק, קושר בערך פי 100 חזק יותר מאתר T98.
אתר מאסטר אחד עדיף על שניים
להתבונן ראשון, נוכחות שני מוטיבים מפוספוררים רמזה שזוג מולקולות PLK1 עשויות להתחבר זו מצד זו ולייצב זו את זו. מבני גבישיות אכן הראו שני תחומי polo‑box ישובים על שרשרת CENP‑U יחידה. עם זאת, מדידות קשירה מפורטות סיפקו סיפור שונה: הוספת האתר השני לא חיזקה משמעותית את הקשירה הכוללת ואף יכלה להחליש אותה קמעה. במקום זאת, המחברים מצאו שהאתר היחיד הממוקד ב‑T78, ברגע שנוצר, חזק מספיק מעצמו לשמש כנקודת העגינה המאסטרית. כוחו נובע ממשטח מגע גדול שנכנס לכמה כיסים ב‑PLK1, ולא מדימריזציה.
תכנון משותף של מוטיבי עגינה רבי‑השפעה
בהרחבת קטע CENP‑U והשוואתו עם שותפים ידועים אחרים של PLK1 כגון BUB1, BUBR1 ו‑PRC1, החוקרים ראו תבנית חוזרת. מוטיבי מאסטר משתמשים בחומצת אמינו מפוספורלת כדי להיכנס לכיס מרכזי, אך גם ממקמים שיירים הידרופוביים לתוך חריצים סמוכים, כולל כיס "קריפטי" שנמצא עד כה בתת‑הערכה וכן חלל הידרופובי שכונתי. מודלים ממוחשבים המבוססים על AlphaFold מציעים כי מספר שותפים בעלי השפעה גבוהה של PLK1 עוטפים את ה‑polo‑box באותו אופן, ותופסים כמה כיסים בבת אחת. טביעת הרגל המורחבת הזו נראית כסימן היכר של מוטיבי עגינה מאסטריים היכולים להחזיק את PLK1 בקרבת מקום זמן מספיק כדי לתקן רבים מהיעדים המקומיים.
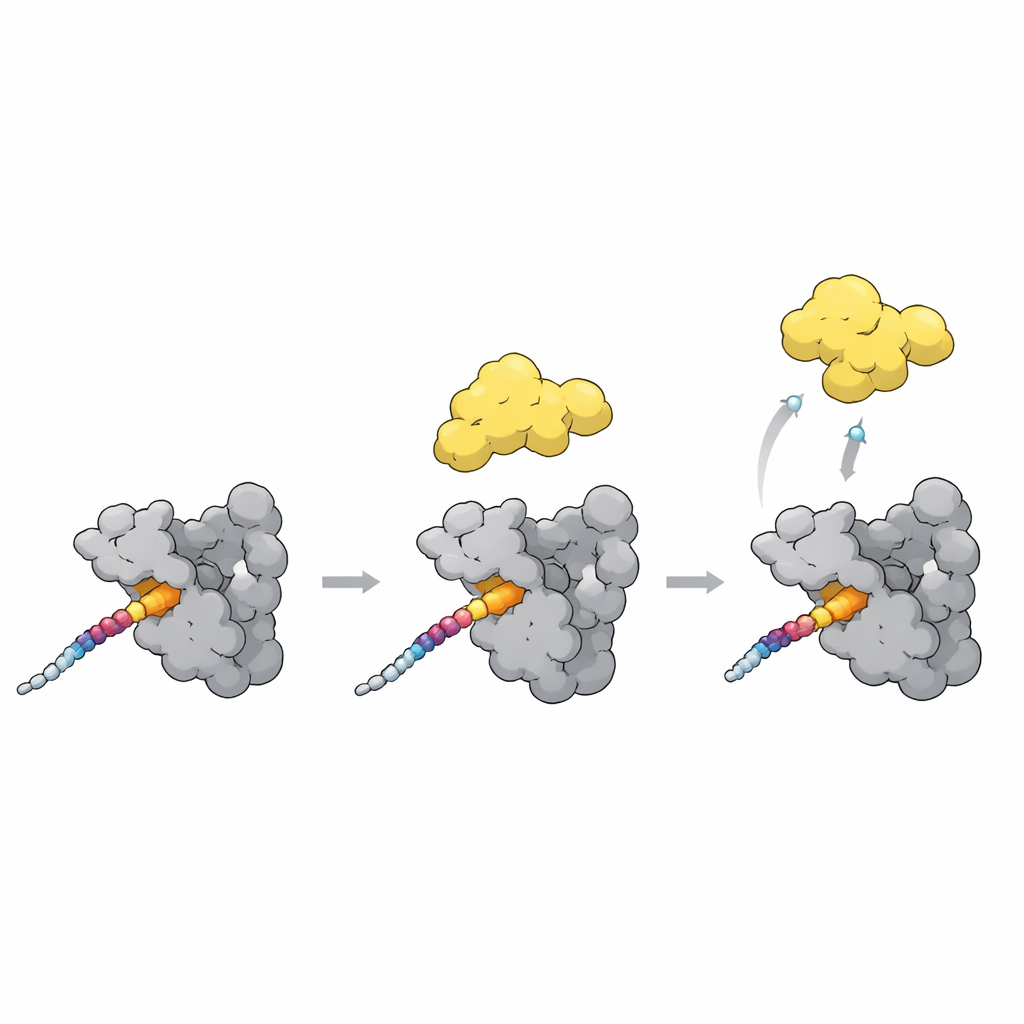
מעבר של PLK1 ממצב סגור לפתוח
חתיכה אחרונה בפזל היא כיצד העגינה משנה את פעילות ה‑PLK1 כלפי מעלה או מטה. במצב סגור, תחום ה‑polo‑box נצמד לחלק הקינאזי של PLK1 ומשאירו במידה מסוימת סגור. המבנים החדשים, יחד עם מודלי AlphaFold, מצביעים על לולאה גמישה בתחום ה‑polo‑box כחיישן מרכזי. כאשר מוטיב עגינה חזק כמו אתר T78 ב‑CENP‑U נקשר על פני משטח ה‑polo‑box, הלולאה הזו זזה ומתנגשת עם הקישור (linker) שמחזיק את הקינאז קרוב. ההתנגשות הזו כנראה דוחפת את PLK1 לצורה פתוחה ופעילה יותר. באופן מעניין, חלבון מעכב טבעי נקשר לאותם כיסים אך מייצב את הצורה הסגורה במקום זאת, מה שמראה כי מגעים דומים יכולים either לשחרר או להדק את PLK1 בהתאם לסידור המדויק.
מדוע המפה המולקולרית הזו חשובה
במילים פשוטות, עבודה זו מראה של‑PLK1 אין צורך להכפיל את עצמו כדי לפעול ביעילות על הכרומוזומים. במקום זאת, אתר עגינה מאסטרי יחיד, שנבנה בשני שלבים על‑ידי CDK1 ו‑PLK1, יכול לתפוס את PLK1 בחוזקה ולהחליפו למצב פעיל. מוטיבים מורחבים דומים על חלבונים אחרים נראים כמשתמשים באותה תחבולה. על‑ידי חשיפת האנטומיה המולקולרית של משטחי הנחיתה החזקים הללו, המחקר מסביר כיצד התאים משיגים שליטה מדויקת על אנזים חלוקה מרכזי ומספק תרשימים לבניית תרופות עתידיות שיכולות לכוונן את פעילות PLK1 בחריפות רבה יותר.
ציטוט: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
מילות מפתח: PLK1, CENP-U, חלוקת תאים, קינטוכור, עיגון חלבוני