Clear Sky Science · ru
Молекулярная анатомия основных докинг-мотивов PLK1
Как клетки держат мотор деления в нужном курсе
Каждый раз при делении клетки ей приходится копировать и разделять хромосомы с поразительной точностью. В этом процессе ключевую роль играет фермент PLK1, который действует как диспетчер для делящихся хромосом. В этом исследовании поставлен простой, но важный вопрос: как PLK1 точно находит нужные места и как он активируется в нужное время и в нужном месте? Картируя его сайты докинга с атомным разрешением, авторы показывают, как несколько специальных «мастер»-площадок обеспечивают PLK1 и точность, и силу.
Целевые посадочные места на хромосомах
PLK1 несет белковый сегмент, называемый polo-box-доменом, который служит модулем докинга. Этот домен распознает короткие фосфорилированные участки на других белках, позволяя PLK1 точно размещаться там, где его активность необходима во время деления клетки. Ранее работы показали, что два белка на месте прикрепления хромосомы, BUB1 и CENP-U, особенно важны: если их сайты докинга удалить, PLK1 больше не появляется в этих структурах. Авторы предположили, что эти «мастер»-мотивы докинга могут иметь особые конструктивные правила, отличающие их от множества более слабых, более временных сайтов докинга, разбросанных по клетке.
Реле, которое создает сверхсильный докинг-сайт
Команда сосредоточилась на CENP-U, который располагается во внутренней части точки прикрепления хромосомы. У CENP-U есть два соседних потенциальных докинг-мотива, сосредоточенных на аминокислотах, обозначаемых как T78 и T98. Биохимические эксперименты и масс-спектрометрия показали, что первый фермент, CDK1, с готовностью фосфорилирует T98. Эта первоначальная маркировка привлекает PLK1, который затем фосфорилирует менее благоприятный сайт T78 в процессе «реле». Структурные данные и измерения сродства показали, что после модификации регион вокруг T78 становится исключительно сильной посадочной площадкой для PLK1, связываясь примерно в 100 раз прочнее, чем сайт T98.
Один мастер-сайт лучше, чем два
На первый взгляд наличие двух фосфорилированных мотивов приводило к предположению, что пара молекул PLK1 может связаться бок о бок и стабилизировать друг друга. Кристаллические структуры действительно показали два polo-box-домена, сидящие на одной цепочке CENP-U. Однако подробные измерения сродства показали другую картину: добавление второго сайта не усиливало существенно общее связывание и даже могло немного его ослаблять. Вместо этого авторы обнаружили, что одиночный сайт, сосредоточенный вокруг T78, как только он сформирован, сам по себе достаточно силён, чтобы служить мастер-точкой докинга. Его сила исходит от большой контактной поверхности, которая входит в несколько карманов PLK1, а не от димеризации.
Общая конструкция мощных докинг-мотивов
Расширив фрагмент CENP-U и сопоставив его с другими известными партнёрами PLK1, такими как BUB1, BUBR1 и PRC1, исследователи выявили повторяющийся шаблон. Мастер-мотивы используют фосфорилированную аминокислоту для взаимодействия с центральным карманом, но также вводят гидрофобные боковые цепи в соседние борозды, включая ранее недооценённый «криптический» карман и прилегающую гидрофобную полость. Компьютерные модели на основе AlphaFold предполагают, что несколько высокоэффектных партнёров PLK1 охватывают polo-box схожим образом, занимая несколько карманов одновременно. Этот расширенный отпечаток кажется характерной чертой мастер-мотивов докинга, которые могут удерживать PLK1 рядом достаточно долго, чтобы он модифицировал множество локальных целей.
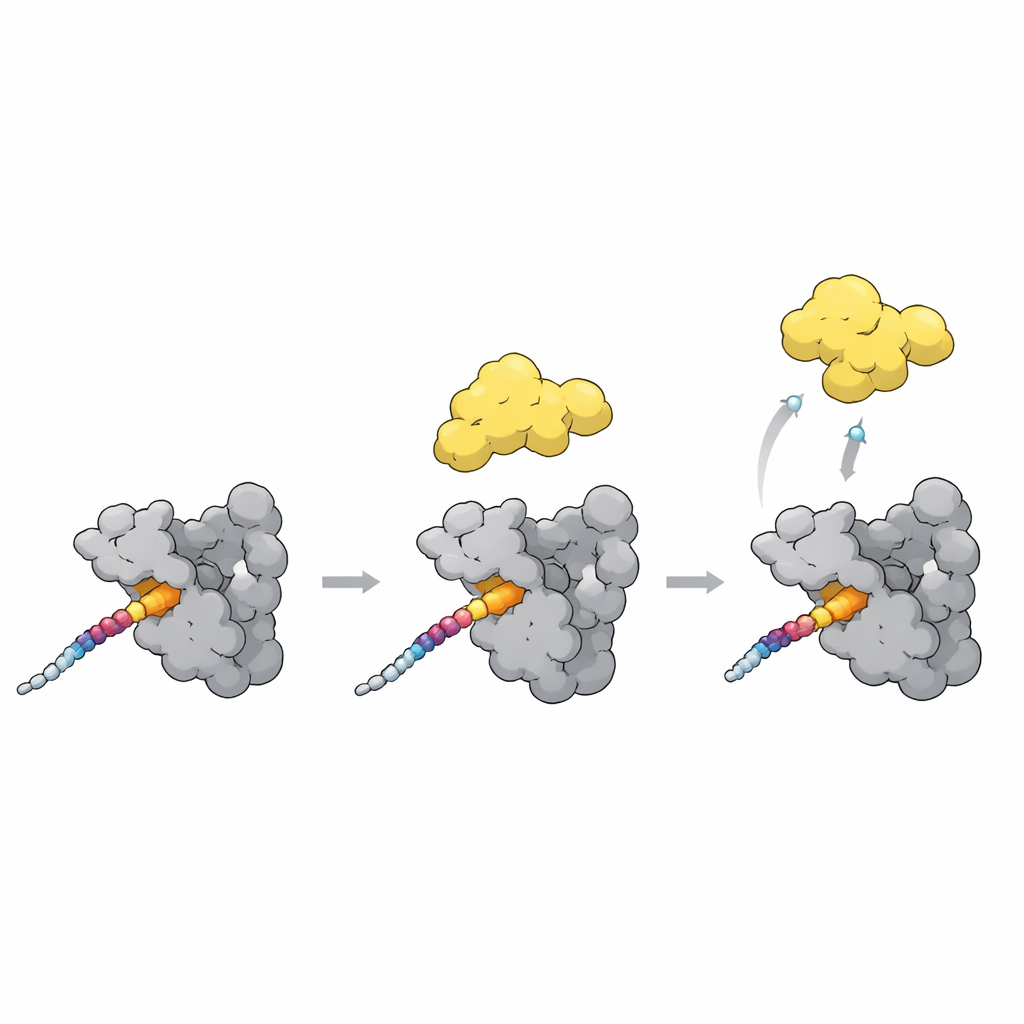
Переключение PLK1 из закрытого в открытое состояние
Последний кусок пазла — это то, как докинг повышает или понижает активность PLK1. В закрытом состоянии polo-box-домен прилегает к киназной части PLK1 и частично её блокирует. Новые структуры вместе с моделями AlphaFold указывают на гибкую петлю в polo-box как на ключевой сенсор. Когда сильный докинг-мотив, такой как сайт T78 на CENP-U, связывается с поверхностью polo-box, эта петля смещается и конфликтует с линкером, который держит киназу вблизи. Этот конфликт, вероятно, подталкивает PLK1 к более открытому, активному состоянию. Примечательно, что природный ингибиторный белок связывается с теми же карманами, но стабилизирует закрытую форму, показывая, что похожие контакты могут либо разблокировать, либо зажать PLK1 в зависимости от точного расположения.
Почему эта молекулярная карта важна
Проще говоря, эта работа показывает, что PLK1 не нуждается в удвоении, чтобы эффективно работать на хромосомах. Вместо этого один тщательно собранный мастер-докинг-сайт, сформированный в два шага CDK1 и PLK1, может очень сильно захватить PLK1 и перевести его в активное состояние. Похожие расширенные докинг-мотивы на других белках, по-видимому, используют тот же приём. Раскрывая молекулярную анатомию этих мощных посадочных площадок, исследование объясняет, как клетки добиваются точного контроля над ключевым ферментом деления и предлагает чертежи для будущих лекарств, которые могли бы избирательнее настраивать активность PLK1.
Цитирование: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Ключевые слова: PLK1, CENP-U, клеточное деление, кинетохор, докинг белков