Clear Sky Science · pl
Molekularna anatomia głównych motywów dokujących PLK1
Jak komórki utrzymują swoje maszyny podziału na właściwym torze
Za każdym razem, gdy komórka się dzieli, musi skopiować i rozdzielić chromosomy z oszałamiającą precyzją. Kluczowym pomocnikiem w tym procesie jest enzym o nazwie PLK1, pełniący rolę kontrolera ruchu dla dzielących się chromosomów. Badanie stawia proste, lecz ważne pytanie: skąd PLK1 wie dokładnie, dokąd ma podążać i jak włącza się w odpowiednim miejscu i czasie? Mapując jego miejsca dokowania w skali atomowej, autorzy ukazują, jak kilka specjalnych „nadrzędnych” platform dokujących zapewnia PLK1 zarówno precyzję, jak i siłę działania.
Ukierunkowane miejsca dokowania na chromosomach
PLK1 posiada fragment białkowy zwany domeną polo-box, która działa jako moduł dokujący. Domenę tę rozpoznaje krótkie sfałdowane (fosphorylowane) odcinki na innych białkach, co pozwala PLK1 zaparkować dokładnie tam, gdzie jego aktywność jest potrzebna podczas podziału komórki. Wcześniejsze badania wykazały, że dwa białka w miejscu przyczepu chromosomów, BUB1 i CENP-U, są szczególnie istotne: jeśli ich miejsca dokowania zostaną usunięte, PLK1 przestaje pojawiać się w tych strukturach. Autorzy podejrzewali, że te „nadrzędne” motywy dokujące mogą dzielić specjalne zasady konstrukcji, które odróżniają je od wielu słabszych, bardziej tymczasowych miejsc dokowania rozproszonych po komórce.
Przekaźnik budujący supermocne miejsce dokowania
Zespół skoncentrował się na CENP-U, które znajduje się w wewnętrznej części punktu przyczepu chromosomu. CENP-U ma dwa bliskie potencjalne motywy dokujące, skupione wokół aminokwasów oznaczonych jako T78 i T98. Doświadczenia biochemiczne i spektrometria mas wykazały, że pierwszy enzym, CDK1, chętnie znakuję T98 grupą fosforanową. To początkowe znakowanie przyciąga następnie PLK1, który w procesie „przekaźnikowym” fosforyluje mniej korzystne miejsce T78. Dane strukturalne i pomiary wiązania ujawniły, że po modyfikacji otoczenie wokół T78 staje się wyjątkowo silną platformą dokującą dla PLK1, wiążąc około 100 razy mocniej niż miejsce T98.
Jeden nadrzędny motyw lepszy niż dwa
Pierwotnie obecność dwóch sfosforylowanych motywów sugerowała, że para cząsteczek PLK1 mogłaby wiązać się obok siebie i wzajemnie stabilizować. Struktury krystaliczne rzeczywiście pokazały dwie domeny polo-box osadzone na jednym łańcuchu CENP-U. Jednak szczegółowe pomiary wiązania opowiedziały inną historię: dodanie drugiego miejsca nie wzmacniało znacząco całkowitego wiązania, a nawet mogło je nieco osłabić. Zamiast tego autorzy stwierdzili, że pojedyncze miejsce skoncentrowane wokół T78, gdy już powstanie, jest samo w sobie wystarczająco silne, by pełnić rolę nadrzędnego punktu dokującego. Jego siła wynika z dużej powierzchni kontaktu, która wypełnia kilka kieszeni na PLK1, a nie z dymeryzacji.
Wspólny projekt potężnych motywów dokujących
Rozszerzając fragment CENP-U i porównując go z innymi znanymi partnerami PLK1, takimi jak BUB1, BUBR1 i PRC1, badacze dostrzegli powtarzający się wzorzec. Motywy nadrzędne używają sfosforylowanego aminokwasu do zajęcia centralnej kieszeni, ale także umieszczają hydrofobowe łańcuchy boczne w sąsiednich rowkach, w tym w wcześniej niedocenianej „krypticznej” kieszeni i przylegającej jamie hydrofobowej. Modele komputerowe bazujące na AlphaFold sugerują, że kilku partnerów PLK1 o dużym wpływie owija się wokół domeny polo-box w podobny sposób, zajmując jednocześnie wiele kieszeni. Ten rozszerzony odcisk stopowy wydaje się być cechą charakterystyczną nadrzędnych motywów dokujących, które mogą utrzymać PLK1 blisko wystarczająco długo, by zmodyfikować liczne lokalne cele.
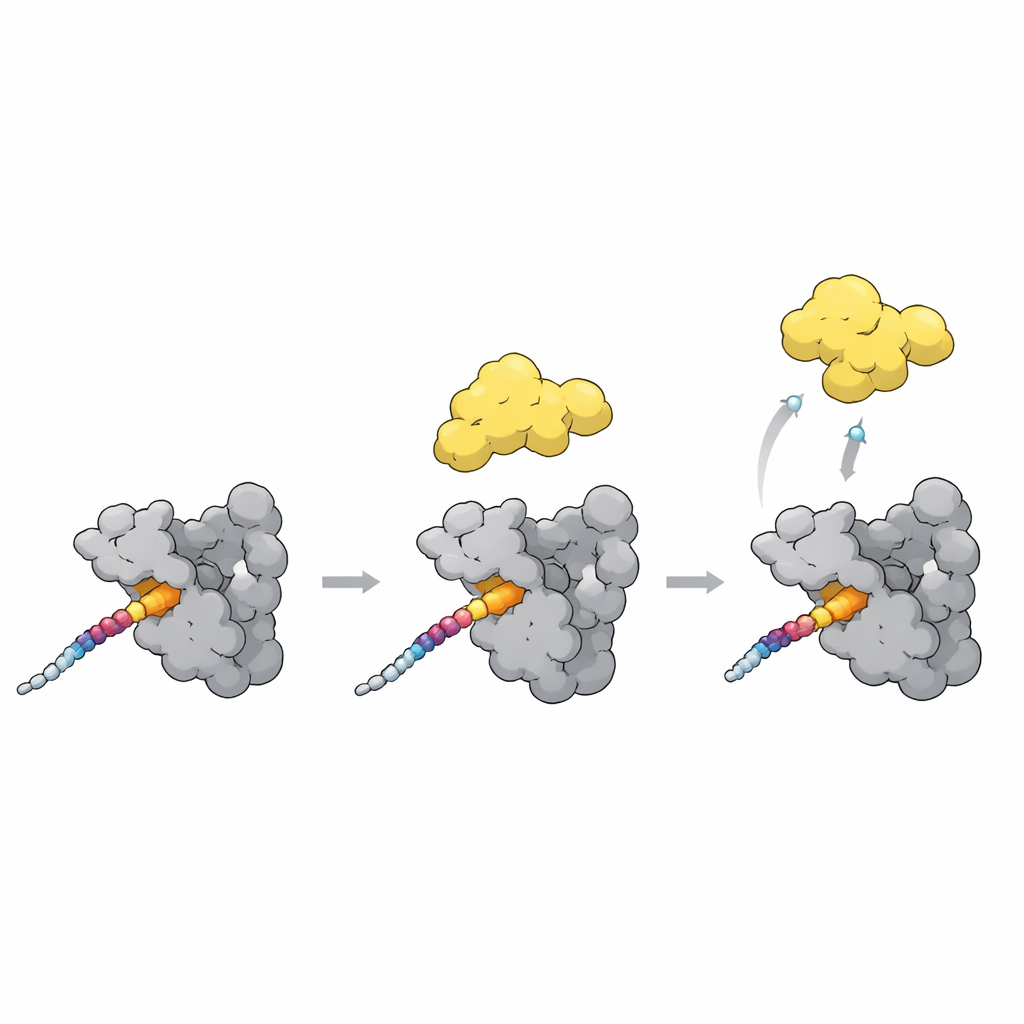
Przełączanie PLK1 z formy zamkniętej na otwartą
Ostatnim elementem układanki jest to, jak dokowanie zwiększa lub zmniejsza aktywność PLK1. W stanie zamkniętym domena polo-box przylega do części kinazowej PLK1 i utrzymuje ją częściowo zamkniętą. Nowe struktury, wraz z modelami AlphaFold, wskazują na elastyczną pętlę w polo-boxie jako kluczowy czujnik. Gdy mocny motyw dokujący, taki jak miejsce T78 na CENP-U, wiąże się po powierzchni polo-boxu, ta pętlą przesuwa się i koliduje z łącznikiem trzymającym kinazę blisko. Ta kolizja prawdopodobnie popycha PLK1 w bardziej otwartą, aktywną konformację. Co ciekawe, naturalne białko inhibitorowe wiąże te same kieszenie, ale stabilizuje formę zamkniętą, pokazując, że podobne kontakty mogą albo odblokować, albo zablokować PLK1, w zależności od dokładnego ułożenia.
Dlaczego ta molekularna mapa ma znaczenie
Mówiąc prosto, praca pokazuje, że PLK1 nie potrzebuje parowania, by działać efektywnie przy chromosomach. Zamiast tego pojedyncze, starannie zbudowane nadrzędne miejsce dokujące, powstające w dwóch krokach przez CDK1 i PLK1, potrafi bardzo mocno uchwycić PLK1 i przełączyć go w stan aktywny. Podobne rozszerzone motywy dokujące na innych białkach wydają się używać tego samego triku. Ujawniając molekularną anatomię tych potężnych platform dokujących, badanie wyjaśnia, jak komórki osiągają precyzyjną kontrolę nad kluczowym enzymem podziału i dostarcza planów do przyszłych leków, które mogłyby selektywniej modulować aktywność PLK1.
Cytowanie: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Słowa kluczowe: PLK1, CENP-U, podział komórkowy, kinetochor, dokowanie białek