Clear Sky Science · ja
PLK1のマスタードッキングモチーフの分子解剖学
細胞が分裂のエンジンを軌道に乗せる仕組み
細胞が分裂するたびに、染色体を複製し分離する必要があり、その精度は驚くべきものです。この過程で重要な助っ人となるのがPLK1と呼ばれる酵素で、分裂中の染色体の交通整理役を務めます。本研究は単純だが重要な問いを投げかけます:PLK1は正確にどこへ行くべきかをどう認識し、適切な場所とタイミングでどうやって活性化するのか? 著者らはドッキング部位を原子レベルで地図化することで、わずかな数の特別な「マスター」着地点がPLK1に精度と力をもたらす仕組みを明らかにします。
染色体上の標的化された着地点
PLK1はポロボックスドメインと呼ばれるタンパク質領域を持ち、これがドッキングモジュールとして働きます。このドメインは他のタンパク質上の短いリン酸化配列を認識し、分裂中にPLK1が活動を発揮すべき正確な位置に停泊させます。以前の研究で、染色体の付着部位に存在するBUB1とCENP-Uという二つのタンパク質が特に重要であることが示されていました:これらのドッキング部位が取り除かれると、PLK1はそれらの構造に現れなくなります。著者らは、これらの「マスター」ドッキングモチーフが、細胞内に散在する多くの弱く一時的なドッキング部位と区別される特別な設計ルールを共有しているのではないかと考えました。
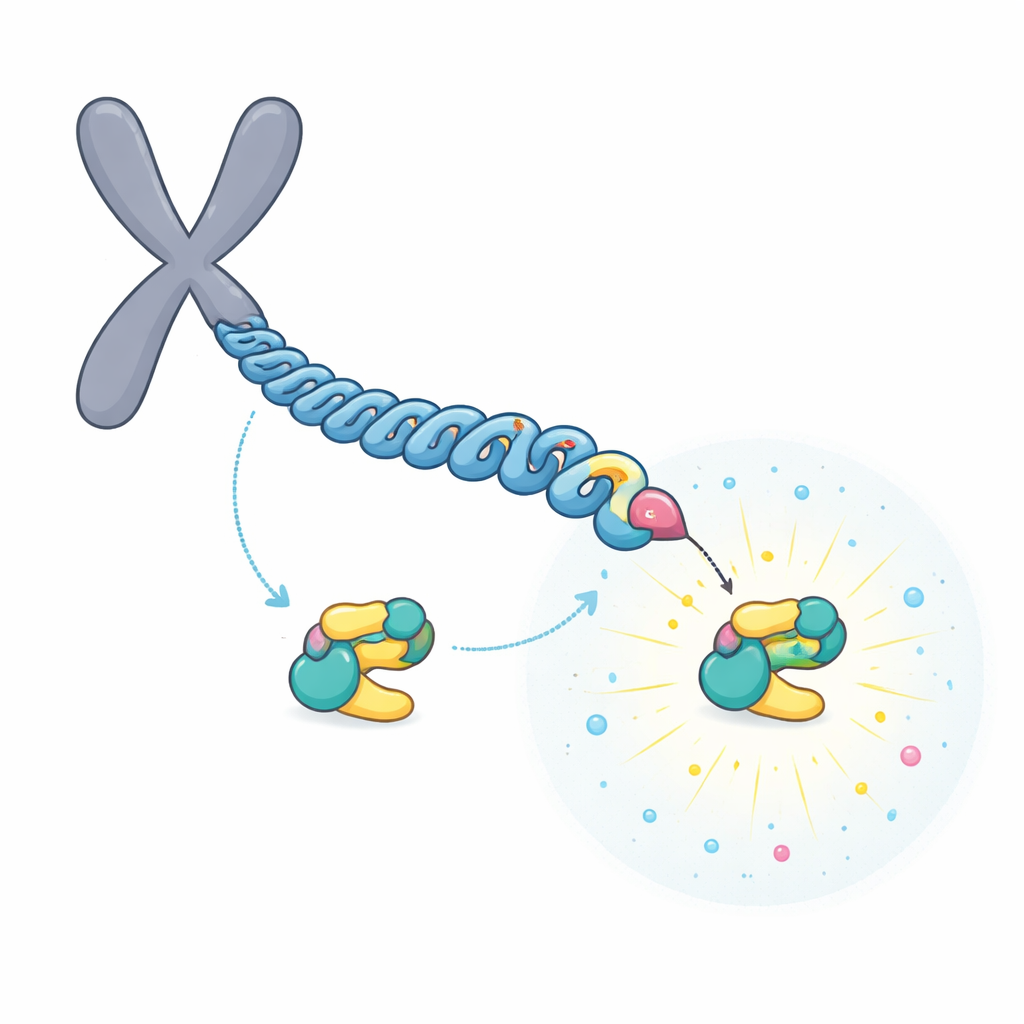
スーパー強力なドッキング部位を作るリレー
チームは染色体付着点の内側に位置するCENP-Uに注目しました。CENP-UはT78とT98と呼ばれるアミノ酸を中心に、近接した二つの潜在的ドッキングモチーフを持っています。生化学実験と質量分析の結果、最初の酵素であるCDK1がT98に容易にリン酸を付加することが示されました。この最初の修飾がPLK1を引き寄せ、PLK1がより不利なT78部位を「リレー」的にリン酸化します。構造データと結合測定は、T78周辺が修飾されると、T98部位に比べて約100倍強くPLK1に結合する非常に強力な着地点になることを示しました。
二つより一つのマスターサイトが優れている
一見すると、二つのリン酸化モチーフの存在は、二つのPLK1分子が並んで結合し互いを安定化することを示唆していました。結晶構造では確かに一つのCENP-U鎖上に二つのポロボックスドメインが座っている様子が示されました。しかし、詳細な結合測定は異なる物語を語りました:第二の部位を追加しても全体の結合が有意に強くなることはなく、むしろわずかに弱くなることさえあり得ました。代わりに著者らは、T78を中心とした単一のサイトが一度形成されれば、それ自体でマスター・ドッキング点として十分に強力であることを発見しました。その強さは二量体化によるものではなく、PLK1の複数のポケットに差し込む大きな接触面から生じます。
強力なドッキングモチーフの共通設計
CENP-U断片を延長し、BUB1、BUBR1、PRC1など他の既知のPLK1パートナーと比較することで、再発するパターンが見えてきました。マスター・モチーフはリン酸化されたアミノ酸を中央のポケットに差し込み、さらに疎水性側鎖を近隣の溝に配置します。その中にはこれまで過小評価されてきた「暗号的」ポケットや隣接する疎水性キャビティも含まれます。AlphaFoldに基づくコンピュータモデルは、いくつかの影響力の大きいPLK1パートナーがポロボックスの周りに似たように巻きつき、複数のポケットを同時に占めることを示唆します。この拡張されたフットプリントは、PLK1を近傍に長く保持して多くの局所標的を修飾することができるマスター・ドッキングモチーフの特徴のように見えます。
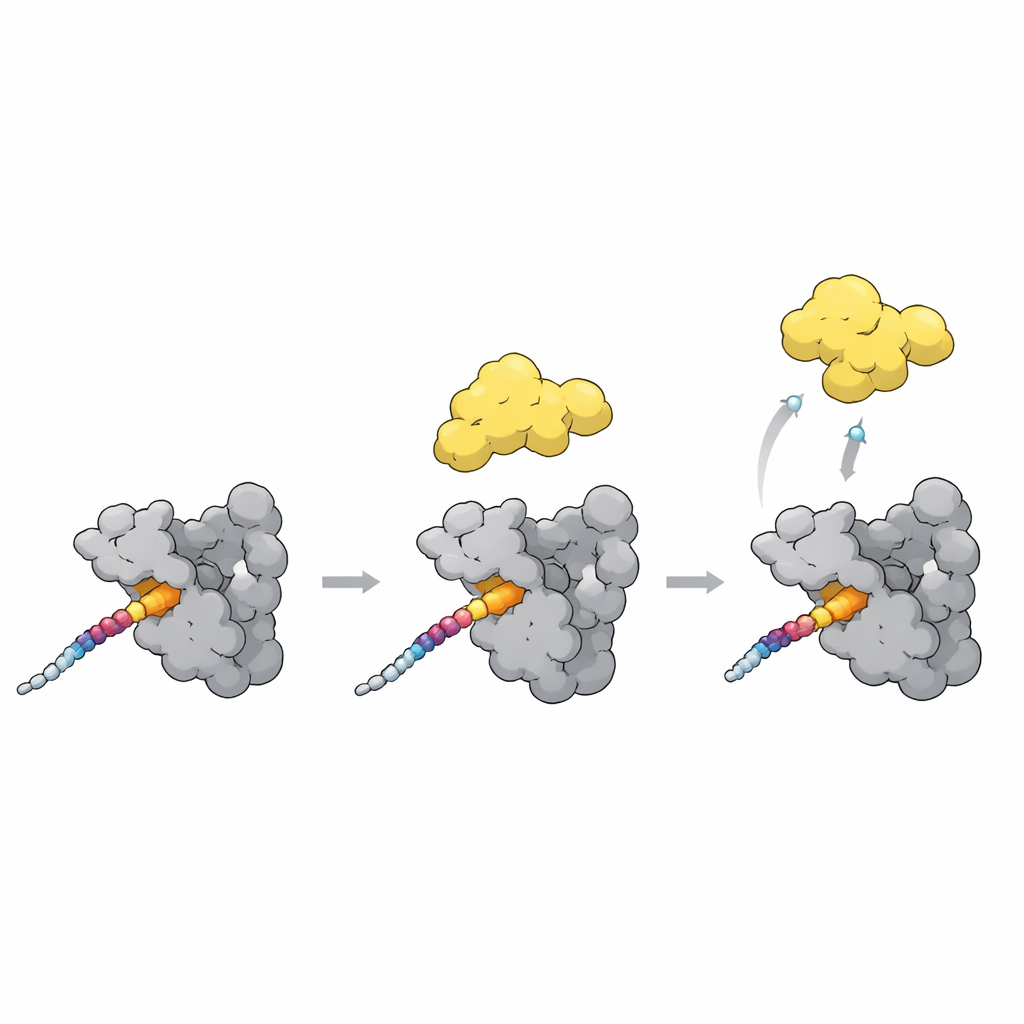
PLK1を閉じた状態から開いた状態へ切り替える
パズルの最終ピースは、ドッキングがPLK1の活性をどのように上げ下げするかという点です。閉じた状態では、ポロボックスドメインがPLK1のキナーゼ部位に寄り添い、それを部分的に閉じたままにします。新しい構造とAlphaFoldモデルは、ポロボックス内の柔軟なループが重要なセンサーであることを示しています。CENP-UのT78のような強力なドッキングモチーフがポロボックス表面にまたがって結合すると、このループが移動してキナーゼを近くに保つリンカーと衝突します。その衝突がPLK1をより開いた、活性な形へと押しやる可能性があります。興味深いことに、天然の阻害タンパク質は同じポケットに結合するものの、むしろ閉じた形を安定化させることで、類似した接触が配置次第でPLK1を解錠したり締め付けたりできることを示しています。
この分子地図が重要な理由
簡単に言えば、本研究はPLK1が染色体上で効果的に働くために二量化を必要としないことを示しています。代わりに、CDK1とPLK1の二段階で作られる単一の綿密に構築されたマスター・ドッキングサイトがPLK1を非常に強く捕らえ、それを活性状態へと反転させ得ます。他のタンパク質上の類似した拡張ドッキングモチーフも同じ手口を使っているようです。これら強力な着地点の分子解剖を明らかにすることで、研究は細胞が主要な分裂酵素を精密に制御する仕組みを説明し、将来PLK1活性をより選択的に調節する薬剤設計の青写真を提供します。
引用: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
キーワード: PLK1, CENP-U, 細胞分裂, キネトコア, タンパク質ドッキング