Clear Sky Science · pt
Anatomia molecular dos motivos mestres de ancoragem da PLK1
Como as células mantêm seus motores de divisão nos trilhos
Cada vez que uma célula se divide, ela precisa copiar e separar seus cromossomos com precisão impressionante. Um ajudante chave nesse processo é uma enzima chamada PLK1, que atua como um controlador de tráfego para os cromossomos em divisão. Este estudo faz uma pergunta simples, porém importante: como a PLK1 sabe exatamente para onde ir e como se ativa no lugar e no momento certos? Ao mapear seus sítios de ancoragem em detalhe atômico, os autores revelam como alguns “andares” mestres especiais dão à PLK1 tanto precisão quanto potência.
Locais de ancoragem direcionados nos cromossomos
A PLK1 carrega um segmento proteico chamado domínio polo-box que funciona como um módulo de ancoragem. Esse domínio reconhece trechos curtos fosforilados em outras proteínas, permitindo que a PLK1 se posicione precisamente onde sua atividade é necessária durante a divisão celular. Trabalhos anteriores mostraram que duas proteínas no sítio de fixação do cromossomo, BUB1 e CENP-U, são especialmente importantes: se seus sítios de ancoragem são removidos, a PLK1 deixa de aparecer nessas estruturas. Os autores suspeitaram que esses motivos mestres podem compartilhar regras de projeto especiais que os distinguem dos muitos sítios de ancoragem mais fracos e temporários espalhados pela célula.
Um revezamento que constrói um sítio de ancoragem superforte
A equipe concentrou-se em CENP-U, que fica na parte interna do ponto de fixação do cromossomo. O CENP-U tem dois motivos de ancoragem potenciais próximos, centrados nos aminoácidos chamados T78 e T98. Experimentos bioquímicos e de espectrometria de massa mostraram que uma primeira enzima, a CDK1, marca prontamente o T98 com um grupo fosfato. Essa marcação inicial atrai a PLK1, que então fosforila o sítio menos favorável T78 em um processo de “revezamento”. Dados estruturais e medidas de ligação revelaram que, uma vez modificada, a região ao redor de T78 torna-se um módulo de ancoragem excepcionalmente forte para a PLK1, ligando-se cerca de 100 vezes com maior afinidade do que o sítio T98.
Um sítio mestre é melhor que dois
A primeira vista, a presença de dois motivos fosforilados sugeria que um par de moléculas de PLK1 poderia se ligar lado a lado e se estabilizar mutuamente. Estruturas cristalinas mostraram de fato dois domínios polo-box assentados em uma única cadeia de CENP-U. No entanto, medidas detalhadas de ligação contaram uma história diferente: adicionar o segundo sítio não fortaleceu significativamente a ligação geral e poderia até torná-la ligeiramente mais fraca. Em vez disso, os autores descobriram que o único sítio centrado em T78, uma vez criado, é forte o suficiente por si só para servir como ponto mestre de ancoragem. Sua força provém de uma grande superfície de contato que se encaixa em vários bolsões na PLK1, em vez de dimerização.
Projeto compartilhado de motivos de ancoragem poderosos
Ao estender o fragmento de CENP-U e compará-lo com outros parceiros conhecidos da PLK1, como BUB1, BUBR1 e PRC1, os pesquisadores observaram um padrão recorrente. Os motivos mestres usam um aminoácido fosforilado para engajar um bolsão central, mas também posicionam cadeias laterais hidrofóbicas em ranhuras próximas, incluindo um bolsão “críptico” previamente pouco apreciado e uma cavidade hidrofóbica vizinha. Modelos computacionais baseados no AlphaFold sugerem que vários parceiros de alto impacto da PLK1 envolvem o polo-box de maneira semelhante, ocupando múltiplos bolsões ao mesmo tempo. Essa impressão digital estendida parece ser a marca registrada dos motivos mestres de ancoragem que conseguem manter a PLK1 próxima por tempo suficiente para modificar muitos alvos locais.
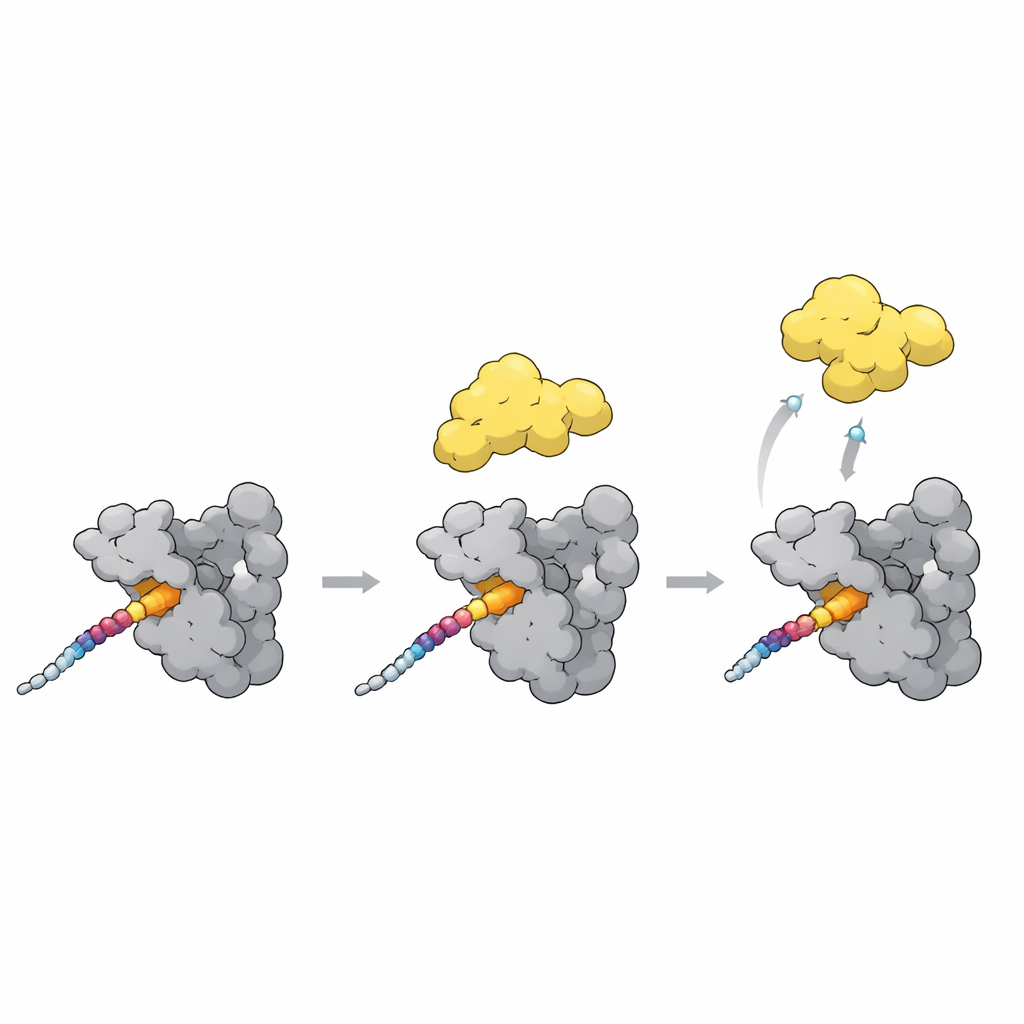
Ligando a PLK1 do estado fechado ao aberto
Uma peça final do quebra-cabeça é como a ancoragem aumenta ou reduz a atividade da PLK1. Em um estado fechado, o domínio polo-box repousa contra a parte quinase da PLK1 e a mantém parcialmente fechada. As novas estruturas, juntamente com modelos do AlphaFold, apontam para uma alça flexível no polo-box como um sensor chave. Quando um motivo de ancoragem forte, como o sítio T78 do CENP-U, se liga à superfície do polo-box, essa alça se desloca e colide com o conector que mantém a quinase próxima. Essa colisão provavelmente empurra a PLK1 para uma forma mais aberta e ativa. Intrigantemente, uma proteína inibidora natural se liga aos mesmos bolsões, mas estabiliza a forma fechada, mostrando que contatos semelhantes podem tanto destravar quanto travar a PLK1 dependendo do arranjo exato.
Por que este mapa molecular importa
Em termos simples, este trabalho mostra que a PLK1 não precisa se duplicar para funcionar efetivamente nos cromossomos. Em vez disso, um único sítio mestre cuidadosamente construído, criado em dois passos pela CDK1 e pela PLK1, pode agarrar a PLK1 com muita afinidade e transformá-la em um estado ativo. Motivos estendidos semelhantes em outras proteínas parecem usar o mesmo truque. Ao revelar a anatomia molecular desses poderosos pontos de ancoragem, o estudo explica como as células alcançam controle preciso sobre uma enzima-chave da divisão e oferece projetos para futuros fármacos que possam ajustar a atividade da PLK1 de forma mais seletiva.
Citação: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Palavras-chave: PLK1, CENP-U, divisão celular, cinetocoro, ancoragem de proteínas