Clear Sky Science · es
Anatomía molecular de los motivos maestros de acoplamiento de PLK1
Cómo las células mantienen a raya sus motores de división
Cada vez que una célula se divide, debe copiar y separar sus cromosomas con una precisión asombrosa. Un ayudante clave en este proceso es una enzima llamada PLK1, que actúa como un controlador de tráfico para los cromosomas en división. Este estudio plantea una pregunta simple pero importante: ¿cómo sabe PLK1 exactamente adónde ir y cómo se activa en el lugar y momento adecuados? Al cartografiar sus sitios de acoplamiento con detalle atómico, los autores muestran cómo unas pocas «plataformas» maestras dan a PLK1 tanto precisión como potencia.
Puntos de aterrizaje dirigidos en los cromosomas
PLK1 lleva un segmento proteico llamado dominio polo-box que actúa como un módulo de acoplamiento. Este dominio reconoce pequeños tramos fosforilados en otras proteínas, permitiendo que PLK1 se ubique precisamente donde su actividad es necesaria durante la división celular. Trabajos previos mostraron que dos proteínas en el sitio de unión cromosómico, BUB1 y CENP-U, son especialmente importantes: si se eliminan sus sitios de acoplamiento, PLK1 deja de aparecer en esas estructuras. Los autores sospecharon que estos motivos «maestros» de acoplamiento podrían compartir reglas de diseño especiales que los distinguen de los muchos sitios de acoplamiento más débiles y temporales dispersos por la célula.
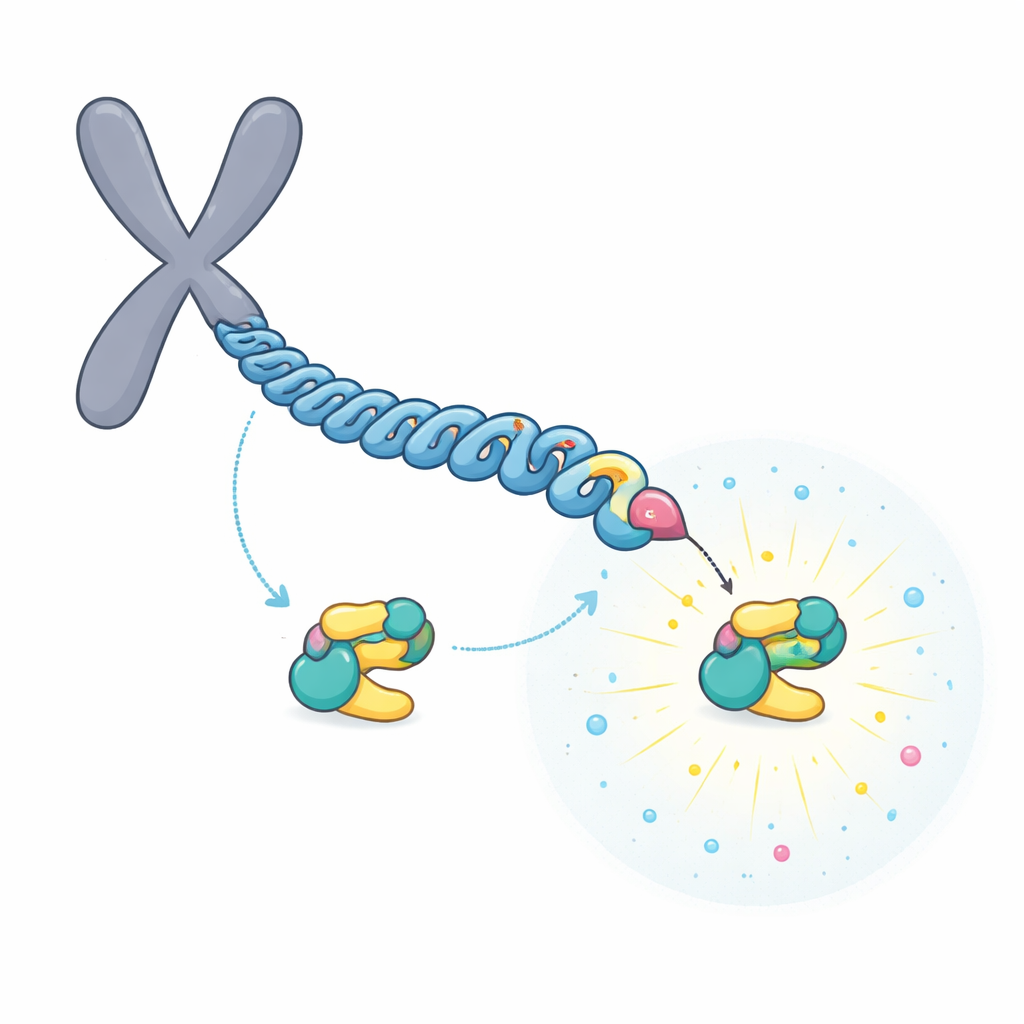
Un relevo que construye un sitio de acoplamiento súper fuerte
El equipo se centró en CENP-U, que se localiza en la parte interna del punto de unión del cromosoma. CENP-U tiene dos motivos de acoplamiento potenciales cercanos, centrados en los aminoácidos denominados T78 y T98. Experimentos bioquímicos y de espectrometría de masas mostraron que una primera enzima, CDK1, etiqueta fácilmente T98 con un grupo fósforo. Esta marcación inicial atrae a PLK1, que a su vez fosforila el sitio menos favorable T78 en un proceso de «relevo». Los datos estructurales y las mediciones de unión revelaron que, una vez modificada, la región alrededor de T78 se convierte en una plataforma de aterrizaje excepcionalmente fuerte para PLK1, uniéndose unas 100 veces con mayor afinidad que el sitio T98.
Un sitio maestro es mejor que dos
A primera vista, la presencia de dos motivos fosforilados sugería que un par de moléculas de PLK1 podrían unirse lado a lado y estabilizarse mutuamente. Estructuras cristalinas mostraron efectivamente dos dominios polo-box sentados en una única cadena de CENP-U. Sin embargo, mediciones detalladas de unión contaron otra historia: añadir el segundo sitio no fortalecía de forma significativa la unión global e incluso podía hacerla ligeramente más débil. En su lugar, los autores encontraron que el único sitio centrado en T78, una vez creado, es lo bastante fuerte por sí solo para servir de punto maestro de acoplamiento. Su fuerza proviene de una gran superficie de contacto que encaja en varios huecos de PLK1, en lugar de depender de una dimerización.
Diseño compartido de motivos de acoplamiento potentes
Al extender el fragmento de CENP-U y compararlo con otros socios conocidos de PLK1 como BUB1, BUBR1 y PRC1, los investigadores observan un patrón recurrente. Los motivos maestros usan un aminoácido fosforilado para enganchar un hueco central, pero también colocan cadenas laterales hidrofóbicas en ranuras cercanas, incluyendo un hueco «críptico» previamente poco valorado y una cavidad hidrofóbica vecina. Modelos por ordenador basados en AlphaFold sugieren que varios socios de alto impacto de PLK1 se envuelven alrededor del polo-box de manera similar, ocupando múltiples huecos a la vez. Esta huella ampliada parece ser una señal distintiva de los motivos maestros de acoplamiento que pueden retener PLK1 el tiempo suficiente para modificar numerosos objetivos locales.
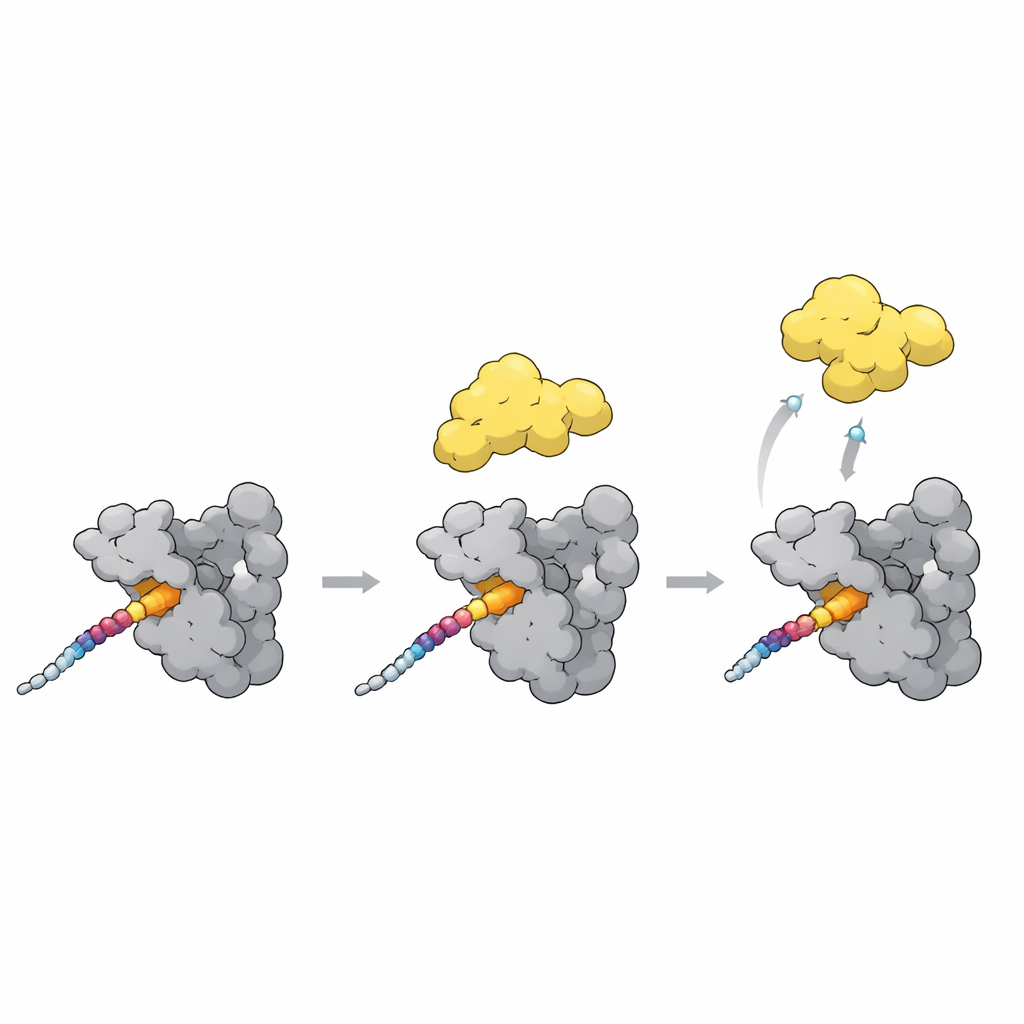
Cómo cambiar a PLK1 de cerrado a abierto
Una pieza final del rompecabezas es cómo el acoplamiento regular la actividad de PLK1. En un estado cerrado, el dominio polo-box se ubica junto a la parte quinasa de PLK1 y la mantiene parcialmente cerrada. Las nuevas estructuras, junto con modelos de AlphaFold, señalan a una lazo flexible en el polo-box como un sensor clave. Cuando un motivo de acoplamiento fuerte como el sitio T78 de CENP-U se une a la superficie del polo-box, este lazo se desplaza y choca con el enlazador que mantiene la quinasa cercana. Ese choque probablemente empuja a PLK1 hacia una conformación más abierta y activa. De forma intrigante, una proteína inhibidora natural se une a los mismos huecos pero estabiliza la forma cerrada, mostrando que contactos similares pueden bien desbloquear o bien inmovilizar a PLK1 según la disposición exacta.
Por qué importa este mapa molecular
En términos simples, este trabajo muestra que PLK1 no necesita duplicarse para funcionar eficazmente en los cromosomas. En lugar de ello, un único sitio maestro cuidadosamente construido, creado en dos pasos por CDK1 y PLK1, puede atrapar a PLK1 con gran firmeza y cambiarlo a un estado activo. Motivos de acoplamiento extendidos similares en otras proteínas parecen usar el mismo truco. Al revelar la anatomía molecular de estas potentes plataformas, el estudio explica cómo las células logran un control preciso sobre una enzima clave de la división y ofrece planos para futuros fármacos que podrían ajustar la actividad de PLK1 de forma más selectiva.
Cita: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Palabras clave: PLK1, CENP-U, división celular, cinetocoro, anclaje de proteínas