Clear Sky Science · de
Molekulare Anatomie der PLK1-Master-Docking-Motive
Wie Zellen ihre Teilungsmaschinen auf Kurs halten
Jedes Mal, wenn eine Zelle sich teilt, muss sie ihre Chromosomen mit verblüffender Präzision kopieren und trennen. Ein wichtiger Helfer in diesem Prozess ist das Enzym PLK1, das wie ein Verkehrslotsen für die teilenden Chromosomen wirkt. Die Studie stellt eine einfache, aber zentrale Frage: Wie weiß PLK1 genau, wohin es gehen soll, und wie wird es am richtigen Ort zur richtigen Zeit aktiviert? Durch das kartografische Aufschlüsseln seiner Andockstellen bis auf atomare Details zeigen die Autoren, wie einige wenige spezielle „Master“-Landezonen PLK1 sowohl Genauigkeit als auch Schlagkraft verleihen.
Gezielte Landezonen auf Chromosomen
PLK1 trägt ein Proteinsegment, die Polo‑Box‑Domäne, das als Andockmodul fungiert. Diese Domäne erkennt kurze phosphorylierte Abschnitte auf anderen Proteinen und erlaubt PLK1, genau dort zu binden, wo seine Aktivität während der Zellteilung gebraucht wird. Frühere Arbeiten zeigten, dass zwei Proteine am Chromosomen‑Anheftungspunkt, BUB1 und CENP‑U, besonders wichtig sind: Werden ihre Andockstellen entfernt, erscheint PLK1 nicht mehr an diesen Strukturen. Die Autoren vermuteten, dass diese „Master“-Docking‑Motive gemeinsame Gestaltungsprinzipien haben könnten, die sie von den vielen schwächeren, vorübergehenden Andockstellen in der Zelle unterscheiden.
Ein Relay, das eine superstarke Andockstelle aufbaut
Das Team konzentrierte sich auf CENP‑U, das im inneren Teil des Chromosomen‑Anheftungspunkts sitzt. CENP‑U besitzt zwei benachbarte potenzielle Dockingmotive, zentriert um die Aminosäuren T78 und T98. Biochemische und Massenspektrometrie‑Experimente zeigten, dass ein erstes Enzym, CDK1, T98 leicht mit einer Phosphatgruppe versieht. Diese erste Markierung zieht PLK1 an, das dann in einem „Relay“-Prozess das weniger günstige T78 phosphoryliert. Strukturdaten und Bindungsmessungen enthüllten, dass die Region um T78 nach dieser Modifikation zu einer außergewöhnlich starken Landezone für PLK1 wird und etwa 100‑mal fester bindet als die T98‑Stelle.
Eine Masterstelle ist besser als zwei
Auf den ersten Blick deutete das Vorhandensein zweier phosphorylierter Motive darauf hin, dass zwei PLK1‑Moleküle nebeneinander binden und sich gegenseitig stabilisieren könnten. Kristallstrukturen zeigten tatsächlich zwei Polo‑Box‑Domänen, die an einer einzigen CENP‑U‑Kette sitzen. Detaillierte Bindungsmessungen erzählten jedoch eine andere Geschichte: Das Hinzufügen der zweiten Stelle verstärkte die Gesamtbindung nicht signifikant und konnte sie sogar leicht abschwächen. Stattdessen fanden die Autoren, dass die einzelne, um T78 zentrierte Stelle, einmal gebildet, ausreicht, um als Master‑Andockpunkt zu dienen. Ihre Stärke rührt von einer großen Kontaktfläche her, die mehrere Taschen auf PLK1 ausfüllt, und nicht von einer Dimerisierung.
Geteilte Gestaltung mächtiger Dockingmotive
Indem sie das CENP‑U‑Fragment verlängerten und mit anderen bekannten PLK1‑Partnern wie BUB1, BUBR1 und PRC1 verglichen, entdeckten die Forscher ein wiederkehrendes Muster. Mastermotive nutzen eine phosphorylierte Aminosäure, um eine zentrale Tasche zu besetzen, platzieren aber zugleich hydrophobe Seitenketten in benachbarten Rillen, einschließlich einer zuvor unterschätzten „kryptischen“ Tasche und einer angrenzenden hydrophoben Kavität. Computermodelle auf der Basis von AlphaFold legen nahe, dass mehrere PLK1‑Partner mit großer Wirkung die Polo‑Box auf ähnliche Weise umschließen und mehrere Taschen gleichzeitig belegen. Diese erweiterte Kontaktfläche scheint ein Kennzeichen von Master‑Dockingmotiven zu sein, die PLK1 lange genug in der Nähe festhalten können, um zahlreiche lokale Ziele zu modifizieren.
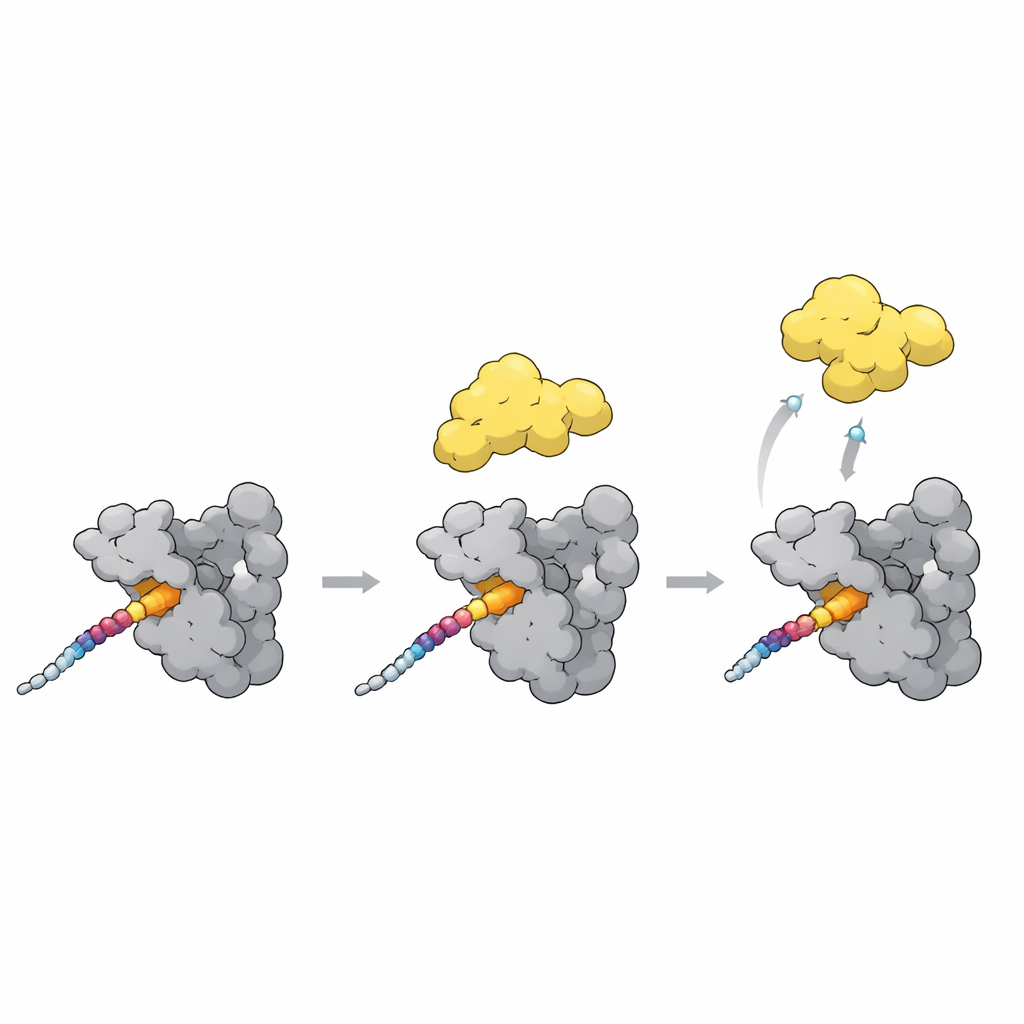
PLK1 vom geschlossenen in den offenen Zustand schalten
Ein letztes Puzzleteil ist, wie Andocken die Aktivität von PLK1 hoch- oder herunterregelt. Im geschlossenen Zustand liegt die Polo‑Box‑Domäne an der Kinaseeinheit von PLK1 an und hält sie teilweise verschlossen. Die neuen Strukturen zusammen mit AlphaFold‑Modellen zeigen eine flexible Schleife in der Polo‑Box als wichtigen Sensor. Wenn ein starkes Dockingmotiv wie die T78‑Stelle auf CENP‑U über die Polo‑Box‑Oberfläche bindet, verschiebt sich diese Schleife und kollidiert mit dem Linker, der die Kinase nahehält. Diese Kollision dürfte PLK1 in eine offenere, aktivere Form schieben. Erstaunlicherweise bindet ein natürlicher Inhibitor dieselben Taschen, stabilisiert aber stattdessen die geschlossene Form, was zeigt, dass ähnliche Kontakte PLK1 je nach genauer Anordnung entweder entriegeln oder versperren können.
Warum diese molekulare Karte wichtig ist
Einfach ausgedrückt zeigt diese Arbeit, dass PLK1 nicht verdoppelt werden muss, um an Chromosomen effektiv zu arbeiten. Stattdessen kann eine einzelne, sorgfältig aufgebaute Master‑Andockstelle, die in zwei Schritten von CDK1 und PLK1 erzeugt wird, PLK1 sehr fest binden und in einen aktiven Zustand umschalten. Ähnliche erweiterte Dockingmotive auf anderen Proteinen scheinen denselben Trick zu nutzen. Indem die Studie die molekulare Anatomie dieser mächtigen Landezonen offenlegt, erklärt sie, wie Zellen die präzise Kontrolle über ein zentrales Teilungsenzym erreichen, und liefert Blaupausen für künftige Wirkstoffe, die PLK1‑Aktivität gezielter modulieren könnten.
Zitation: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Schlüsselwörter: PLK1, CENP-U, Zellteilung, Kinetochor, Protein‑Andocken