Clear Sky Science · it
Anatomia molecolare dei motivi master di aggancio di PLK1
Come le cellule mantengono il loro motore di divisione sulla giusta traiettoria
Ogni volta che una cellula si divide, deve copiare e separare i cromosomi con sorprendente precisione. Un aiuto chiave in questo processo è un enzima chiamato PLK1, che agisce come un controllore del traffico per i cromosomi in divisione. Questo studio pone una domanda semplice ma importante: come fa PLK1 a sapere esattamente dove andare e come si attiva nel luogo e nel momento giusti? Mappando i suoi siti di aggancio in dettaglio atomico, gli autori rivelano come pochi speciali "docking" master conferiscano a PLK1 sia accuratezza sia potenza.
Siti di atterraggio mirati sui cromosomi
PLK1 porta un segmento proteico chiamato dominio polo-box che agisce come modulo di aggancio. Questo dominio riconosce brevi porzioni fosforilate su altre proteine, permettendo a PLK1 di posizionarsi precisamente dove la sua attività è necessaria durante la divisione cellulare. Lavori precedenti avevano mostrato che due proteine nel sito di attacco del cromosoma, BUB1 e CENP-U, sono particolarmente importanti: se i loro siti di aggancio vengono rimossi, PLK1 non compare più in quelle strutture. Gli autori hanno ipotizzato che questi motivi "master" possano condividere regole di progettazione particolari che li distinguono dai molti siti di aggancio più deboli e temporanei sparsi nella cellula.
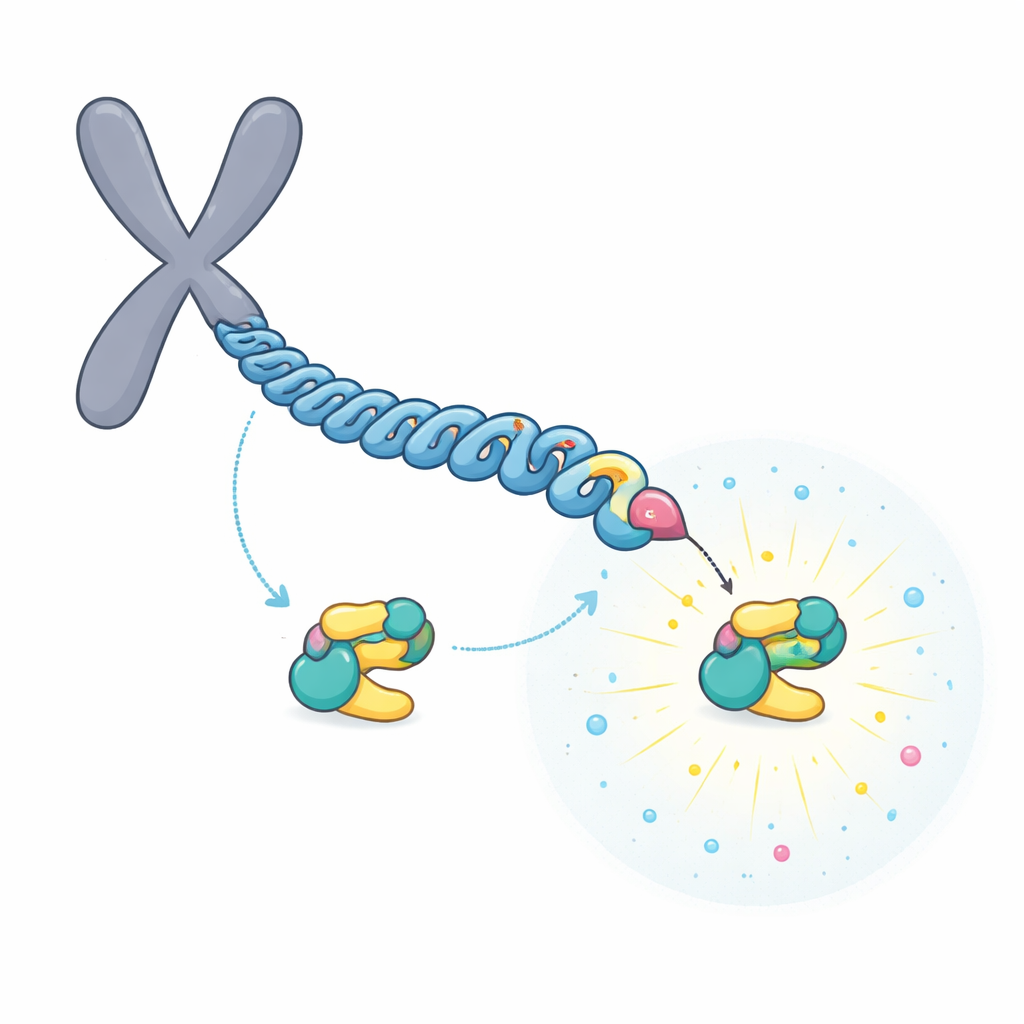
Una staffetta che costruisce un sito di aggancio super-forte
Il gruppo si è concentrato su CENP-U, che si trova nella parte interna del punto di attacco del cromosoma. CENP-U presenta due potenziali motivi di aggancio vicini, centrati sugli amminoacidi chiamati T78 e T98. Esperimenti biochimici e di spettrometria di massa hanno mostrato che un primo enzima, CDK1, fosforila prontamente T98. Questa fosforilazione iniziale attira PLK1, che a sua volta fosforila il sito meno favorevole T78 in un processo a "staffetta". Dati strutturali e misure di legame hanno rivelato che, una volta modificata, la regione intorno a T78 diventa un sito di atterraggio eccezionalmente forte per PLK1, legando circa 100 volte più strettamente rispetto al sito T98.
Un sito master è meglio di due
A prima vista, la presenza di due motivi fosforilati suggeriva che una coppia di molecole PLK1 potesse legarsi fianco a fianco e stabilizzarsi a vicenda. Le strutture cristalline mostrarono infatti due domini polo-box seduti su una singola catena di CENP-U. Tuttavia, misurazioni di legame dettagliate raccontarono una storia diversa: l'aggiunta del secondo sito non rafforzava in modo significativo il legame complessivo e poteva perfino renderlo leggermente più debole. Gli autori hanno invece scoperto che il singolo sito centrato su T78, una volta creato, è sufficientemente forte da servire da punto master di aggancio da solo. La sua forza deriva da una larga superficie di contatto che si inserisce in diverse tasche su PLK1, piuttosto che dalla dimerizzazione.
Progetto condiviso dei motivi di aggancio potenti
Estendendo il frammento di CENP-U e confrontandolo con altri noti partner di PLK1 come BUB1, BUBR1 e PRC1, i ricercatori hanno osservato un modello ricorrente. I motivi master utilizzano un amminoacido fosforilato per impegnare una tasca centrale, ma dispongono anche catene laterali idrofobiche in scanalature vicine, inclusa una tasca "criptica" precedentemente sottovalutata e una cavità idrofobica adiacente. Modelli al computer basati su AlphaFold suggeriscono che diversi partner di PLK1 ad alto impatto avvolgano il polo-box in modo simile, occupando più tasche contemporaneamente. Questa impronta estesa sembra essere un marchio distintivo dei motivi master che possono trattenere PLK1 nelle vicinanze abbastanza a lungo da modificare molti bersagli locali.
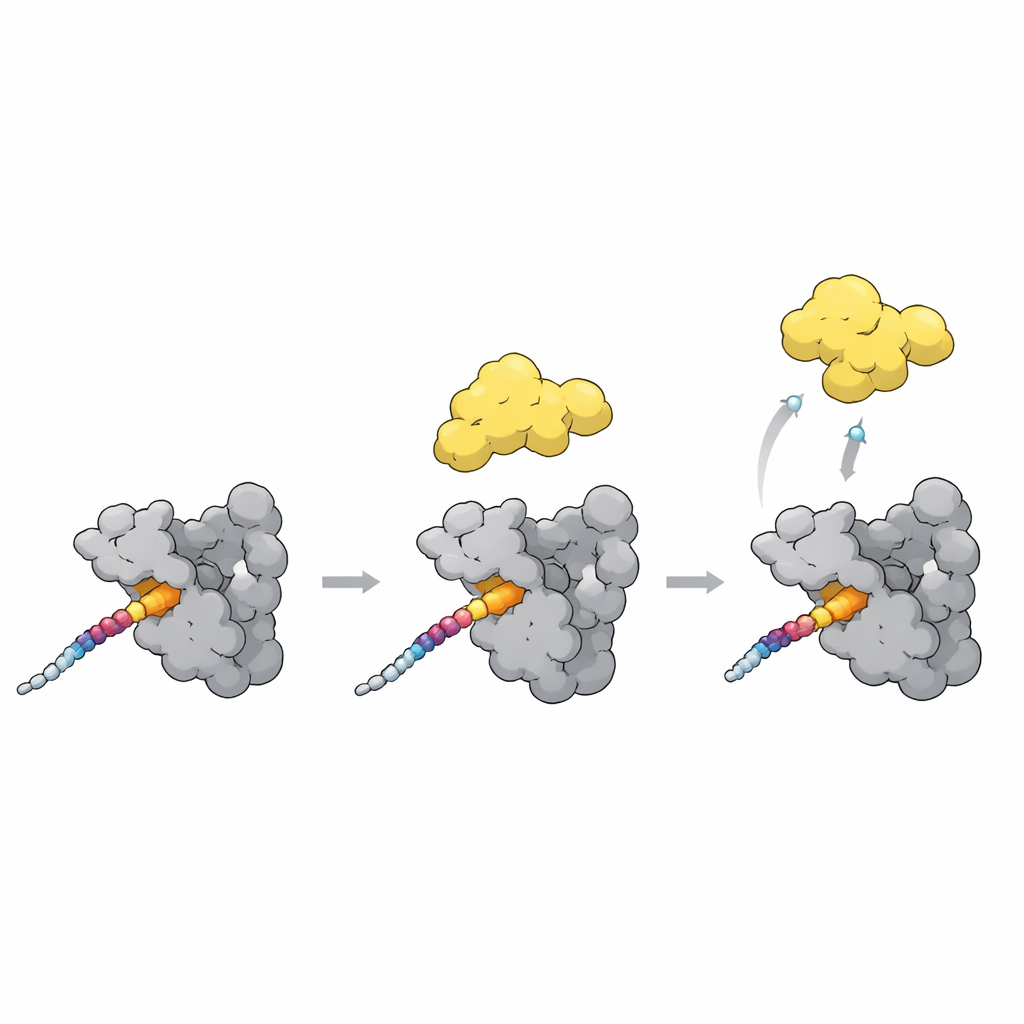
Da PLK1 chiuso a PLK1 aperto
Un ultimo pezzo del puzzle è come l'aggancio aumenti o diminuisca l'attività di PLK1. In uno stato chiuso, il dominio polo-box si appoggia contro la parte chinasi di PLK1 e la mantiene parzialmente chiusa. Le nuove strutture, insieme ai modelli AlphaFold, indicano un anello flessibile nel polo-box come sensore chiave. Quando un motivo di aggancio forte come il sito T78 su CENP-U si lega estendendosi sulla superficie del polo-box, questo anello si sposta e entra in collisione con il linker che tiene vicina la chinasi. Questa collisione probabilmente spinge PLK1 in una forma più aperta e attiva. In modo intrigante, una proteina inibitrice naturale si lega alle stesse tasche ma stabilizza invece la forma chiusa, mostrando che contatti simili possono sia sbloccare sia comprimere PLK1 a seconda dell'esatta disposizione.
Perché questa mappa molecolare è importante
In termini semplici, questo lavoro mostra che PLK1 non ha bisogno di duplicarsi per funzionare efficacemente sui cromosomi. Piuttosto, un singolo e accuratamente costruito sito master di aggancio, creato in due passaggi da CDK1 e PLK1, può catturare PLK1 molto saldamente e ribaltarlo in uno stato attivo. Motivi di aggancio estesi simili su altre proteine sembrano usare lo stesso trucco. Rivelando l'anatomia molecolare di queste potenti piattaforme di atterraggio, lo studio spiega come le cellule ottengano un controllo preciso su un enzima chiave della divisione e offre progetti per futuri farmaci che potrebbero modulare l'attività di PLK1 in modo più selettivo.
Citazione: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Parole chiave: PLK1, CENP-U, divisione cellulare, chetocore, aggancio proteico