Clear Sky Science · ar
التشريح الجزيئي لمواقع الإرساء الرئيسية لـ PLK1
كيف تحافظ الخلايا على دقة محركات الانقسام
في كل مرة تنقسم فيها الخلية، يجب أن تنسخ فصل كروموسوماتها وتفصلها بدقة مذهلة. مساعد رئيسي في هذه العملية هو إنزيم يُسمى PLK1، الذي يعمل كمنسق لحركة الكروموسومات أثناء الانقسام. يطرح هذا البحث سؤالاً بسيطًا ولكنه مهمًا: كيف يعرف PLK1 المكان الدقيق الذي يجب أن يتوجه إليه، وكيف ينشغل في المكان والوقت المناسبين؟ من خلال رسم مواقع إرسائه بتفاصيل ذرية، يكشف المؤلفون كيف تمنح بعض «مهابط» الإرساء الخاصة PLK1 كلًا من الدقة والقوة.
مواقع إرساء موجهة على الكروموسومات
يحمل PLK1 قطعة بروتينية تسمى دومين بوكس البولّو تعمل كوحدة إرساء. يتعرف هذا الدومين على تسلسلات قصيرة مفسفرة على بروتينات أخرى، مما يسمح لـ PLK1 بالتوقف بدقة حيث يلزم نشاطه أثناء انقسام الخلية. أظهرت أعمال سابقة أن بروتينين في موقع ارتكاز الكروموسوم، BUB1 وCENP-U، مهمان بشكل خاص: إذا أُزيلت مواقع إرسائهما، لا يظهر PLK1 عند تلك البنى. شكّ المؤلفون في أن هذه الموتيفات «الرئيسية» قد تتشارك قواعد تصميم خاصة تميّزها عن مواقع الإرساء الأضعف والأكثر مؤقتية المنتشرة في الخلية.
تتابع يبني موقع إرساء فائق القوة
ركّز الفريق على CENP-U، الموجود في الجزء الداخلي لنقطة ارتكاز الكروموسوم. لدى CENP-U موتيفان محتملان للإرساء متقاربان، مركزان على الأحماض الأمينية المسماة T78 وT98. أظهرت تجارب كيمياء حيوية وقياسات مطيافية الكتلة أن إنزيمًا أوليًا، CDK1، يفسفر بسهولة T98 بوضع مجموعة فوسفات. تجذب هذه الإشارة الأولية PLK1، الذي يقوم بعد ذلك بفوسفرة الموقع الأقل ملاءمة T78 في عملية «تتابع». أظهرت البيانات الهيكلية وقياسات الارتباط أنه بمجرد التعديل، تصبح المنطقة حول T78 مهبطًا استثنائيًا قويًا لـ PLK1، بقدرة ارتباط أقوى بحوالي 100 مرة من موقع T98.
موقع رئيسي واحد أفضل من اثنين
للوهلة الأولى، اقترح وجود موتيفين مفسفرين أن زوجًا من جزيئات PLK1 قد يرتبط جنبًا إلى جنب ويثبّت كلًا منهما الآخر. أظهرت البلورات بالفعل وجود دوميني بوكس بولّو اثنين جالسين على سلسلة واحدة من CENP-U. ومع ذلك، أخبرت قياسات الارتباط التفصيلية قصة مختلفة: إضافة الموقع الثاني لم تقوِّ الارتباط الكلي بشكل كبير وقد تجعله أضعف قليلًا. بدلاً من ذلك، وجد المؤلفون أن الموقع المفترض حول T78، بمجرد تكوينه، قوي بما يكفي لوحده ليعمل كنقطة الإرساء الرئيسية. تأتي قوته من سطح اتصال واسع يندمج في عدة جيوب على PLK1، بدلاً من الاعتماد على ازدواجية الروابط.
تصميم مشترك لموتيفات إرساء قوية
بتمديد قطعة CENP-U ومقارنتها مع شركاء PLK1 المعروفين الآخرين مثل BUB1 وBUBR1 وPRC1، لاحظ الباحثون نمطًا متكررًا. تستخدم الموتيفات الرئيسية حمضًا أمينيًا مفسفرًا للانخراط في جيب مركزي، لكنها أيضًا تضع سلاسل جانبية هيدروفوبية في أخاديد قريبة، بما في ذلك «جيب خفي» كان يقل تقديره سابقًا وتجويف هيدروفوبي مجاور. تشير نماذج الحاسوب المبنية على AlphaFold إلى أن عدة شركاء ذوي تأثير عالٍ على PLK1 يلتفون حول دومين بوكس البولّو بشكل مماثل، محتلين عدة جيوب في آن واحد. يبدو أن هذه البصمة الموسعة سمة مميزة لموتيفات الإرساء الرئيسية القادرة على إبقاء PLK1 قريبًا لفترة كافية لتعديل العديد من الأهداف المحلية.
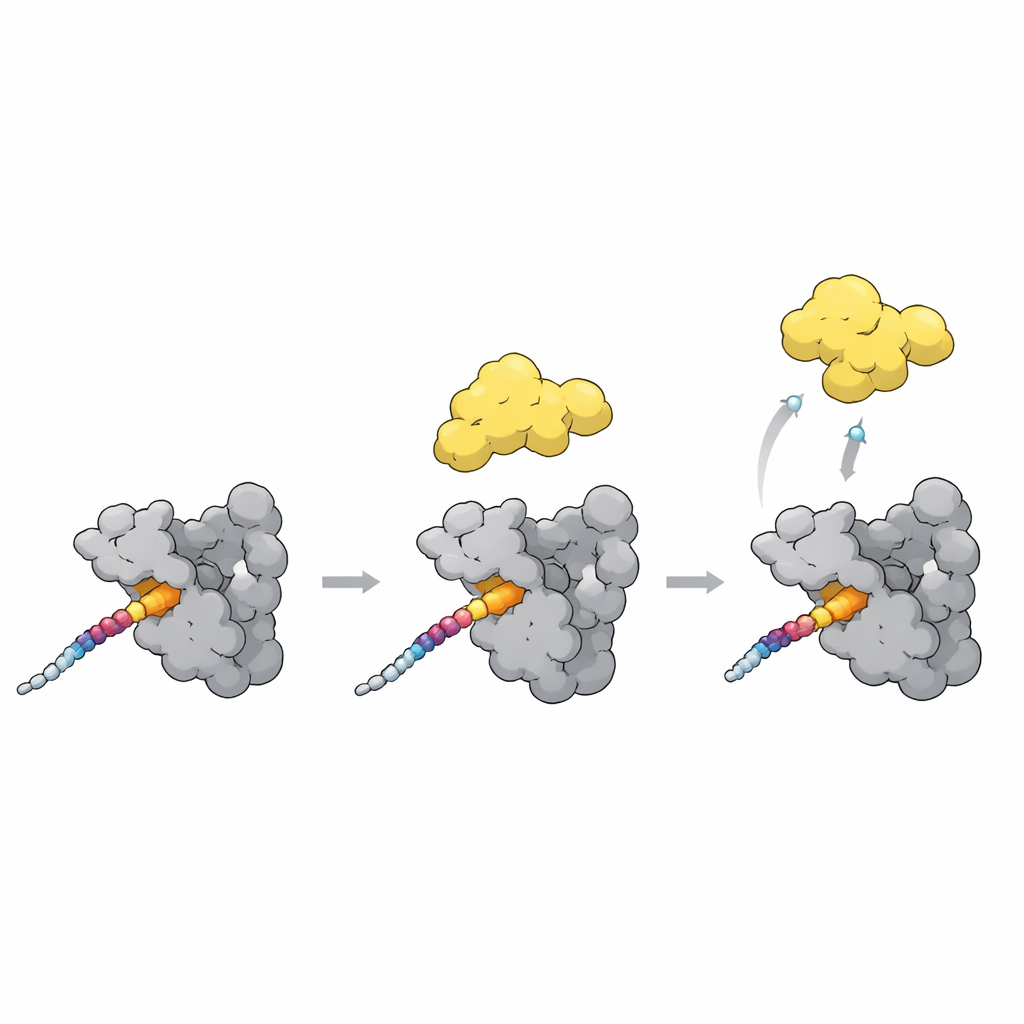
تحويل PLK1 من الشكل المغلق إلى المفتوح
قطعة أخيرة من اللغز هي كيف يزيد الإرساء أو يخفض نشاط PLK1. في الحالة المغلقة، يستقر دومين بوكس البولّو مقابل جزء الكيناز في PLK1 ويبقيه جزئيًا مغلقًا. تشير الهياكل الجديدة، جنبًا إلى جنب مع نماذج AlphaFold، إلى حلقة مرنة في دومين بوكس تعمل كمستشعر أساسي. عندما يرتبط موتيف إرساء قوي مثل موقع T78 على CENP-U عبر سطح البولّو بوكس، تتحرك هذه الحلقة وتصطدم بالموصل الذي يربط الكيناز بالقرب منه. من المحتمل أن هذه الاصطدامات تدفع PLK1 إلى شكل أكثر انفتاحًا ونشاطًا. ومن المثير للاهتمام أن بروتينًا طبيعيًا مثبطًا يرتبط بنفس الجيوب لكنه يثبت الشكل المغلق بدلًا من ذلك، مما يبيّن أن اتصالات مماثلة يمكن إما أن تفتح أو تثبّت PLK1 اعتمادًا على الترتيب الدقيق.
لماذا تهم هذه الخريطة الجزيئية
بعبارات بسيطة، يوضح هذا العمل أن PLK1 لا يحتاج إلى الازدواجية ليعمل بفعالية عند الكروموسومات. بدلًا من ذلك، يمكن لموقع إرساء رئيسي واحد مُبنى بعناية، يتم إنشاؤه على مرحلتين بواسطة CDK1 وPLK1، أن يمسك PLK1 بقوة ويقلبه إلى حالة نشطة. يبدو أن موتيفات الإرساء الموسعة المماثلة على بروتينات أخرى تستخدم نفس الخدعة. من خلال كشف التشريح الجزيئي لهذه المهابط القوية، يشرح البحث كيف تحقق الخلايا تحكمًا دقيقًا في إنزيم الانقسام الرئيسي ويقدّم مخططات أولية لأدوية مستقبلية قد تضبط نشاط PLK1 بشكل أكثر انتقائية.
الاستشهاد: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
الكلمات المفتاحية: PLK1, CENP-U, انقسام الخلية, الكنيتوكور, إرساء البروتين