Clear Sky Science · sv
Molekylär anatomi för PLK1:s huvudsakliga dockningsmotif
Hur celler håller sina delningsmaskiner på rätt spår
Varje gång en cell delar sig måste den kopiera och separera sina kromosomer med häpnadsväckande precision. En viktig hjälpare i denna process är ett enzym som kallas PLK1, som fungerar som en trafikledare för de delande kromosomerna. Denna studie ställer en enkel men viktig fråga: hur vet PLK1 exakt vart det ska gå, och hur slås det på på rätt plats och vid rätt tidpunkt? Genom att kartlägga dess dockningsställen i atomär detalj visar författarna hur några få speciella ”huvud” landningsplatser ger PLK1 både precision och kraft.
Målinriktade landningsplatser på kromosomerna
PLK1 bär på ett proteinsegment kallat polo-box-domän som fungerar som en dockningsmodul. Denna domän känner igen korta, fosforylerade sekvenser på andra proteiner, vilket tillåter PLK1 att parkera precis där dess aktivitet behövs under celldelningen. Tidigare arbete visade att två proteiner vid kromosomernas fästpunkter, BUB1 och CENP-U, är särskilt viktiga: om deras dockningsställen tas bort syns inte PLK1 längre vid dessa strukturer. Författarna misstänkte att dessa ”huvud” dockningsmotif kan dela särskilda designregler som skiljer dem från de många svagare, mer tillfälliga dockningsställena utspridda i cellen.
En relay som bygger en superstark dockningsplats
Teamet fokuserade på CENP-U, som sitter i den inre delen av kromosomens fästpunkt. CENP-U har två närliggande potentiella dockningsmotif, centrerade på aminosyrorna kallade T78 och T98. Biokemiska och masspektrometriska experiment visade att ett första enzym, CDK1, lätt sätter en fosfatgrupp på T98. Denna inledande märkning lockar PLK1, som sedan fosforylerar den mindre gynnade T78-platsen i en ”relay”-process. Strukturella data och bindningsmätningar avslöjade att, när den väl modifierats, blir området kring T78 en exceptionellt stark landningsplatta för PLK1 och binder cirka 100 gånger starkare än T98-platsen.
En huvudplats är bättre än två
Vid första anblick antydde förekomsten av två fosforylerade motiv att ett par PLK1-molekyler kanske binder sida vid sida och stabiliserar varandra. Kristallstrukturer visade faktiskt två polo-box-domäner sittande på en enda CENP-U-kedja. Men detaljerade bindningsmätningar berättade en annan historia: att lägga till den andra platsen stärkte inte den totala bindningen märkbart och kunde till och med göra den något svagare. Istället fann författarna att den enskilda T78-centrerade platsen, när den väl skapats, är tillräckligt stark för att ensam fungera som huvud-dockningspunkt. Dess styrka kommer från en stor kontaktyta som låser in sig i flera fickor på PLK1, snarare än från dimerisering.
Delad utformning hos kraftfulla dockningsmotif
Genom att förlänga CENP-U-fragmentet och jämföra det med andra kända PLK1-partners som BUB1, BUBR1 och PRC1, såg forskarna ett återkommande mönster. Huvudmotif använder en fosforylerad aminosyra för att engagera en central ficka, men placerar också hydrofoba sidokedjor i närliggande spår, inklusive en tidigare underskattad ”kryptisk” ficka och ett intilliggande hydrofobt hålrum. Datorbaserade modeller med AlphaFold tyder på att flera högpåverkande PLK1-partners sveper runt polo-boxen på ett liknande sätt och ockuperar flera fickor samtidigt. Detta utvidgade fotavtryck verkar vara ett kännetecken för huvud-dockningsmotif som kan hålla PLK1 i närheten tillräckligt länge för att modifiera många lokala mål.
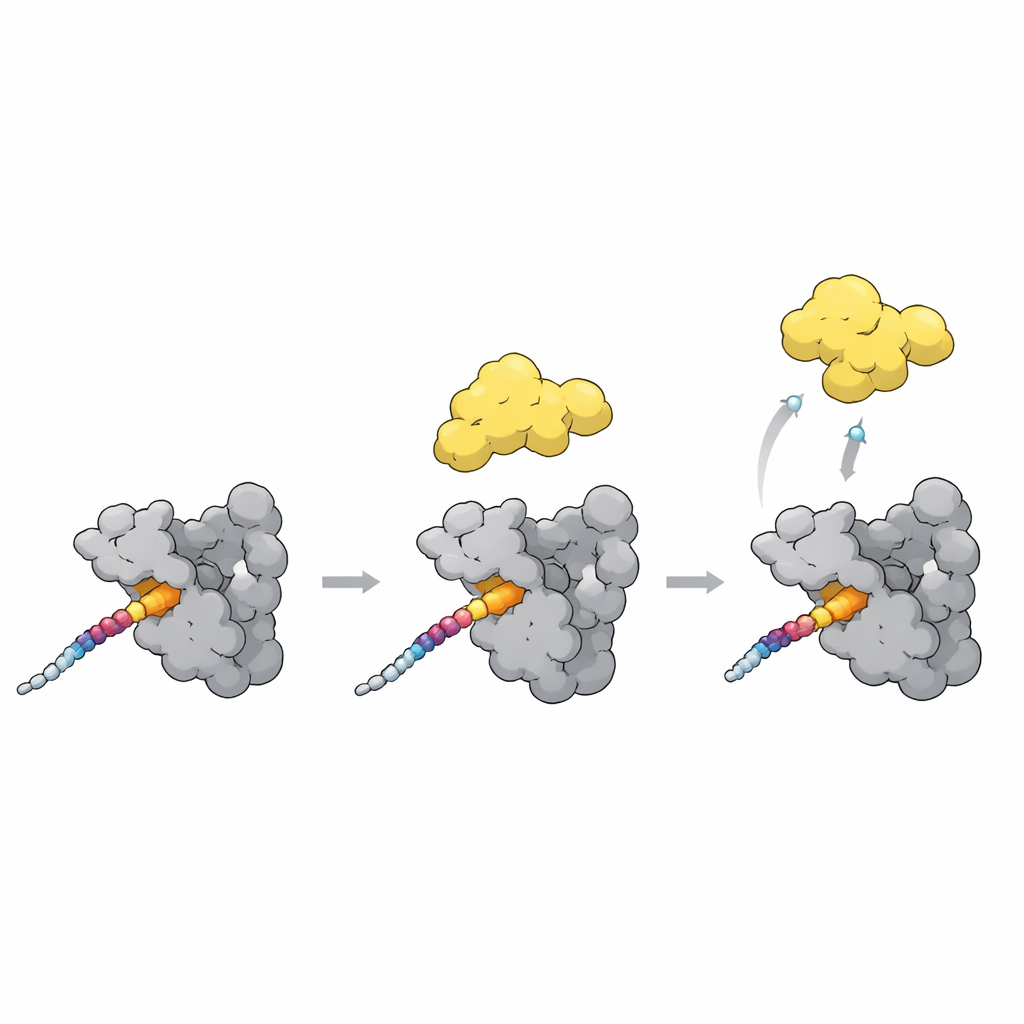
Att växla PLK1 från stängt till öppet
En sista pusselbit är hur dockning höjer eller sänker PLK1:s aktivitet. I ett stängt tillstånd ligger polo-box-domänen intill kinasedelen av PLK1 och håller den delvis stängd. De nya strukturerna, tillsammans med AlphaFold-modeller, pekar på en flexibel slinga i polo-boxen som en nyckelsensor. När en stark dockningsmotif som T78-platsen på CENP-U binder över polo-boxens yta, flyttar denna slinga och kolliderar med länken som håller kinasen nära. Den kollisionen skjuter sannolikt PLK1 mot en mer öppen, aktiv form. Intressant nog binder ett naturligt inhibitorprotein till samma fickor men stabiliserar istället den stängda formen, vilket visar att liknande kontakter antingen kan låsa upp eller spärra PLK1 beroende på den exakta arrangemanget.
Varför denna molekylära karta är viktig
Enkelt uttryckt visar detta arbete att PLK1 inte behöver dubbleras för att fungera effektivt vid kromosomer. Istället kan en enskild, omsorgsfullt uppbyggd huvud-dockningsplats, skapad i två steg av CDK1 och PLK1, fånga PLK1 mycket tätt och växla det till ett aktivt tillstånd. Liknande utvidgade dockningsmotif på andra proteiner tycks använda samma knep. Genom att avslöja den molekylära anatomien hos dessa kraftfulla landningsplatser förklarar studien hur celler uppnår precis kontroll över ett nyckelenzym i delningen och erbjuder ritningar för framtida läkemedel som kan justera PLK1-aktivitet mer selektivt.
Citering: Ren, L., Esposito-Verza, A., Gasper, R. et al. Molecular anatomy of PLK1 master docking motifs. Nat Commun 17, 4228 (2026). https://doi.org/10.1038/s41467-026-73038-8
Nyckelord: PLK1, CENP-U, celldelning, kinetokor, proteindockning